名校
1 . 一定量的 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: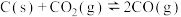 。平衡时,体系中气体体积分数与温度的关系如图所示:
。平衡时,体系中气体体积分数与温度的关系如图所示:
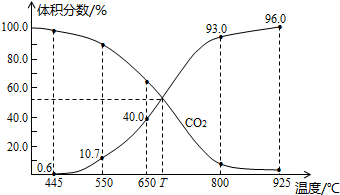
已知:气体分压(p分)=气体总压(p总)×体积分数
下列说法正确的是
 与足量的碳在体积可变的恒压密闭容器中反应:
与足量的碳在体积可变的恒压密闭容器中反应: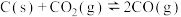 。平衡时,体系中气体体积分数与温度的关系如图所示:
。平衡时,体系中气体体积分数与温度的关系如图所示:
已知:气体分压(p分)=气体总压(p总)×体积分数
下列说法正确的是
A. 时,若充入惰性气体,V正,V逆均减小,平衡不移动 时,若充入惰性气体,V正,V逆均减小,平衡不移动 |
B. 时,反应达平衡后 时,反应达平衡后 的转化率为 的转化率为 |
C. 时,若充入等体积的 时,若充入等体积的 和 和 ,平衡向逆反应方向移动 ,平衡向逆反应方向移动 |
D.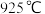 时,化学平衡常数 时,化学平衡常数 |
您最近一年使用:0次
解题方法
2 . 对于反应N2O4(g)⇌2NO2(g),在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示。下列说法中,正确的是


| A.A、C两点对应状态的正反应速率大小关系为vA<vC |
| B.A、B、C、D、E各点对应状态中,v(正)<v(逆)的是B |
| C.维持p1不变,E→A所需时间为t1;维持p2不变,D→C所需时间为t2,则t1=t2 |
| D.欲使E状态从水平方向到达C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的方法是从pl迅速加压至p2,再由p2无限缓慢降压至p1 |
您最近一年使用:0次
名校
解题方法
3 . 某化学研究小组探究外界条件对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响,图象如下,下列判断正确的是()
pC(g)的速率和平衡的影响,图象如下,下列判断正确的是()
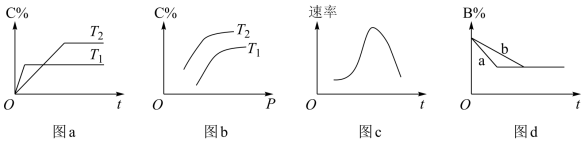
| A.由图a可知,T1>T2,该反应的逆反应为吸热反应 |
| B.由图b可知,该反应m+n<p |
| C.图c是绝热条件下速率和时间的图象,由此说明该反应吸热 |
| D.图d中,曲线a一定增加了催化剂 |
您最近一年使用:0次
2020-11-20更新
|
928次组卷
|
5卷引用:四川省成都市简阳市阳安中学2020-2021学年高二上学期期中考试化学试题
解题方法
4 . 甲醇是重要的化工原料。利用合成气(主要成分为(CO,CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
i:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
ii:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
iii:CH3OH(g) CO(g)+2H2(g) ΔH3
CO(g)+2H2(g) ΔH3
回答下列问题:
(1)已知反应2中相关化学键键能数据如下:
由此计算ΔH2=___ kJ·mol-1。已知ΔH1=-63kJ·mol-1,则ΔH3=___ kJ·mol-1。
(2)对于反应1,不同温度对CO2的平衡转化率及催化剂的效率影响如图所示,请回答下列问题:
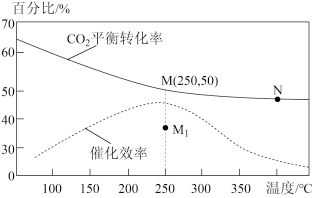
①下列说法不正确的是( )
A.M点时平衡常数比N点时平衡常数大
B.温度低于250℃时,随温度升高甲醇的平衡产率降低
C.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
②若在刚性容器中充入3molH2和1molCO2发生反应1,起始压强为4MPa,则图中M点CH3OH的体积分数为___ ,250℃时反应的平衡常数Kp=___ (MPa)-2(保留三位有效数字);
③若要进一步提高甲醇产率,可采取的措施有___ (写两条即可)
(3)相同条件下,一定比例CO/CO2/H2混合气体甲醇生成速率大于CO2/H2混合气体甲醇生成速率,结合反应1、2分析原因:___ 。
(4)以二氧化钛表面覆盖Cu2A12O4为催化剂,可以将CO2和CH4直接转化成乙酸,CO2(g)+CH4(g) CH3COOH(g),在不同温度下催化剂的催化效率与乙酸的生成速率如图所示:
CH3COOH(g),在不同温度下催化剂的催化效率与乙酸的生成速率如图所示:
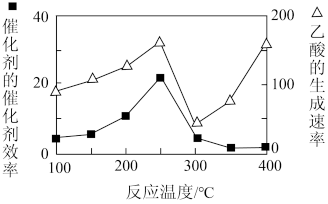
250~300℃时,乙酸的生成速率降低的主要原因是___ 。
300~400℃时,乙酸的生成速率升高的主要原因是___ 。
i:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1ii:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2iii:CH3OH(g)
 CO(g)+2H2(g) ΔH3
CO(g)+2H2(g) ΔH3回答下列问题:
(1)已知反应2中相关化学键键能数据如下:
| 化学键 | H—H | C=O | C≡O | H—O |
| E/KJ·mol-1 | 436 | 803 | 1076 | 465 |
由此计算ΔH2=
(2)对于反应1,不同温度对CO2的平衡转化率及催化剂的效率影响如图所示,请回答下列问题:

①下列说法不正确的是
A.M点时平衡常数比N点时平衡常数大
B.温度低于250℃时,随温度升高甲醇的平衡产率降低
C.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于M1
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
②若在刚性容器中充入3molH2和1molCO2发生反应1,起始压强为4MPa,则图中M点CH3OH的体积分数为
③若要进一步提高甲醇产率,可采取的措施有
(3)相同条件下,一定比例CO/CO2/H2混合气体甲醇生成速率大于CO2/H2混合气体甲醇生成速率,结合反应1、2分析原因:
(4)以二氧化钛表面覆盖Cu2A12O4为催化剂,可以将CO2和CH4直接转化成乙酸,CO2(g)+CH4(g)
 CH3COOH(g),在不同温度下催化剂的催化效率与乙酸的生成速率如图所示:
CH3COOH(g),在不同温度下催化剂的催化效率与乙酸的生成速率如图所示:
250~300℃时,乙酸的生成速率降低的主要原因是
300~400℃时,乙酸的生成速率升高的主要原因是
您最近一年使用:0次
名校
5 . 在恒容密闭容器中存在如下反应。2A(g)+B(g) 3C(g)+D(s) H<0,在其他条件不变时,改变某一条件对上述平衡的影响,下列分析正确的是
3C(g)+D(s) H<0,在其他条件不变时,改变某一条件对上述平衡的影响,下列分析正确的是
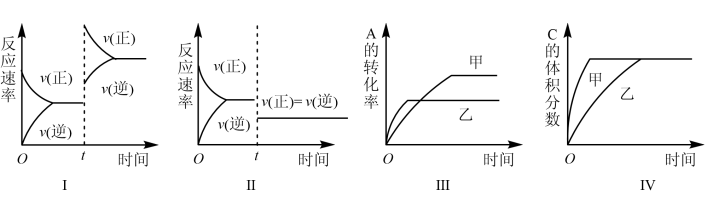
 3C(g)+D(s) H<0,在其他条件不变时,改变某一条件对上述平衡的影响,下列分析正确的是
3C(g)+D(s) H<0,在其他条件不变时,改变某一条件对上述平衡的影响,下列分析正确的是
| A.图Ⅰ表示增加生成物浓度对该平衡的影响 |
| B.图Ⅱ表示增大压强对该平衡的影响 |
| C.图Ⅲ表示温度对该平衡的影响,温度:乙>甲 |
| D.图Ⅳ表示催化剂对该平衡的影响,催化效率:乙>甲 |
您最近一年使用:0次
2019-12-15更新
|
949次组卷
|
5卷引用:广东省深圳市人大附中2019-2020学年高二上学期期中考试化学试题
名校
解题方法
6 . 可逆反应aA(g)+bB(g)⇌cC(g)+dD(g)△H,根据图像判断,下列叙述正确的是( )
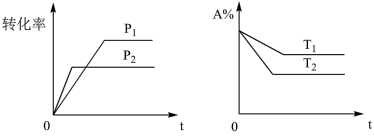

| A.p1<p2,a+b<c+d,T1<T2,△H>0 |
| B.p1<p2,a+b>c+d,T1>T2,△H>0 |
| C.p1<p2,a+b<c+d,T1>T2,△H>0 |
| D.以上答案均不对 |
您最近一年使用:0次
2019-12-06更新
|
204次组卷
|
2卷引用:广东省广州市2019-2020学年高二上学期期中模拟测试化学试题(一)
解题方法
7 . 丙烯(C3H6)是重要的有机化工原料。丙烷脱氢制丙烯发生的主要反应及能量变化如下图。
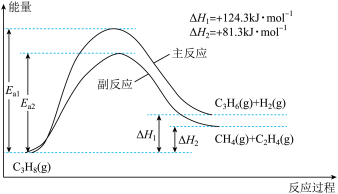
(1)丙烷脱氢制丙烯为强吸热过程。
①为提供反应所需热量,恒压时若向原料气中掺入水蒸气,则K(主反应)____ (填“增大”、“减小”或“不变”,下同),转化率α(C3H8)_____ 。
②温度升高,副反应更容易发生的主要原因是__________________________________ 。
(2)下图为丙烷直接脱氢法中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中的压强分
别为104 Pa和105 Pa)。
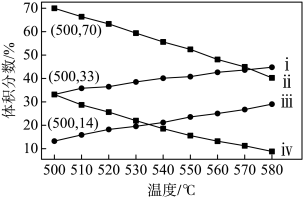
①104 Pa时,图中表示丙烯的曲线是____ (填“ⅰ”、“ⅱ”、“ⅲ”或“ⅳ”)。
②104 Pa、500 ℃时,主反应用平衡分压代替平衡浓度表示的化学平衡常数Kp=_____ (已知:气体分压=气体总压×体积分数)。
(3)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。
该工艺可采用铬的氧化物为催化剂,其反应机理如图。
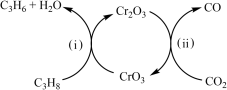
已知:CO和H2的燃烧热分别为△H =-283.0 kJ·mol-1、△H =-285.8 kJ·mol-1。
①图中催化剂为______ 。
②298 K 时,该工艺总反应的热化学方程式为_____________________________________ 。
③该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是__________ 。

(1)丙烷脱氢制丙烯为强吸热过程。
①为提供反应所需热量,恒压时若向原料气中掺入水蒸气,则K(主反应)
②温度升高,副反应更容易发生的主要原因是
(2)下图为丙烷直接脱氢法中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中的压强分
别为104 Pa和105 Pa)。

①104 Pa时,图中表示丙烯的曲线是
②104 Pa、500 ℃时,主反应用平衡分压代替平衡浓度表示的化学平衡常数Kp=
(3)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。
该工艺可采用铬的氧化物为催化剂,其反应机理如图。

已知:CO和H2的燃烧热分别为△H =-283.0 kJ·mol-1、△H =-285.8 kJ·mol-1。
①图中催化剂为
②298 K 时,该工艺总反应的热化学方程式为
③该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是
您最近一年使用:0次
9-10高二下·广东东莞·期末
名校
8 . 在密闭容器中,对于可逆反应:A(?)+3B(?) 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是

 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
| A.若正反应方向△H<0,则T1>T2 | B.压强增大时,混合气体的平均相对分子质量减小 |
| C.A一定为气体 | D.B一定为气体 |
您最近一年使用:0次
2018-01-16更新
|
628次组卷
|
19卷引用:2010年广东省东莞市高二第二学期期末考试化学A卷
(已下线)2010年广东省东莞市高二第二学期期末考试化学A卷(已下线)2011-2012学年广东省中山市高二下学期期末考试化学试卷(已下线)2013-2014广东汕头市金山中学第一学期期末高二化学试卷2015-2016学年广东省湛江市高二上学期期末质检化学试卷广东省佛山市第一中学2017-2018学年高二上学期期中考试化学试题广东省普宁市华美实验学校2017-2018学年高二上学期第二次月考化学试题广东省台山市华侨中学2020-2021学年高二上学期第一次月考化学试题(已下线)2011届福建省三明一中高三上学期第三次月考化学试卷(已下线)2013-2014四川省宜昌市部分市级示范高中春季期中考试高二化学试卷(已下线)2015届山西大学附中高三上学期期中化学试卷2015-2016学年湖北省武汉三十九中高二上学期期末化学试卷河南省濮阳市2016-2017学年高二下学期升级(期末)考试(A卷)化学试题河北省张家口市第一中学2016-2017学年高一(衔接班)下学期期末考试(理)化学试题陕西省黄陵中学高新部2016-2017学年高一下学期期末考试化学试题吉林省吉化第一高级中学校2017-2018学年高二上学期期末考试化学试题北京市通州区2019-2020学年高二下学期期末考试化学试题(已下线)第六单元 化学反应速率和化学平衡测试题-2021年高考化学一轮复习名师精讲练【学科网名师堂】江西省吉安三中2021-2022学年高二上学期10月第一次段考化学试题天津市七校联考2022届高三第二次质量调查化学试题
名校
9 . 向密闭容器中,按n(CO):n(H2)=1:2充入反应物,发生反应:CO(g)+2H2(g) CH3OH(g) △H<0。L(L1、L2)、X可分别代表压强或温度,下图表示L一定时,平衡混合物中CH3OH的体积分数随X的变化关系。
CH3OH(g) △H<0。L(L1、L2)、X可分别代表压强或温度,下图表示L一定时,平衡混合物中CH3OH的体积分数随X的变化关系。

下列说法中,正确的是( )
 CH3OH(g) △H<0。L(L1、L2)、X可分别代表压强或温度,下图表示L一定时,平衡混合物中CH3OH的体积分数随X的变化关系。
CH3OH(g) △H<0。L(L1、L2)、X可分别代表压强或温度,下图表示L一定时,平衡混合物中CH3OH的体积分数随X的变化关系。
下列说法中,正确的是( )
| A.X代表压强 | B.L1<L2 |
| C.平衡常数:K(A)=K(B) | D.在C点时,CO转化率为75% |
您最近一年使用:0次
2016-12-09更新
|
430次组卷
|
7卷引用:安徽省淮北市濉溪中学2017-2018学年高二上学期开学考试化学试题
名校
10 . 在某容积一定的密闭容器中,有下列可逆反应xA(g)+B(g)⇌2C(g),反应曲线(T表示温度,P表示压强,C% 表示C的体积分数)如图所示,试判断对图的说法中一定正确的是( )
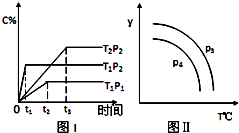

| A.该反应是吸热反应 |
| B.x=2 |
| C.P3<P4,y轴可表示混合气体的相对分子质量 |
| D.P3>P4,y轴可表示C物质在平衡体积中的百分含量 |
您最近一年使用:0次
2016-12-09更新
|
429次组卷
|
5卷引用:广东省中山纪念中学2020-2021学年高二上学期第一次段考化学试题



