1 . 在一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g) 2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
(1)判断该反应达到平衡状态的标志是___________ (填字母);
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为___________ ,用SO2的浓度变化表示的平均反应速率v(SO2)=___________ 。
(3)若反应温度降低,SO2的转化率___________ (填“增大”“减小”或“不变”);如图表示平衡时SO2的体积分数随压强和温度变化的曲线。则温度关系:T1___________ T2(填“>”“<”或“=”)。
 2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:(1)判断该反应达到平衡状态的标志是
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为
(3)若反应温度降低,SO2的转化率

您最近半年使用:0次
2 . 已知反应: 。在一定压强下,按
。在一定压强下,按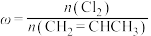 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数( )与温度(T)、
)与温度(T)、 的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
 。在一定压强下,按
。在一定压强下,按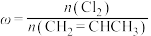 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数( )与温度(T)、
)与温度(T)、 的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
A.此反应 H>0 H>0 | B.图甲中 |
| C.图乙中,曲线A表示正反应的平衡常数 | D.温度T1、 , , 的转化率约为33.3% 的转化率约为33.3% |
您最近半年使用:0次
解题方法
3 . 聚丙烯是生产N95口罩和医用无纺布口罩防护服材料,而丙烯是制造聚丙烯的单体。工业上,生成丙烯的方法有多种。
Ⅰ.以异丙醇为原料制备丙烯。已知:
①
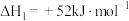 ;
;
②
 ;
;
③
 。
。
(1) 为
为___________  。
。
(2)反应③在___________ (填“较高”“较低”或“任意”)温度下能自发进行。
Ⅱ.近日,中国石油大学(华东)代鹏程副教授课题组开发富含硼氧活性位点的热稳定层柱状框架类材料助力丙烷氧化脱氢。有关反应如下:
反应1: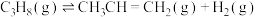

反应2: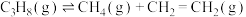
 。
。
(3)向密闭反应器中充入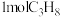 ,发生上述反应1,测得平衡时的丙烯的体积分数与温度、压强的关系如图1所示。
,发生上述反应1,测得平衡时的丙烯的体积分数与温度、压强的关系如图1所示。
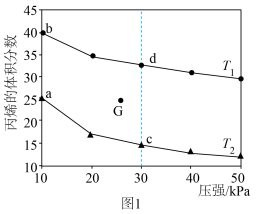
①其他条件相同,增大压强,丙烯体积分数减小的原因是___________ 。
②已知G点为某条件下的平衡状态,若将G点对应反应容器降温同时缩小容器体积使体系压强增大,重新达到平衡状态可能是图中a、b、c、d中的___________ 点。
③下列物理量中,图中c点大于d点的是___________ (填字母)。
A.正反应速率 B.对应温度的平衡常数 C.逆反应速率 D.平均摩尔质量
(4)一定温度下,若向密闭反应器中充入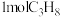 ,发生上述两个反应,达到平衡时,丙烯的体积分数为
,发生上述两个反应,达到平衡时,丙烯的体积分数为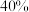 ,丙烯、乙烯体积之比为
,丙烯、乙烯体积之比为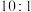 ,丙烷的平衡转化率为
,丙烷的平衡转化率为___________ (用百分数表示,结果保留3位有效数字)。
(5)一定温度下,总压保持为 时,向反应器中充入
时,向反应器中充入 和
和 ,发生上述两个反应。测得丙烷平衡转化率与投料比
,发生上述两个反应。测得丙烷平衡转化率与投料比 的关系如图2所示。
的关系如图2所示。
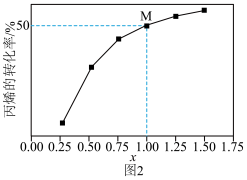
①向反应器充入 的目的是
的目的是___________ 。
②该温度下, 点丙烯的选择性为
点丙烯的选择性为 ,此时反应1的平衡常数
,此时反应1的平衡常数 为
为___________ 。
提示:(i)用分压计算的平衡常数为 ,分压
,分压 总压
总压 物质的量分数;(ii)丙烯的选择性
物质的量分数;(ii)丙烯的选择性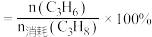 。
。
Ⅰ.以异丙醇为原料制备丙烯。已知:
①

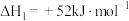 ;
;②

 ;
;③

 。
。(1)
 为
为 。
。(2)反应③在
Ⅱ.近日,中国石油大学(华东)代鹏程副教授课题组开发富含硼氧活性位点的热稳定层柱状框架类材料助力丙烷氧化脱氢。有关反应如下:
反应1:
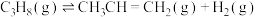

反应2:
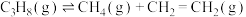
 。
。(3)向密闭反应器中充入
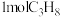 ,发生上述反应1,测得平衡时的丙烯的体积分数与温度、压强的关系如图1所示。
,发生上述反应1,测得平衡时的丙烯的体积分数与温度、压强的关系如图1所示。
①其他条件相同,增大压强,丙烯体积分数减小的原因是
②已知G点为某条件下的平衡状态,若将G点对应反应容器降温同时缩小容器体积使体系压强增大,重新达到平衡状态可能是图中a、b、c、d中的
③下列物理量中,图中c点大于d点的是
A.正反应速率 B.对应温度的平衡常数 C.逆反应速率 D.平均摩尔质量
(4)一定温度下,若向密闭反应器中充入
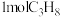 ,发生上述两个反应,达到平衡时,丙烯的体积分数为
,发生上述两个反应,达到平衡时,丙烯的体积分数为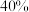 ,丙烯、乙烯体积之比为
,丙烯、乙烯体积之比为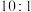 ,丙烷的平衡转化率为
,丙烷的平衡转化率为(5)一定温度下,总压保持为
 时,向反应器中充入
时,向反应器中充入 和
和 ,发生上述两个反应。测得丙烷平衡转化率与投料比
,发生上述两个反应。测得丙烷平衡转化率与投料比 的关系如图2所示。
的关系如图2所示。
①向反应器充入
 的目的是
的目的是②该温度下,
 点丙烯的选择性为
点丙烯的选择性为 ,此时反应1的平衡常数
,此时反应1的平衡常数 为
为提示:(i)用分压计算的平衡常数为
 ,分压
,分压 总压
总压 物质的量分数;(ii)丙烯的选择性
物质的量分数;(ii)丙烯的选择性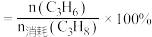 。
。
您最近半年使用:0次
名校
4 . T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图-1所示;若保持其他条件不变,温度分别为T1和T2,Y的体积百分含量与时间的关系如图-2所示。下列分析正确的是
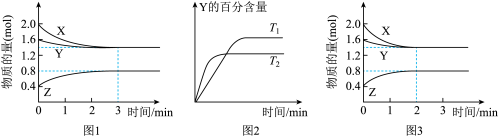

A.容器中发生的反应可表示为:2X(g)+Y(g) 2Z(g) 2Z(g) |
B.0~3 min内, (X)=0.2 mol•L-1•min-1 (X)=0.2 mol•L-1•min-1 |
C.其他条件不变升高温度, 正、 正、 逆都增大,且重新平衡前 逆都增大,且重新平衡前 正> 正> 逆 逆 |
| D.若改变条件,使反应进程如图-3所示,则改变的条件可能是增大压强 |
您最近半年使用:0次
名校
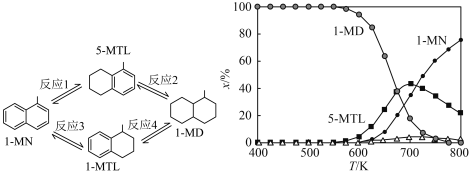
5 . 下图(左)表示1-甲基萘(1-MN)加氢饱和反应网络,四个加氢反应均为放热反应(用反应1、2、3、4表示)。下图(右)表示反应温度(T)对平衡时反应体系中有机化合物物质的量分数(x/%)的影响(6MPa,1-MN和 体积比为1∶5条件下)。下列说法
体积比为1∶5条件下)。下列说法不正确 的是
 体积比为1∶5条件下)。下列说法
体积比为1∶5条件下)。下列说法
| A.800K反应2和反应4生成1-MD的程度很小 |
| B.600K到800K,反应1的平衡常数逐渐减小 |
| C.700K反应1的平衡常数小于反应3的平衡常数 |
| D.600K到650K,反应2中5-MTL增加的量大于反应1中5-MTL减少的量 |
您最近半年使用:0次
6 . 可逆反应A(?)+aB(g) C(g)+2D(g)(a为正整数) ΔH。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(p)的关系如图所示。下列说法正确的是
C(g)+2D(g)(a为正整数) ΔH。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(p)的关系如图所示。下列说法正确的是
 C(g)+2D(g)(a为正整数) ΔH。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(p)的关系如图所示。下列说法正确的是
C(g)+2D(g)(a为正整数) ΔH。反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(p)的关系如图所示。下列说法正确的是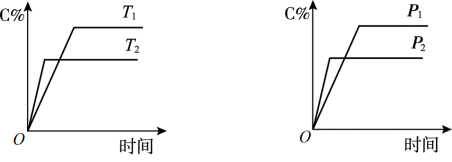
| A.T1>T2、p1>p2 | B.a不可能大于3 |
| C.该反应的ΔH>0 | D.反应过程中,始终有v(C)=2v(D) |
您最近半年使用:0次
名校
解题方法
7 .  温度下,向
温度下,向 恒容密闭容器中加入
恒容密闭容器中加入 固体,发生反应
固体,发生反应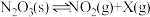 (未配平),反应过程如图,下列说法正确的是
(未配平),反应过程如图,下列说法正确的是
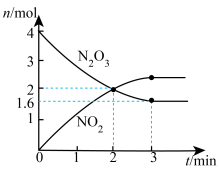
A.X可能为 |
B.第 时逆反应速率大于第 时逆反应速率大于第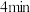 时逆反应速率 时逆反应速率 |
C. 用 用 表示的反应速率为 表示的反应速率为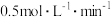 |
D.第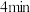 时,保持T和V不变,向容器中再加入 时,保持T和V不变,向容器中再加入 ,正反应速率加快 ,正反应速率加快 |
您最近半年使用:0次
8 . 可逆反应mA(g)+nB(g)⇌pC(g)+qD(g)的相关物质体积分数的变化图像如下,请回答下列问题:

(1)温度T1_______ T2(填“>”、“<”或“=”,下同)。
(2)压强p1_______ p2。
(3)m+n_______ p+q。
(4)正反应为_______ (填“放热”或“吸热”)反应。

(1)温度T1
(2)压强p1
(3)m+n
(4)正反应为
您最近半年使用:0次
解题方法
9 . 实现碳的氧化物循环利用在工业上占有重要的地位。一氧化碳加氢制甲醇的原理为 。回答下列问题;
。回答下列问题;
(1)用甲醇燃料电池作为外接电源按图1所示电解硫酸铜溶液,起始时盛有 的硫酸铜溶液(25℃,
的硫酸铜溶液(25℃, 足量)。
足量)。
①电解的总反应方程式为______ ,此时可观察到的现象是______ 。
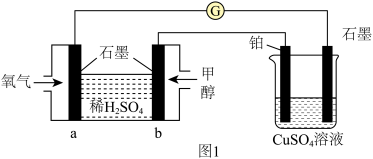
②一段时间后溶液的pH变为1,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入______ (填物质名称),其质量约为______ g。
(2)在不同条件下,向体积可变的密闭容器中充入0.50molCO(g)和1.00molH2(g)的混合气体,实验测得平衡时CH3OH的物质的量随温度、压强的变化如图2所示。
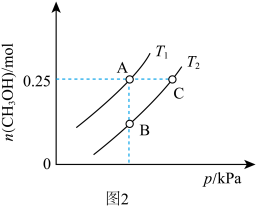
则温度:
______ (填“>”“<”或“=”) 三点对应的平衡常数由大到小关系为
三点对应的平衡常数由大到小关系为______ 。
(3)一定温度下,向恒容密闭容器中充入 和
和 混合气体,测得初始压强为
混合气体,测得初始压强为 。反应至
。反应至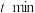 时,恢复到原来温度,测得
时,恢复到原来温度,测得 的转化率为
的转化率为 。已知正反应速率
。已知正反应速率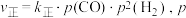 为分压(分压=总压
为分压(分压=总压 物质的量分数)。若该条件下
物质的量分数)。若该条件下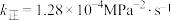 ,则
,则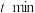 时,
时,
______ 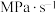 。若升高温,k正
。若升高温,k正______ (填“增大”“减小”或“不变”)。
 。回答下列问题;
。回答下列问题;(1)用甲醇燃料电池作为外接电源按图1所示电解硫酸铜溶液,起始时盛有
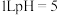 的硫酸铜溶液(25℃,
的硫酸铜溶液(25℃, 足量)。
足量)。①电解的总反应方程式为

②一段时间后溶液的pH变为1,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入
(2)在不同条件下,向体积可变的密闭容器中充入0.50molCO(g)和1.00molH2(g)的混合气体,实验测得平衡时CH3OH的物质的量随温度、压强的变化如图2所示。

则温度:

 三点对应的平衡常数由大到小关系为
三点对应的平衡常数由大到小关系为(3)一定温度下,向恒容密闭容器中充入
 和
和 混合气体,测得初始压强为
混合气体,测得初始压强为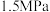 。反应至
。反应至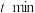 时,恢复到原来温度,测得
时,恢复到原来温度,测得 的转化率为
的转化率为 。已知正反应速率
。已知正反应速率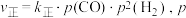 为分压(分压=总压
为分压(分压=总压 物质的量分数)。若该条件下
物质的量分数)。若该条件下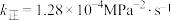 ,则
,则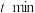 时,
时,
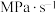 。若升高温,k正
。若升高温,k正
您最近半年使用:0次
名校
解题方法
10 . 对于可逆反应A(g)+2B(g) 2C(g) (正反应吸热),下列图像正确的是
2C(g) (正反应吸热),下列图像正确的是
 2C(g) (正反应吸热),下列图像正确的是
2C(g) (正反应吸热),下列图像正确的是A. | B. | C.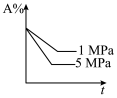 | D.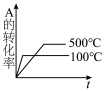 |
您最近半年使用:0次
2024-03-09更新
|
187次组卷
|
2卷引用:云南省昆明市云南师范大学实验中学2023-2024学年高二下学期3月月考化学试题



