名校
解题方法
1 . 汽车尾气中含有CO、NO2等有毒气体,对汽车家装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
已知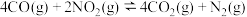
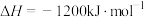
(1)该反应在___________ (填“高温、低温或任何温度”)下能自发进行。
(2)对于该反应,改变某一反应条件(温度 ),下列图象正确的是___________(填标号)。
),下列图象正确的是___________(填标号)。
(3)某实验小组模拟上述净化过程,一定温度下,在 的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲:
的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲: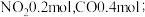 乙:
乙: ,经过一段时间后达到平衡状态。
,经过一段时间后达到平衡状态。
① 的平衡体积分数:甲
的平衡体积分数:甲___________ 乙(填“>、=、<或不确定”,下同)。
② 的平衡浓度:甲
的平衡浓度:甲___________ 乙。
③甲中 的转化率为
的转化率为 ,该反应的平衡常数为
,该反应的平衡常数为___________ 。
已知
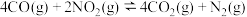
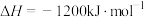
(1)该反应在
(2)对于该反应,改变某一反应条件(温度
 ),下列图象正确的是___________(填标号)。
),下列图象正确的是___________(填标号)。A.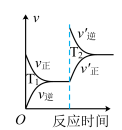 | B.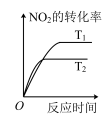 | C.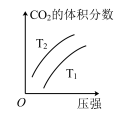 | D.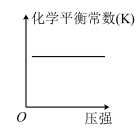 |
(3)某实验小组模拟上述净化过程,一定温度下,在
 的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲:
的恒容密闭容器中,起始时按照甲、乙两种方式进行投料。甲: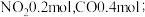 乙:
乙: ,经过一段时间后达到平衡状态。
,经过一段时间后达到平衡状态。①
 的平衡体积分数:甲
的平衡体积分数:甲②
 的平衡浓度:甲
的平衡浓度:甲③甲中
 的转化率为
的转化率为 ,该反应的平衡常数为
,该反应的平衡常数为
您最近一年使用:0次
名校
解题方法
2 . 灰锡结构松散,不能用于制造器皿。现把白锡制造的器皿在0℃、100kPa环境下存放,它会不会变成灰锡而不能继续使用呢?(已知在0℃、100kPa条件下白锡转化为灰锡的反应的焓变和熵变分别为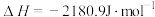 ,
, ,当
,当 时能自发反应)
时能自发反应)
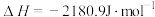 ,
, ,当
,当 时能自发反应)
时能自发反应)| A.会变 | B.不会变 | C.不能确定 | D.升高温度才会变 |
您最近一年使用:0次
名校
3 . 可以利用 反应制备H2和CO,下列说法正确的是
反应制备H2和CO,下列说法正确的是
 反应制备H2和CO,下列说法正确的是
反应制备H2和CO,下列说法正确的是| A.该反应△S>0 |
B.反应的平衡常数表达式为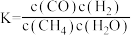 |
| C.上述反应中消耗1molCH4,转移电子的数目约为2×6.02×1023 |
| D.其他条件相同时,增大压强,可以提高CH4的平衡转化率 |
您最近一年使用:0次
解题方法
4 . 下列说法正确的是
A.反应N2+3H2 2NH3的△H<0,△S>0 2NH3的△H<0,△S>0 |
| B.反应2CO(g)+2NO(g)=N2(g)+2CO2(g) △H>0在常温下能自发进行 |
| C.反应2Mg(s)+CO2(g)=C(s)+2MgO(s)的△H<0,则该反应能在高温自发进行 |
| D.反应C(s)+CO2(g)=2CO(g)常温下不能自发进行,则该反应的△H>0 |
您最近一年使用:0次
解题方法
5 .  的资源化利用对碳循环经济技术的发展具有重要意义。
的资源化利用对碳循环经济技术的发展具有重要意义。
Ⅰ.利用 和
和 制备合成气(CO、
制备合成气(CO、 ),反应分两步进行:
),反应分两步进行:
反应①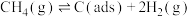

反应②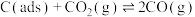

有关物质的相对能量与反应历程的变化如图所示[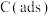 为吸附性活性炭]:
为吸附性活性炭]:
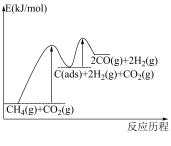
(1)总反应 能自发进行的条件为
能自发进行的条件为_______ 。
(2)总反应速率由反应_______ (填“①”或“②”)决定,增加 的浓度,
的浓度,_______ (填“能”或“不能”)显著提升总反应的速率。
Ⅱ.工业上可利用 生产燃料甲醇。该过程发生下列反应:
生产燃料甲醇。该过程发生下列反应:
反应③

反应④
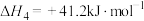
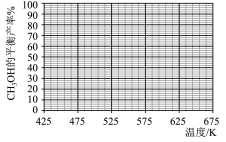
在5MPa的恒压反应器中,按照 投料,测得体系中平衡时
投料,测得体系中平衡时 和CO的选择性及
和CO的选择性及 的平衡转化率随温度的变化如图所示(选择性:转化的
的平衡转化率随温度的变化如图所示(选择性:转化的 中生成
中生成 或CO的百分比)。
或CO的百分比)。

(3)在425℃~675℃范围内(其他条件不变), 的平衡转化率随温度升高发生变化,写出该变化规律并分析原因:
的平衡转化率随温度升高发生变化,写出该变化规律并分析原因:_______ ,_______ 。
(4)下列说法正确的是_______(填字母)。
(5)反应④在545K时的平衡常数
_______ 。
(6)结合上图,在下图中画出 的平衡产率随温度的变化曲线
的平衡产率随温度的变化曲线_______ (标出B点坐标)。
 的资源化利用对碳循环经济技术的发展具有重要意义。
的资源化利用对碳循环经济技术的发展具有重要意义。Ⅰ.利用
 和
和 制备合成气(CO、
制备合成气(CO、 ),反应分两步进行:
),反应分两步进行:反应①
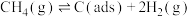

反应②
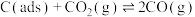

有关物质的相对能量与反应历程的变化如图所示[
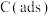 为吸附性活性炭]:
为吸附性活性炭]:
(1)总反应
 能自发进行的条件为
能自发进行的条件为(2)总反应速率由反应
 的浓度,
的浓度,Ⅱ.工业上可利用
 生产燃料甲醇。该过程发生下列反应:
生产燃料甲醇。该过程发生下列反应:反应③


反应④

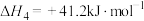
在5MPa的恒压反应器中,按照
 投料,测得体系中平衡时
投料,测得体系中平衡时 和CO的选择性及
和CO的选择性及 的平衡转化率随温度的变化如图所示(选择性:转化的
的平衡转化率随温度的变化如图所示(选择性:转化的 中生成
中生成 或CO的百分比)。
或CO的百分比)。
(3)在425℃~675℃范围内(其他条件不变),
 的平衡转化率随温度升高发生变化,写出该变化规律并分析原因:
的平衡转化率随温度升高发生变化,写出该变化规律并分析原因:(4)下列说法正确的是_______(填字母)。
| A.曲线Ⅱ代表CO的选择性随温度的变化 |
B.温度越低,越有利于工业生产 |
C.上述反应条件下, 的平衡转化率等于 的平衡转化率等于 的平衡转化率 的平衡转化率 |
D.原料气中掺入适量CO能提高 的产率 的产率 |
(5)反应④在545K时的平衡常数

(6)结合上图,在下图中画出
 的平衡产率随温度的变化曲线
的平衡产率随温度的变化曲线
您最近一年使用:0次
解题方法
6 . 一个化学反应在给定条件(通常指温度、压强)下能否自发进行以及在什么条件下有可能按预期的方向发生,需寻求一种客观的判据,用它来判断一个化学反应能否正向自发进行。研究表明,可逆反应在适当条件下进行一段时间后一定会达到化学平衡状态。在研究了大量实验的基础上,人们发现可以用化学平衡常数来定量描述化学反应的限度。
(1)下列关于自发反应的叙述,正确的是___________。
(2)下列说法中正确的是___________。
(3)某温度下,可逆反应 的平衡常数为K。下列对K的说法正确的是___________。
的平衡常数为K。下列对K的说法正确的是___________。
(4)在一定温度下,下列反应的化学平衡常数数值如下:
①
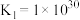
②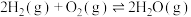
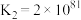
③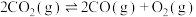
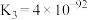
下列说法正确的是___________。
(5)在某密闭容器中把CO和 的混合物加热到800℃,存在平衡:
的混合物加热到800℃,存在平衡: ,且平衡常数
,且平衡常数 。若在2L的密闭容器中充入1molCO和1mol
。若在2L的密闭容器中充入1molCO和1mol 的混合物并加热到800℃,则平衡时CO的转化率为___________。
的混合物并加热到800℃,则平衡时CO的转化率为___________。
(6)地下水中的氮污染主要是由 引起的,人们对
引起的,人们对 的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,
的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下, 将硝酸盐还原成氮气:
将硝酸盐还原成氮气: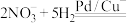

①氮肥 溶于水的过程中熵值
溶于水的过程中熵值___________ (填“增大”或“减小”),Pd/Cu双金属催化剂___________ (填“是”或“不是”)决定反应自发发生的决定因素。
②已知: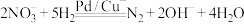 的
的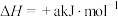 ,
, (a、b均为正值),该反应
(a、b均为正值),该反应___________ (填“能”“不能”或“无法判断是否能”)自发进行。
(7)在一定体积的密闭容器中进行如下化学反应:
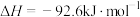 ,其化学平衡常数(K)和温度(T)的关系如下表所示:
,其化学平衡常数(K)和温度(T)的关系如下表所示:
①试判断
___________  (填写“>”、“=”或“<”)
(填写“>”、“=”或“<”)
②T℃( )的某时刻下,
)的某时刻下, ,
,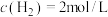 ,
, ,此时该反应是否处于平衡状态
,此时该反应是否处于平衡状态___________ (选填“是”或“否”),此时反应速率是
___________  (选择“>”、“=”或“<”),其原因是
(选择“>”、“=”或“<”),其原因是___________ 。
(1)下列关于自发反应的叙述,正确的是___________。
| A.自发反应的逆过程在相同条件下也必定是自发的 |
| B.铁在潮湿的空气中生锈属于非自发反应 |
| C.自发过程可以是物理过程,不一定是自发反应,而自发反应一定是自发过程 |
| D.自发反应与外界条件无关 |
A.若 , , ,化学反应在任何温度下都能自发进行 ,化学反应在任何温度下都能自发进行 |
B.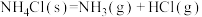 在室温下不能自发进行,则该反应的 在室温下不能自发进行,则该反应的 |
C. 在低温下能自发进行,则该反应的 在低温下能自发进行,则该反应的 |
| D.加入合适的催化剂能降低反应的活化能,从而改变反应的焓变 |
 的平衡常数为K。下列对K的说法正确的是___________。
的平衡常数为K。下列对K的说法正确的是___________。| A.温度越高,K一定越大 |
B.如果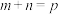 ,则 ,则 |
| C.若缩小反应器的容积,增大压强,则K增大 |
| D.K值越大,表明该反应越有利于C的生成,反应物的转化率越大 |
①

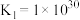
②
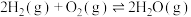
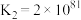
③
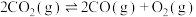
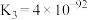
下列说法正确的是___________。
A.该温度下,反应①的平衡常数表达式为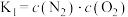 |
B.该温度下,反应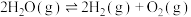 的平衡常数的数值约为 的平衡常数的数值约为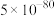 |
C.该温度下,反应①、反应②的逆反应、反应③产生 的倾向由大到小的顺序为 的倾向由大到小的顺序为 |
| D.以上说法都不正确 |
 的混合物加热到800℃,存在平衡:
的混合物加热到800℃,存在平衡: ,且平衡常数
,且平衡常数 。若在2L的密闭容器中充入1molCO和1mol
。若在2L的密闭容器中充入1molCO和1mol 的混合物并加热到800℃,则平衡时CO的转化率为___________。
的混合物并加热到800℃,则平衡时CO的转化率为___________。| A.40% | B.50% | C.60% | D.83.3% |
 引起的,人们对
引起的,人们对 的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,
的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下, 将硝酸盐还原成氮气:
将硝酸盐还原成氮气: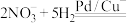

①氮肥
 溶于水的过程中熵值
溶于水的过程中熵值②已知:
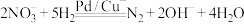 的
的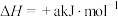 ,
, (a、b均为正值),该反应
(a、b均为正值),该反应(7)在一定体积的密闭容器中进行如下化学反应:

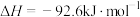 ,其化学平衡常数(K)和温度(T)的关系如下表所示:
,其化学平衡常数(K)和温度(T)的关系如下表所示:| T℃ | 25 | 125 | 225 |
| K | 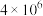 |  |  |

 (填写“>”、“=”或“<”)
(填写“>”、“=”或“<”)②T℃(
 )的某时刻下,
)的某时刻下, ,
,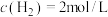 ,
, ,此时该反应是否处于平衡状态
,此时该反应是否处于平衡状态
 (选择“>”、“=”或“<”),其原因是
(选择“>”、“=”或“<”),其原因是
您最近一年使用:0次
名校
7 . 将产能过剩的乙酸在特定催化剂作用下和氢气反应生成乙醇,其反应原理如下:CH3COOH(g)+2H2(g)⇌CH3CH2OH(g)+H2O(g) △H1
已知:298k和100kPa时物质的燃烧热:
1.根据以上燃烧热,计算该反应在298k和100kPa的△H1时,需补充_______ 。
A.水的汽化热 B.乙酸、乙醇和水的汽化热 C.反应物的汽化热
2.一定温度下,将不同量的原料通入恒压密闭容器中,测出平衡时的热量变化
则,该温度下,△H1=_______kJ·mol–1。
3.该反应在_______能向正反应方向自发进行。
4.250℃,恒压绝热密闭容器中充入一定量CH3COOH和H2,下列条件能判断反应达到平衡状态的是_______。
上述反应发生时还伴随有副反应发生,生成少量乙酸乙酯:CH3COOH(g)+CH3CH2OH(g)⇌CH3COOCH2CH3(g)+H2O(g) △H2<0
已知:①该副反应的热效应很小;
②S表示产物选择性,乙醇、乙酸乙酯选择性表示为:
S(乙醇)= ;S(乙酸乙酯)=
;S(乙酸乙酯)=
当nH2(g):n(CH3COOH)=10:1时,下图表示2Mpa,平衡时S(乙醇)、S(乙酸乙酯)随温度的变化以及250℃,平衡时S(乙醇)、S(乙酸乙酯)随压强的变化:_______ 。
A.a B.c C.d
6.曲线b是S(乙醇)随温度变化的曲线,解释b的变化趋势。_______ 。
7.150℃,在催化剂作用下,H2和CH3COOH反应一段时间后,S(乙醇)位于m点,不改变反应时间和温度,一定能提高S(乙醇)的措施是_______ 。(任写一条)
8.一定温度和压强下,向初始体积为1L的密闭容器中通入2molH2(g)和1molCH3COOH(g),同时发生主反应和副反应,测定平衡时n[H2O(g)]=0.8mol,体积减小20%,则平衡时n(CH3COOH)=_______ mol、c(H2)=_______ mol·L–1。主反应的平衡常数K=_______ 。
已知:298k和100kPa时物质的燃烧热:
| 物质 | CH3COOH(l) | H2(g) | CH3CH2OH(l) |
| 燃烧热/kJ·mol–1 | –871 | –286 | –1367 |
A.水的汽化热 B.乙酸、乙醇和水的汽化热 C.反应物的汽化热
2.一定温度下,将不同量的原料通入恒压密闭容器中,测出平衡时的热量变化
| 实验编号 | 反应物投入量 | 平衡时, 热量变化 | |||
| CH3CH2OH(g) | H2(g) | CH3CH2OH(g) | H2O(g) | ||
| I | 1mol | 2mol | 0 | 0 | 放热xkJ |
| II | 0 | 0 | 1mol | 1mol | 吸收ykJ |
| A.x+y | B.x-y | C.-(x+y) | D.y-x |
| A.任何温度下 | B.较低温度下 | C.较高温度下 | D.无法确定 |
| A.混合气体的密度保持不变 | B.v(H2)正:v(H2O)正=2:1 |
| C.n(CH3COOH):n(H2)=1:2 | D.反应体系的温度保持不变 |
上述反应发生时还伴随有副反应发生,生成少量乙酸乙酯:CH3COOH(g)+CH3CH2OH(g)⇌CH3COOCH2CH3(g)+H2O(g) △H2<0
已知:①该副反应的热效应很小;
②S表示产物选择性,乙醇、乙酸乙酯选择性表示为:
S(乙醇)=
 ;S(乙酸乙酯)=
;S(乙酸乙酯)=
当nH2(g):n(CH3COOH)=10:1时,下图表示2Mpa,平衡时S(乙醇)、S(乙酸乙酯)随温度的变化以及250℃,平衡时S(乙醇)、S(乙酸乙酯)随压强的变化:

A.a B.c C.d
6.曲线b是S(乙醇)随温度变化的曲线,解释b的变化趋势。
7.150℃,在催化剂作用下,H2和CH3COOH反应一段时间后,S(乙醇)位于m点,不改变反应时间和温度,一定能提高S(乙醇)的措施是
8.一定温度和压强下,向初始体积为1L的密闭容器中通入2molH2(g)和1molCH3COOH(g),同时发生主反应和副反应,测定平衡时n[H2O(g)]=0.8mol,体积减小20%,则平衡时n(CH3COOH)=
您最近一年使用:0次
2024-04-01更新
|
187次组卷
|
2卷引用:上海市华东师范大学第二附属中学2023-2024学年高二下学期等级考 阶段检测 化学试题
8 . 已知反应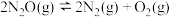 的势能曲线示意图如下(…表示吸附作用,A表示催化剂,
的势能曲线示意图如下(…表示吸附作用,A表示催化剂, 表示过渡态分子):
表示过渡态分子):
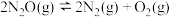 的势能曲线示意图如下(…表示吸附作用,A表示催化剂,
的势能曲线示意图如下(…表示吸附作用,A表示催化剂, 表示过渡态分子):
表示过渡态分子):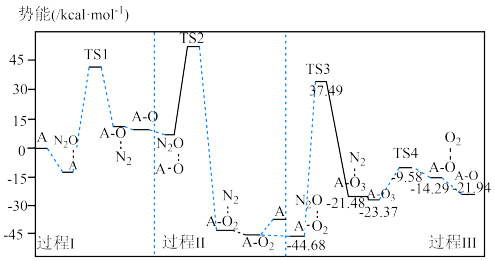
A.过程Ⅰ、Ⅱ、Ⅲ中都有 生成 生成 |
| B.若在任意温度下均能自发进行,则反应为吸热反应 |
C.该反应中只有两种物质能够吸附 分子 分子 |
D.过程Ⅲ中最大势能垒(活化能)为 |
您最近一年使用:0次
2024-04-01更新
|
297次组卷
|
3卷引用:江西省宜春市丰城市第九中学2023-2024学年高二下学期4月期中考试化学试题
江西省宜春市丰城市第九中学2023-2024学年高二下学期4月期中考试化学试题江西省九江市十校2024届高三第二次联考化学试题(已下线)压轴题04?化学反应机理、历程、能垒图分析(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
9 . 已知:空间位阻越大,离去越容易。2-溴-2-甲基丙烷(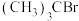 )发生水解反应[
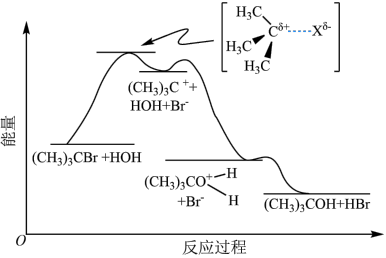
)发生水解反应[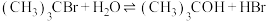 ]的能量变化与反应过程的关系如图所示。下列说法不正确的是
]的能量变化与反应过程的关系如图所示。下列说法不正确的是
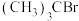 )发生水解反应[
)发生水解反应[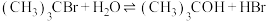 ]的能量变化与反应过程的关系如图所示。下列说法不正确的是
]的能量变化与反应过程的关系如图所示。下列说法不正确的是
| A.该反应在低温下自发进行 |
B.碘原子半径比氧大,因此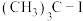 水解生成 水解生成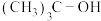 的速率比 的速率比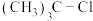 快 快 |
| C.升高温度,可能加快反应速率,同时提高2-溴-2甲基丙烷的平衡转化率 |
D.为了提高2-溴-2-甲基丙烷的水解程度,可以加入适量 固体 固体 |
您最近一年使用:0次
名校
10 . 某小组学生用如图所示简易量热计进行中和反应反应热的测定。近似处理实验所用酸、碱溶液的密度为1.0 g∙cm-3、比热容为4.2J/(g∙℃),忽略量热计的比热容。
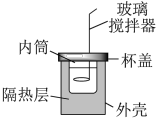
【药品】:50mL 0.50mol/L 盐酸、50mL 0.55mol/L NaOH溶液、50mL 0.55mol/L KOH溶液。
【实验数据】学生甲进行的三次实验数据如下表所示:
(1)从实验装置上看,还缺少的仪器名称是___________ 。
(2)学生甲实测数据处理
①∆t=___________ ℃。
②放出的热量Q甲___________ kJ(保留一位数)。
③Q甲kJ比该反应理论上放热为Q kJ略微偏小,其原因可能是___________ (写一条)。
(3)学生乙选用KOH溶液,其他均与学生甲同,且操作规范,预测实验放出热量的数值Q乙___________ Q甲(填“<”或“=”或“>”)。
(4)写出上面实验理论上生成1mol H2O时,中和反应的反应热的热化学方程式为(用含Q的代数式表示)___________ 。
(5)TiO2转化为TiCl4有直接氯化法和碳氯化法。1000 ℃时反应的热化学方程式及其平衡常数如下:
(i)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) ΔH1=+172 kJ·mol-1,Kp1=1.0×10-2
(ii)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) ΔH2=-51 kJ·mol-1,Kp2=1.2×1012Pa
①反应2C(s)+O2(g)=2CO(g)的ΔH为___________ kJ·mol-1,Kp=___________ Pa。
②碳氯化的反应趋势远大于直接氯化,其原因是___________ 。
③数据显示在200 ℃平衡时TiO2几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是___________ 。
④TiO2碳氯化是一个“气-固-固”反应,有利于TiO2-C“固-固”接触的措施是___________ 。

【药品】:50mL 0.50mol/L 盐酸、50mL 0.55mol/L NaOH溶液、50mL 0.55mol/L KOH溶液。
【实验数据】学生甲进行的三次实验数据如下表所示:
| 实验次数 | 反应前体系的温度/℃ | 反应后体系温度/℃ | 温度差平均值/℃ | ||
| 50mL 0.50mol/L盐酸 | 50mL 0.55mol/L NaOH溶液 | 平均值 | |||
| 1 | 24.9 | 25.1 | 28.4 | ∆t | |
| 2 | 25.1 | 25.0 | 26.3 | ||
| 3 | 25.0 | 25.0 | 28.4 | ||
(1)从实验装置上看,还缺少的仪器名称是
(2)学生甲实测数据处理
①∆t=
②放出的热量Q甲
③Q甲kJ比该反应理论上放热为Q kJ略微偏小,其原因可能是
(3)学生乙选用KOH溶液,其他均与学生甲同,且操作规范,预测实验放出热量的数值Q乙
(4)写出上面实验理论上生成1mol H2O时,中和反应的反应热的热化学方程式为(用含Q的代数式表示)
(5)TiO2转化为TiCl4有直接氯化法和碳氯化法。1000 ℃时反应的热化学方程式及其平衡常数如下:
(i)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) ΔH1=+172 kJ·mol-1,Kp1=1.0×10-2
(ii)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) ΔH2=-51 kJ·mol-1,Kp2=1.2×1012Pa
①反应2C(s)+O2(g)=2CO(g)的ΔH为
②碳氯化的反应趋势远大于直接氯化,其原因是
③数据显示在200 ℃平衡时TiO2几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是
④TiO2碳氯化是一个“气-固-固”反应,有利于TiO2-C“固-固”接触的措施是
您最近一年使用:0次



