解题方法
1 . 已知常温下,碳酸的电离平衡常数为K1、K2。向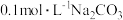 溶液中缓缓通入HCl气体(忽略溶液体积的变化,假设没有二氧化碳放出)。下列各指定溶液中微粒浓度关系正确的是
溶液中缓缓通入HCl气体(忽略溶液体积的变化,假设没有二氧化碳放出)。下列各指定溶液中微粒浓度关系正确的是
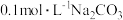 溶液中缓缓通入HCl气体(忽略溶液体积的变化,假设没有二氧化碳放出)。下列各指定溶液中微粒浓度关系正确的是
溶液中缓缓通入HCl气体(忽略溶液体积的变化,假设没有二氧化碳放出)。下列各指定溶液中微粒浓度关系正确的是A.pH=12的 溶液: 溶液: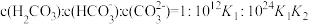 |
B.pH=7的溶液: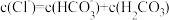 |
C.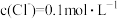 的溶液: 的溶液: |
D.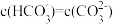 的碱性溶液: 的碱性溶液: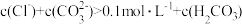 |
您最近一年使用:0次
2 . 已知 溶于水后,会水解生成多种微粒。常温下,
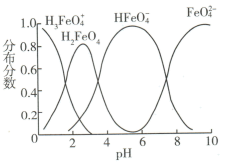
溶于水后,会水解生成多种微粒。常温下, 溶液中各含铁微粒随溶液pH的变化如图所示,纵轴表示其分布分数,则下列说法错误的是
溶液中各含铁微粒随溶液pH的变化如图所示,纵轴表示其分布分数,则下列说法错误的是
 溶于水后,会水解生成多种微粒。常温下,
溶于水后,会水解生成多种微粒。常温下, 溶液中各含铁微粒随溶液pH的变化如图所示,纵轴表示其分布分数,则下列说法错误的是
溶液中各含铁微粒随溶液pH的变化如图所示,纵轴表示其分布分数,则下列说法错误的是
| A.根据图中信息,铁元素有4种存在形态,它们总是大量存在 |
B.向pH=10的溶液中加硫酸至pH=2,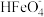 的分布分数先增大后减小 的分布分数先增大后减小 |
C.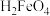 既能和强碱反应又能和强酸反应 既能和强碱反应又能和强酸反应 |
D.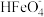 的水解能力强于其电离能力 的水解能力强于其电离能力 |
您最近一年使用:0次
解题方法
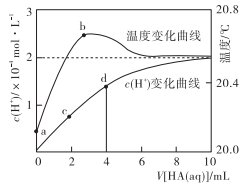
3 . 常温下向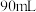 蒸馏水中滴入
蒸馏水中滴入 溶液,已知溶液中的氢离子浓度和温度随
溶液,已知溶液中的氢离子浓度和温度随 溶液体积变化曲线如图所示。下列说法错误的是
溶液体积变化曲线如图所示。下列说法错误的是
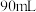 蒸馏水中滴入
蒸馏水中滴入 溶液,已知溶液中的氢离子浓度和温度随
溶液,已知溶液中的氢离子浓度和温度随 溶液体积变化曲线如图所示。下列说法错误的是
溶液体积变化曲线如图所示。下列说法错误的是
A.常温下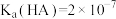 |
B. 过程中温度升高是由于 过程中温度升高是由于 电离放热 电离放热 |
C.在 点时加入 点时加入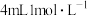 的 的 溶液时存在 溶液时存在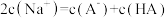 |
D.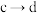 过程中水的电离程度逐渐增大 过程中水的电离程度逐渐增大 |
您最近一年使用:0次
2014高三·全国·专题练习
名校
解题方法
4 . 今有室温下四种溶液,下列有关叙述不正确的是
| 序号 | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A.③和④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大 |
| B.②和③两溶液等体积混合,所得溶液中c(H+)<c(OH-) |
| C.分别加水稀释10倍,四种溶液的pH:①>②>④>③ |
| D.V1 L ④与V2 L ①溶液混合后,若混合后溶液pH=7,则V1<V2 |
您最近一年使用:0次
2021-02-22更新
|
485次组卷
|
58卷引用:新疆石河子第一中学人教版高中化学选修4知识点练习:3.3.2 盐类水解
新疆石河子第一中学人教版高中化学选修4知识点练习:3.3.2 盐类水解(已下线)2014高考名师推荐化学弱电解电离2015届浙江省嘉兴市一中等五校高三上学期第一次联考化学试卷2015届浙江省高三第一次五校联考化学试卷2016届山东省枣庄第三中学高三上10月阶段质检化学试卷2015-2016学年浙江余姚中学高二上学期期中考试化学试卷2015-2016学年黑龙江省大兴安岭实验中学高二上学期期末化学试卷2016-2017学年四川省双流中学高二3月月考化学试卷2018版化学(苏教版)高考总复习专题八课时跟踪训练--弱电解质的电离平衡黑龙江省哈尔滨市第三中学2018届高三上学期(10月)第二次验收考试化学试题河南省商丘市第一高级中学2017-2018学年高二上学期期中考试化学试题贵州省铜仁市第一中学2017-2018学年高二上学期期末考试化学试题福建省晋江市季延中学2017-2018学年高二下学期期末考试化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二(理)10月月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期期末考试化学试题【全国百强校】黑龙江省双鸭山市第一中学2018-2019学年高二下学期开学考试化学试题【全国百强校】内蒙古自治区杭锦后旗奋斗中学2018-2019学年高二下学期期中考试化学试题新疆霍城县江苏中学2018-2019学年高二上学期期末考试化学试题北京市2019—2020学年高二上学期期中考试化学试题(选修4人教版)北京市2019—2020学年高二上学期期末考试模拟试题(选修4人教版 )2019—2020学年高二上学期化学期末复习—选择题专题训练一湖南省株洲市醴陵市第四中学2019-2020学年高二上学期12月月考化学试题(已下线)考点14 化学基本理论——《备战2020年高考精选考点专项突破题集》宁夏石嘴山市第三中学2020届高三12月月考化学试题辽宁省丹东市凤城市第一中学2019-2020学年高二上学期12月月考化学试题黑龙江省哈尔滨市尚志市尚志中学2019-2020学年高二上学期第三次月考化学试题云南省屏边县民族中学2019-2020学年高二上学期12月月考化学试题河南省驻马店市正阳县高级中学2019-2020学年高二上学期第三次素质检测化学试题黑龙江省哈尔滨工业大学附属中学2019-2020学年高二上学期期末考试化学试题安徽省合肥市六校2019-2020学年高二上学期期末考试化学(理)试题云南省陆良县联办高级中学2019-2020学年高二上学期期末考试化学试题安徽省枞阳县浮山中学2019-2020学年高二下学期开学考试化学试题黑龙江省绥化市安达市第七中学2019-2020学年高二下学期期中考试化学试题河北省枣强中学2019-2020学年高二下学期第三次月考化学试题四川省成都龙泉第二中学2021届高三上学期九月月考化学试题江西省高安中学2020-2021学年高二第一次段考化学(B)试题山东省临沂市第四中学2020-2021学年高二11月份阶段检测化学试题四川省成都市简阳市阳安中学2020-2021学年高二上学期期中考试化学试题安徽省肥东县高级中学2020-2021学年高二上学期期中考试化学试题山西省朔州市怀仁县大地学校2020-2021学年高二上学期第三次月考化学试题河南省漯河市漯河实验高中2020-2021学年高二上学期期中考试化学试题甘肃省白银市第十中学2019-2020学年高二上学期期中考试化学试题江西省南昌市第十中学2020-2021学年高二上学期期末考试化学试题湖北省石首市第一中学2020-2021学年高二上学期12月月考化学试题(已下线)【浙江新东方】高中化学20210304-004黑龙江大庆市东风中学2020-2021学年高二下开学测试化学试题湖南省常德市一中2020-2021学年高二下学期第一次月考化学试题(已下线)第24讲 水的电离和溶液的pH(精讲)-2022年一轮复习讲练测(已下线)课时39 弱电解质的电离平衡-2022年高考化学一轮复习小题多维练(全国通用)北京市第十四中学2021-2022学年高二上学期期中考试化学试题湖北省恩施利川市第五中学2019-2020学年高二上学期期中考试化学试题重庆育才中学2021-2022学年高二上学期第三次定时练习化学试题湖南省临澧县第一中学2021-2022学年高二上学期期中段考化学试题湖南省常德市临澧县第一中学2021-2022学年高二上学期期中考试化学试题江西省遂川中学2021-2022学年高二上学期第二次月考化学(A卷)试题四川省峨眉第二中学校2021-2022学年高二下学期5月月考化学试题上海市虹口区2021-2022学年高一下学期联合体期末模拟考试化学试题湖北省潜江市华中师范大学潜江附属中学2021-2022学年高二上学期期中考试化学试题
名校
5 . 常温下,向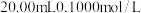 的
的 溶液中滴加
溶液中滴加 的
的 溶液,溶液中,
溶液,溶液中,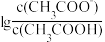 随pH的变化关系如图所示(取
随pH的变化关系如图所示(取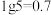 )。
)。
下列说法正确的是
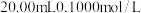 的
的 溶液中滴加
溶液中滴加 的
的 溶液,溶液中,
溶液,溶液中,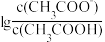 随pH的变化关系如图所示(取
随pH的变化关系如图所示(取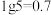 )。
)。
下列说法正确的是
A.常温下, 的电离常数为 的电离常数为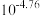 |
B.当溶液的 时,消耗 时,消耗 溶液 溶液 |
| C.溶液中水的电离程度大小:a>b>c |
D.c点溶液中: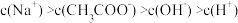 |
您最近一年使用:0次
2021-01-25更新
|
1836次组卷
|
9卷引用:选择性必修1(SJ)专题3专题培优专练
选择性必修1(SJ)专题3专题培优专练湖南省2021年普通高中学业水平选择考适应性测试化学试题“山东六校”2020-2021学年高二下学期(4月)阶段性联合考试化学(A卷)试题(已下线)难点7 溶液稀释与酸碱中和滴定曲线分析-2021年高考化学【热点·重点·难点】专练(新高考)(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题21 电解质溶液图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题11 水溶液中的离子平衡图像(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(已下线)专题四 电解质溶液图象(练)山东省青岛第十七中学2023-2024学年高二上学期12月月考化学试题
20-21高二上·全国·课时练习
名校
解题方法
6 . 实验测得0.5mol•L-1CH3COONa溶液和H2O的pH随温度变化的曲线如图所示。下用说法正确的是
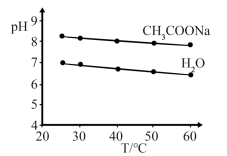

| A.随温度升高,CH3COONa溶液的c(OH-)增大 |
| B.随温度升高,H2O的pH逐渐减小,是因为水中c(H+)>c(OH-) |
| C.随温度升高,CH3COONa溶液的pH变化是Kw改变和水解平衡移动共同作用的结果 |
| D.随温度升高,CH3COONa溶液的pH降低是因为CH3COO-水解平衡向逆反应方向移动的结果 |
您最近一年使用:0次
名校
7 . 25℃时,将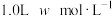 的
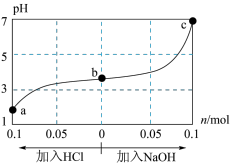
的 溶液与0.1mol NaOH固体混合,充分反应后向混合溶液中通(加)入HCl气体或NaOH固体。溶液pH随通(加)入HCl或NaOH的物质的量的变化如图所示。下列叙述正确的是( )
溶液与0.1mol NaOH固体混合,充分反应后向混合溶液中通(加)入HCl气体或NaOH固体。溶液pH随通(加)入HCl或NaOH的物质的量的变化如图所示。下列叙述正确的是( )
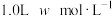 的
的 溶液与0.1mol NaOH固体混合,充分反应后向混合溶液中通(加)入HCl气体或NaOH固体。溶液pH随通(加)入HCl或NaOH的物质的量的变化如图所示。下列叙述正确的是( )
溶液与0.1mol NaOH固体混合,充分反应后向混合溶液中通(加)入HCl气体或NaOH固体。溶液pH随通(加)入HCl或NaOH的物质的量的变化如图所示。下列叙述正确的是( )
A.a、b、c对应的混合液中,水的电离程度由大到小的顺序是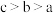 |
B.c点溶液中,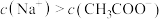 |
C.加入NaOH过程中,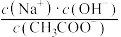 减小 减小 |
D.若忽略体积变化,则25℃, 的电离平衡常数 的电离平衡常数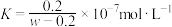 |
您最近一年使用:0次
2020-10-11更新
|
604次组卷
|
5卷引用:鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过综合 章末素养综合检测
鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过综合 章末素养综合检测人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 过综合 章末素养综合检测(已下线)全册综合检测(一)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)四川省大竹中学2021-2022学年高二上学期期中达标测化学试题(提高卷)山东省威海乳山市银滩高级中学2021-2022学年高二12月月考化学试题
8 . 下列关于强、弱电解质的叙述错误的是( )
| A.强电解质在水溶液中完全电离成阴阳离子 |
| B.在水溶液中,导电能力强的电解质是强电解质 |
| C.弱电解质在溶液中以阴、阳离子的形式存在 |
| D.强电解质在熔融态时,有的导电,有的不导电 |
您最近一年使用:0次
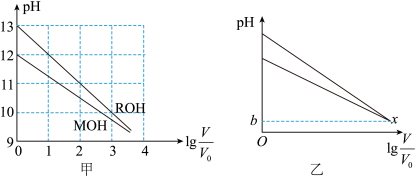
9 . 常温下,浓度均为 、体积均为
、体积均为 的MOH和ROH两种碱溶液,分别加水稀释至体积为V,溶液pH随
的MOH和ROH两种碱溶液,分别加水稀释至体积为V,溶液pH随 的变化如图甲所示。图乙中,
的变化如图甲所示。图乙中, 时,两曲线出现交叉点x。下列叙述正确的是
时,两曲线出现交叉点x。下列叙述正确的是
 、体积均为
、体积均为 的MOH和ROH两种碱溶液,分别加水稀释至体积为V,溶液pH随
的MOH和ROH两种碱溶液,分别加水稀释至体积为V,溶液pH随 的变化如图甲所示。图乙中,
的变化如图甲所示。图乙中, 时,两曲线出现交叉点x。下列叙述正确的是
时,两曲线出现交叉点x。下列叙述正确的是
A. 、 、 均不能确定其数值大小 均不能确定其数值大小 |
| B.x点时,将两种碱溶液等体积混合,混合溶液的pH不变(假设两溶液混合后的体积为二者体积之和) |
| C.x点时,两种溶液中水的电离程度相等 |
D. 相同时,将两种溶液同时升高相同的温度,则 相同时,将两种溶液同时升高相同的温度,则 减小 减小 |
您最近一年使用:0次
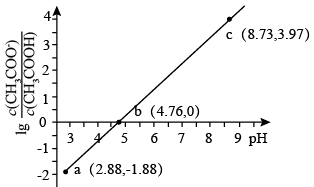
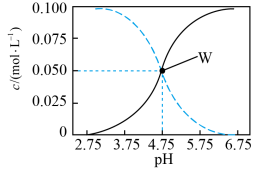
10 . 25℃时,有 的一组醋酸、醋酸钠混合溶液,溶液中
的一组醋酸、醋酸钠混合溶液,溶液中 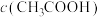 、
、 与pH的关系如图所示。下列有关溶液中粒子浓度关系的叙述正确的是
与pH的关系如图所示。下列有关溶液中粒子浓度关系的叙述正确的是
 的一组醋酸、醋酸钠混合溶液,溶液中
的一组醋酸、醋酸钠混合溶液,溶液中 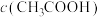 、
、 与pH的关系如图所示。下列有关溶液中粒子浓度关系的叙述正确的是
与pH的关系如图所示。下列有关溶液中粒子浓度关系的叙述正确的是
A. 的溶液中: 的溶液中: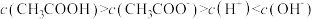 |
B.W点所表示的溶液中: |
C. 的溶液中: 的溶液中: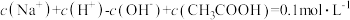 |
D.向W点所表示的1.0L溶液中通入0.05mol HCl气体(溶液体积变化可忽略):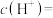 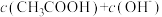 |
您最近一年使用:0次



