解题方法
1 . 纳米CaCO3作为工业上重要的无机填充材料,广泛应用于橡胶、塑料、涂料、油墨和造纸等行业。某化学兴趣小组在实验室中利用下列装置模拟工业制备纳米CaCO3.
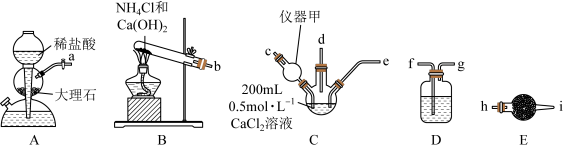
请回答下列问题:
(1)仪器甲的名称是________ ,在该实验中,其作用是_____ 。
(2)将上述接口连接顺序补充完整:a ;b
;b ;d
;d 。
。__________
(3)装置D中选择的试剂是_______ (填序号,下同),装置E中选择的试剂是_______
①饱和Na2CO3溶液 ②饱和NaHCO3溶液 ③无水CaCl2固体 ④碱石灰
(4)装置C中发生反应的离子方程式为__________
(5)随着气体的通入,三颈烧瓶中产生白色沉淀且逐渐增多,但一段时间后,白色沉淀逐渐减少,其可能的原因为_______ (结合化学用语解释)。
(6)当生成5g沉淀时,理论上消耗两种气体(标准状况下)的总体积可能为_________
(7)已知:常温下,Ksp(CaCO3)=2.8×10-9,Ksp(CaSO3)=1.4×10-7。向浓度为1.0mol/L的Na2SO3溶液中加入纳米CaCO3,若使CaCO3向CaSO3转化,则该混合液中c(SO )/c(CO
)/c(CO )的值(x)的取值范围为
)的值(x)的取值范围为__________ 。
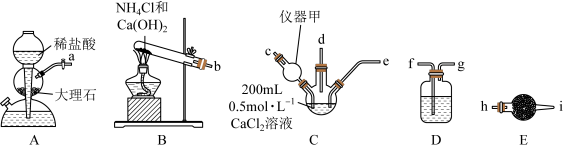
请回答下列问题:
(1)仪器甲的名称是
(2)将上述接口连接顺序补充完整:a
 ;b
;b ;d
;d 。
。(3)装置D中选择的试剂是
①饱和Na2CO3溶液 ②饱和NaHCO3溶液 ③无水CaCl2固体 ④碱石灰
(4)装置C中发生反应的离子方程式为
(5)随着气体的通入,三颈烧瓶中产生白色沉淀且逐渐增多,但一段时间后,白色沉淀逐渐减少,其可能的原因为
(6)当生成5g沉淀时,理论上消耗两种气体(标准状况下)的总体积可能为
(7)已知:常温下,Ksp(CaCO3)=2.8×10-9,Ksp(CaSO3)=1.4×10-7。向浓度为1.0mol/L的Na2SO3溶液中加入纳米CaCO3,若使CaCO3向CaSO3转化,则该混合液中c(SO
 )/c(CO
)/c(CO )的值(x)的取值范围为
)的值(x)的取值范围为
您最近一年使用:0次
2 . 以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)为原料,制备粗铅,实现铅的再生利用。其工作流程如下图所示:
已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-14。
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是__________ 。
(2)过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++ PbO2+4H++SO42- 2Fe3++PbSO4+2H2O
2Fe3++PbSO4+2H2O
ii: ……
①写出ii的离子方程式:________________ 。
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.___________ 。
(3)过程Ⅱ的目的是脱硫。若滤液2中c(SO42-)=1.6mol/L,c(CO32-)=0.1mol/L,则PbCO3中____ (填“是”或“否”)混有PbSO4。
(4)钠离子交换膜固相电解法是从含铅废料中提取铅的一种新工艺,其装置如图所示。将含铅废料投入阴极室,含铅废料中的PbSO4与NaOH溶液发生反应:PbSO4+3OH-=HPbO2-+SO42-+H2O。

①a与外接电源的________ 极相连。
②电解过程中,PbO2、PbO、HPbO2-在阴极放电,其中PbO2放电的电极反应式为___________ 。
③与传统无膜固相电解法相比,使用钠离子交换膜可以 提高Pb元素的利用率,原因是________ 。

已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-14。
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是
(2)过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++ PbO2+4H++SO42-
 2Fe3++PbSO4+2H2O
2Fe3++PbSO4+2H2Oii: ……
①写出ii的离子方程式:
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.
(3)过程Ⅱ的目的是脱硫。若滤液2中c(SO42-)=1.6mol/L,c(CO32-)=0.1mol/L,则PbCO3中
(4)钠离子交换膜固相电解法是从含铅废料中提取铅的一种新工艺,其装置如图所示。将含铅废料投入阴极室,含铅废料中的PbSO4与NaOH溶液发生反应:PbSO4+3OH-=HPbO2-+SO42-+H2O。

①a与外接电源的
②电解过程中,PbO2、PbO、HPbO2-在阴极放电,其中PbO2放电的电极反应式为
③与传统无膜固相电解法相比,使用钠离子交换膜可以 提高Pb元素的利用率,原因是
您最近一年使用:0次
2017-03-16更新
|
749次组卷
|
3卷引用:2017届湖南省长沙市长望浏宁四县高三3月模拟考试理综化学试卷
名校
解题方法
3 . 醋酸亚铬水合物 {[(CH3COO)2Cr]2·2H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水,是常用的氧气吸收剂。实验室中以锌粒、三氯化铬溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如图所示,且仪器2中预先加入锌粒。已知二价铬不稳定,极易被氧气氧化,不与锌反应。制备过程中发生的相关反应如下:
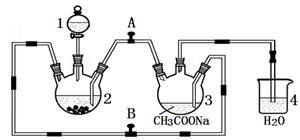
Zn(s)+ 2HCl(aq)=ZnCl2(aq)+ H2(g);
2CrCl3(aq)+Zn(s)= 2CrCl2(aq)+ ZnCl2(aq)
2Cr2+(aq)+ 4CH3COO—(aq)+ 2H2O(l)=[(CH3COO)2Cr]2·2H2O(s)
请回答下列问题:
(1)仪器1的名称是______________________________________ 。
(2)往仪器2中加盐酸和三氯化铬溶液的顺序最好是____________ (填序号);目的是_________________________ 。
A.盐酸和三氯化铬溶液同时加入
B.先加三氯化铬溶液,一段时间后再加盐酸
C.先加盐酸,一段时间后再加三氯化铬溶液
(3)为使生成的CrCl2溶液与醋酸钠溶液顺利混合,应关闭阀门_____ (填“A”或“B",下同),打开阀门____ 。
(4)本实验中锌粒要过量,其原因除了让产生的H2将CrCl2溶液压入装置3与醋酸钠溶液反应外,另一个作用是_____________________________________________ 。
(5)已知其他反应物足量,实验时取用的CrCl3溶液中含溶质9.51g,取用的醋酸钠溶液为1.5L0.1mol/L;实验后得干燥纯净的[(CH3COO)2Cr]2·2H2O 9.4g,则该实验所得产品的产率为____________ (不考虑溶解的醋酸亚铬水合物)。
(6)铬的离子会污染水,常温下要除去上述实验中多余的Cr2+,最好往废液中通入足量的_______ ,再加入碱液,调节pH至少为_______ 才能是铬的离子沉淀完全(铬的离子浓度应小于10-5mol/L)。【已知Cr(OH)3的溶度积为6.3×10-31,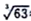 ≈4,lg2≈0.3】
≈4,lg2≈0.3】

Zn(s)+ 2HCl(aq)=ZnCl2(aq)+ H2(g);
2CrCl3(aq)+Zn(s)= 2CrCl2(aq)+ ZnCl2(aq)
2Cr2+(aq)+ 4CH3COO—(aq)+ 2H2O(l)=[(CH3COO)2Cr]2·2H2O(s)
请回答下列问题:
(1)仪器1的名称是
(2)往仪器2中加盐酸和三氯化铬溶液的顺序最好是
A.盐酸和三氯化铬溶液同时加入
B.先加三氯化铬溶液,一段时间后再加盐酸
C.先加盐酸,一段时间后再加三氯化铬溶液
(3)为使生成的CrCl2溶液与醋酸钠溶液顺利混合,应关闭阀门
(4)本实验中锌粒要过量,其原因除了让产生的H2将CrCl2溶液压入装置3与醋酸钠溶液反应外,另一个作用是
(5)已知其他反应物足量,实验时取用的CrCl3溶液中含溶质9.51g,取用的醋酸钠溶液为1.5L0.1mol/L;实验后得干燥纯净的[(CH3COO)2Cr]2·2H2O 9.4g,则该实验所得产品的产率为
(6)铬的离子会污染水,常温下要除去上述实验中多余的Cr2+,最好往废液中通入足量的
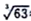 ≈4,lg2≈0.3】
≈4,lg2≈0.3】
您最近一年使用:0次
2018-01-17更新
|
1015次组卷
|
3卷引用:湖南省郴州市2018届高三第二次教学质量监测理科综合化学试题
4 . 高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性。
(1)已知:4 +10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有
+10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有___ 。
同浓度的高铁酸钾在pH为4.74、7.00、11.50的水溶液中最稳定的是pH=_______ 的溶液。
(2)高铁酸钾有以下几种常见制备方法:

①干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为___________ 。
②湿法制备中,若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:___________________________________ 。
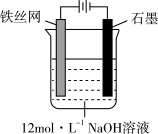
③制备中间产物Na2FeO4,可采用的装置如图所示,则阳极的电极反应式为_______________ 。
(3)比亚迪双模电动汽车使用高铁电池供电,其总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化
3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化_______________ ,正极反应为:____________________ 。
(4)25℃时,CaFeO4的Ksp=4.54×l0-9,若要使1000 L含有2.0×l0-4 mol·L-l K2FeO4的废水中的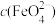 有沉淀产生,理论上至少加入Ca(OH)2的物质的量为
有沉淀产生,理论上至少加入Ca(OH)2的物质的量为________ mol。
(1)已知:4
 +10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有
+10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有同浓度的高铁酸钾在pH为4.74、7.00、11.50的水溶液中最稳定的是pH=
(2)高铁酸钾有以下几种常见制备方法:

①干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为
②湿法制备中,若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:
③制备中间产物Na2FeO4,可采用的装置如图所示,则阳极的电极反应式为

(3)比亚迪双模电动汽车使用高铁电池供电,其总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化
3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化(4)25℃时,CaFeO4的Ksp=4.54×l0-9,若要使1000 L含有2.0×l0-4 mol·L-l K2FeO4的废水中的
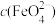 有沉淀产生,理论上至少加入Ca(OH)2的物质的量为
有沉淀产生,理论上至少加入Ca(OH)2的物质的量为
您最近一年使用:0次



