名校
解题方法
1 . 下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 比较 和 和 的 的 | 向盛有 溶液的试管中先加入足量 溶液的试管中先加入足量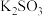 溶液,滤出沉淀后,向沉淀中加入 溶液,滤出沉淀后,向沉淀中加入 溶液,观察现象 溶液,观察现象 |
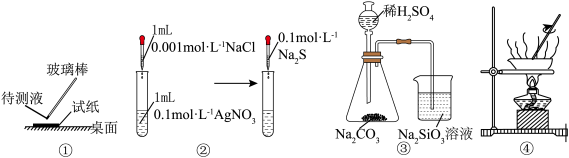
| B | 配制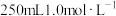 的NaOH溶液 的NaOH溶液 | 将10gNaOH固体放入小烧杯中溶解,转移至250mL容量瓶中,定容 |
| C | 验证 的还原性 的还原性 | 将电石与饱和食盐水反应生成的气体通入酸性高锰酸钾溶液中,观察颜色变化 |
| D | 制备氢氧化铁胶体 | 向沸水中滴入5~6滴饱和氯化铁溶液,继续煮沸至溶液呈红褐色,停止加热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 下列操作或装置能达到实验目的的是

| A.图丁制备NO并用排CO2法收集 | B.图甲证明KSP(AgBr)>KSP(AgI) |
| C.图乙装置构成原电池 | D.图丙探究浓度对反应速率的影响 |
您最近一年使用:0次
名校
解题方法
3 . 用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的的是( )

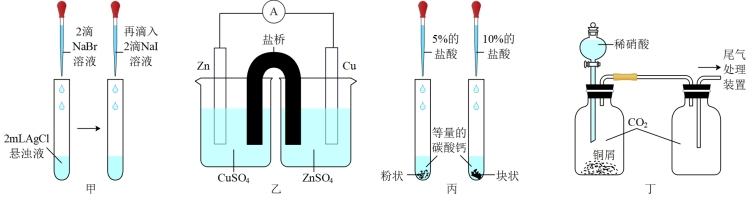
| A.①用pH试纸测某溶液的酸碱性 |
| B.实验室用图②所示装置若先出现白色沉淀后又变黑,则能比较Ksp(AgCl)﹥Ksp(Ag2S) |
| C.实验室用图③所示装置证明酸性:H2SO4>H2CO3>H2SiO3 |
| D.图④可由AlCl3饱和溶液制备AlCl3晶体 |
您最近一年使用:0次
2019-12-21更新
|
177次组卷
|
4卷引用:湖南广益实验中学2019-2020学年高二上学期期末考试化学试题
名校
4 . 三氯氧磷POCl3是一种化工原料,可用于制取有机磷农药、长效磺胺药物等,还可用作染料中间体、有机合成的氯化剂和催化剂、阻燃剂等。利用O2和PCl3为原料可制备三氯氧磷,其制备装置如图所示(夹持装置略去):
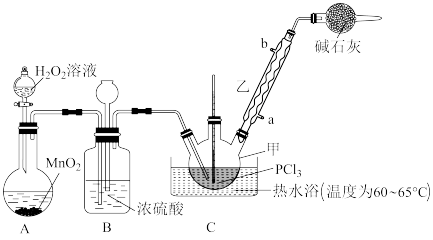
已知 和三氯氧磷的性质如表:
和三氯氧磷的性质如表:
回答下列问题:
(1)装置A中的分液漏斗能否用长颈漏斗代替____ ?做出判断并分析原因:___________ 。
(2)装置B的作用是___________(填标号)。
(3)干燥管中碱石灰的作用___________ 。
(4)写出装置C中发生反应的化学方程式____ 。
(5)通过佛尔哈德法可以测定三氯氧磷产品中Cl素含量,实验步骤如下:
Ⅰ.取ag产品于锥形瓶中,加入足量NaOH溶液待完全水解后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000 的AgNO3溶液40.00 mL,使Cl-完全沉淀。
的AgNO3溶液40.00 mL,使Cl-完全沉淀。
Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀面被有机物覆盖。
Ⅳ.加入指示剂,用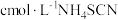 溶液滴过量
溶液滴过量 至终点,记下所用体积为
至终点,记下所用体积为 。
。
已知: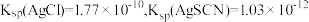
①滴定选用的指示剂是___________ (填标号),滴终点的现象为___________ 。
a. b.
b.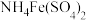 c.淀粉 d.甲基橙
c.淀粉 d.甲基橙
②实验过程中加入硝基苯的目的是___________ ,如无此操作所测Cl元素含量将___________ (填“偏大”“偏小”或“不变”)。
③所测Cl元素含量为___________ 。

已知
 和三氯氧磷的性质如表:
和三氯氧磷的性质如表:| 熔点/℃ | 沸点/℃ | 其他物理或化学性质 | |
| PCl3 | -112.0 | 76.0 | PCl3和POCl3互溶,均为无色液体,遇水均剧烈水解,发生复分解反应生成磷的含氧酸和HCl |
| POCl3 | 1.25 | 106.0 |
(1)装置A中的分液漏斗能否用长颈漏斗代替
(2)装置B的作用是___________(填标号)。
| A.干燥气体 | B.加注浓硫酸 | C.观察气体流出速度 | D.调节气压 |
(4)写出装置C中发生反应的化学方程式
(5)通过佛尔哈德法可以测定三氯氧磷产品中Cl素含量,实验步骤如下:
Ⅰ.取ag产品于锥形瓶中,加入足量NaOH溶液待完全水解后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000
 的AgNO3溶液40.00 mL,使Cl-完全沉淀。
的AgNO3溶液40.00 mL,使Cl-完全沉淀。Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀面被有机物覆盖。
Ⅳ.加入指示剂,用
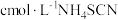 溶液滴过量
溶液滴过量 至终点,记下所用体积为
至终点,记下所用体积为 。
。已知:
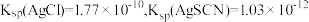
①滴定选用的指示剂是
a.
 b.
b.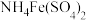 c.淀粉 d.甲基橙
c.淀粉 d.甲基橙②实验过程中加入硝基苯的目的是
③所测Cl元素含量为
您最近一年使用:0次
2022-03-26更新
|
669次组卷
|
3卷引用:湖南省吉首市泸溪一中2022届高三第三次联合检测化学试题
5 . PbCl2是一种重要的化工材料,常用作助溶剂、制备铅黄等染料。工业生产中利用方铅矿(主要成分为PbS,含有FeS2等杂质)和软锰矿(主要成分为MnO2)制备PbCl2的工艺流程如图所示。
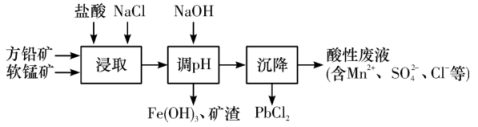
已知:
ⅰ.PbCl2微溶于水
ⅱ.PbCl2(s)+2Cl-(aq) PbCl
PbCl (aq)ΔH>0
(aq)ΔH>0
(1)浸取过程中MnO2与PbS发生反应的离子反应方程式为__ 。
(2)由于PbCl2微溶于水,容易附着在方铅矿表面形成“钝化层”使反应速率大大降低,浸取剂中加入饱和NaCl溶液可有效避免这一现象,原因是__ 。
(3)调pH的目的是__ 。
(4)沉降池中获得PbCl2采取的两种措施是__ 。(根据平衡的观点)
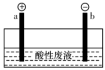
(5)通过电解酸性废液可重新获得MnO2,装置示意图如图,获得MnO2的电极反应式为__ 。

已知:
ⅰ.PbCl2微溶于水
ⅱ.PbCl2(s)+2Cl-(aq)
 PbCl
PbCl (aq)ΔH>0
(aq)ΔH>0(1)浸取过程中MnO2与PbS发生反应的离子反应方程式为
(2)由于PbCl2微溶于水,容易附着在方铅矿表面形成“钝化层”使反应速率大大降低,浸取剂中加入饱和NaCl溶液可有效避免这一现象,原因是
(3)调pH的目的是
(4)沉降池中获得PbCl2采取的两种措施是
(5)通过电解酸性废液可重新获得MnO2,装置示意图如图,获得MnO2的电极反应式为

您最近一年使用:0次
名校
解题方法
6 . 下列方案设计或现象和结论均完全正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 比较CH3COONa与NaClO酸性 | 室温下,用pH试纸分别测定室温下,用pH试纸分别测定 | NaClO溶液pH较大,则酸性:CH3COOH>HClO |
| B | 探究侯氏制碱法 | 向饱和食盐水中先通入二氧化碳至饱和后,再通入过量氨气 | 溶液变浑浊,析出NaHCO3 |
| C | 比较AgCl、AgI的Ksp大小 | 向5mL0.1mol/LAgNO3溶液中先加入4滴0.1mol/LNaCl溶液,再加入4滴0.1mol/LKI溶液 | 若先产生白色沉淀,后变为黄色沉淀,则AgI的Ksp较小 |
| D | 探究Na2SO3是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入BaCl2溶液 | 若有白色沉淀产生,则样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 下列实验方法或操作能达到相应实验目的的是
| 实验目的 | 实验方法或操作 | |
| A | 测定中和反应的反应热 | 酸碱中和滴定的同时,用温度传感器采集锥形瓶内溶液的温度数据并进行计算 |
| B | 探究铜配离子的转化 | 向蓝色硫酸铜溶液中滴加氨水,先生成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色溶液,再加入乙醇,析出深蓝色晶体 |
| C | 检验氯乙烷中的氯元素 | 向氯乙烷中滴加1 mL5%的NaOH溶液,振荡后加热,静置。待溶液分层后,取少量上层溶液,滴加2滴AgNO3溶液,观察现象 |
| D | 重结晶法提纯苯甲酸 | 趁热过滤后将滤液快速冷却结晶,提纯效果更好 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-18更新
|
792次组卷
|
4卷引用:湖南省部分学校2023届高三下学期5月联考化学试题
湖南省部分学校2023届高三下学期5月联考化学试题广东省部分学校2023届高三5月联合考试化学试题(已下线)考点巩固卷12 化学实验基础(一)(3大考点67题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题11 化学实验(选择题)-2023年高考化学真题题源解密(新高考专用)
解题方法
8 . 下列实验过程可以达到实验目的的是
| 选项 | 实验目的 | 实验过程 |
| A | 比较常温下Ksp(BaSO4)与Ksp(BaCO3)大小 | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤后向洗净的沉淀中加稀盐酸,有少量气泡产生 |
| B | 探究浓度对反应速率的影响 | 量取相同体积、不同浓度的盐酸,分别与等质量的大理石发生反应,对比实验现象 |
| C | 验证Na2CO3溶液中存在CO 的水解平衡 的水解平衡 | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,观察溶液的颜色变化 |
| D | 探究Cl2、Br2和I2的氧化性强弱 | 向NaBr溶液中通入过量氯气,再滴加淀粉KI溶液,观察溶液的颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 下列实验目的对应的方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 检验溶液中是否含钠元素 | 将蘸取溶液的玻璃棒放在无色火焰上灼烧 | 火焰出现黄色,说明溶液中含钠元素 |
| B | 在 时,比较 时,比较 与 与 结合 结合 能力强弱 能力强弱 | 向 溶液中,先加NaOH溶液调节 溶液中,先加NaOH溶液调节 ,再加入足量的KSCN溶液 ,再加入足量的KSCN溶液 | 红褐色沉淀不溶解,说明在 时, 时, 结合 结合 的能力更强 的能力更强 |
| C | 比较T℃时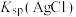 与 与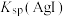 的大小 的大小 | T℃时,向等体积的饱和AgCl、AgI溶液中分别滴加足量 溶液 溶液 | 所得沉淀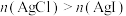 ,则 ,则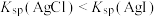 |
| D | 比较亚硫酸与碳酸的酸性强弱 | 分别测定 、 、 饱和溶液的pH 饱和溶液的pH | 前者小,说明亚硫酸酸性更强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 下列实验过程能达到目的,且现象和结论正确的是
| 选项 | 实验目的 | 实验过程 | 现象和结论 |
| A | 比较AgCl和AgI的 大小 大小 | 向2mL0.1mol/L 溶液中滴2滴0.1mol/LNaCl溶液,产生白色沉淀后再滴加2滴0.1mol/LKI溶液 溶液中滴2滴0.1mol/LNaCl溶液,产生白色沉淀后再滴加2滴0.1mol/LKI溶液 | 又生成黄色沉淀,说明 |
| B | 探究不同催化剂对反应速率的影响 | 在两支大小相同的试管中均加2mL5% 溶液,分别滴入2滴1mol/L 溶液,分别滴入2滴1mol/L 溶液和1mol/L 溶液和1mol/L 溶液 溶液 | 加 溶液的试管产生气泡速率更快,说明 溶液的试管产生气泡速率更快,说明 的催化效果强于 的催化效果强于 |
| C | 比较HCN、 的 的 大小 大小 | 用pH计分别测定浓度均为0.1mol/L的NaCN和 的pH 的pH |  的pH更大,所以 的pH更大,所以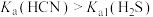 |
| D | 探究可逆反应的热效应 | 已知 溶液中存在下列平衡: 溶液中存在下列平衡: (蓝) (蓝)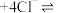 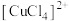 (黄) (黄) ,取一定浓度的 ,取一定浓度的 溶液,升高温度 溶液,升高温度 | 溶液由蓝色变为黄色,说明该反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-22更新
|
257次组卷
|
2卷引用:湖南省长沙市麓山国际实验学校2023-2024学年高三上学期第一次月考化学试题



