解题方法
1 . 地壳中铈占稀土总量的28%,居第一位。铈主要存在于独居石和氟碳铈矿中,其中氧化焙烧—萃取法冶炼氟碳铈矿(含CeFCO3、BaO、SiO2等)制取CeO2的一种工艺流程如图所示:
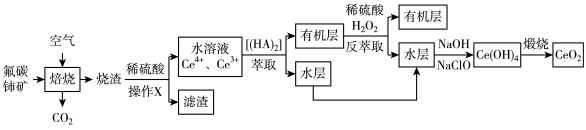
资料:在硫酸体系中,Ce4+在[(HA)2]中的溶解度大于其在水中的溶解度,Ce3+与之相反。回答下列问题:
(1)氟碳铈中元素的化合价为____ ,焙烧过程中,为加快反应速率可采取的措施有____ (答出一条即可)。
(2)操作X的名称为____ ,实验室中进行操作X需要用到的玻璃仪器有烧杯、____ 和____ 。
(3)反萃取中的离子方程式为____ 。
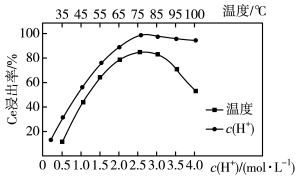
(4)烧渣中加入稀硫酸浸出,Ce的浸出率与c(H+)、温度的关系如图所示,从c(H+)角度考虑应选择的最佳条件为____ 。
(5)常温下,向水层中加入NaOH溶液来调节溶液的pH,当溶液pH=8时,Ce3+____ (填“是”或“否”)沉淀完全。{已知离子浓度小于1.0×10-5mol·L-1时,认为沉淀完全,Ksp[Ce(OH)3]=1.0×10-20)。
(6)取上述流程中得到的CeO2产品0.9200g,加酸溶解后,向其中加入150.0mL0.1mol·L-1FeSO4溶液使Ce4+全部被还原成Ce3+,再用0.1000mol·L-1的酸性KMnO4标准溶液滴定上述溶液,至终点时,消耗20.00mL标准溶液。则该产品中CeO2的质量分数为____ %(保留两位小数)(已知氧化性:Ce4+>KMnO4)。

资料:在硫酸体系中,Ce4+在[(HA)2]中的溶解度大于其在水中的溶解度,Ce3+与之相反。回答下列问题:
(1)氟碳铈中元素的化合价为
(2)操作X的名称为
(3)反萃取中的离子方程式为
(4)烧渣中加入稀硫酸浸出,Ce的浸出率与c(H+)、温度的关系如图所示,从c(H+)角度考虑应选择的最佳条件为

(5)常温下,向水层中加入NaOH溶液来调节溶液的pH,当溶液pH=8时,Ce3+
(6)取上述流程中得到的CeO2产品0.9200g,加酸溶解后,向其中加入150.0mL0.1mol·L-1FeSO4溶液使Ce4+全部被还原成Ce3+,再用0.1000mol·L-1的酸性KMnO4标准溶液滴定上述溶液,至终点时,消耗20.00mL标准溶液。则该产品中CeO2的质量分数为
您最近一年使用:0次
2 . 下列实验操作、现象和结论都正确的是
| 实验操作 | 现象 | 结论 | |
| A | 在苯酚水溶液中滴加饱和溴水 | 溴水褪色 | 发生了取代反应 |
| B | 分别在 、 、 浊液中滴加浓氨水 浊液中滴加浓氨水 | 前者溶解,后者不溶 | 碱性: |
| C | 在稀硫酸中加入少量的红色 粉末 粉末 | 产生蓝色溶液和红色固体 |  在该反应中既体现氧化性,又体现还原性 在该反应中既体现氧化性,又体现还原性 |
| D | 在含 和 和 的溶液中滴加 的溶液中滴加 溶液 溶液 | 先生成黑色沉淀,后生成白色沉淀 | 溶度积: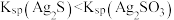 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 某小组同学以AgCl和AgI为例探究物质的溶解度大小与沉淀转化方向之间的关系。已知:
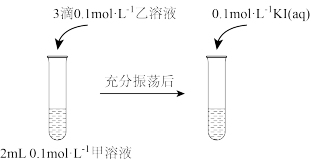
实验Ⅰ:
实验Ⅱ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数: )。
)。
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
请回答下列问题:
(1)实验Ⅰ证明了AgCl转化为AgI,甲溶液可以是_______ (填标号)。
a. 溶液 b.NaCl溶液 c.KI溶液
溶液 b.NaCl溶液 c.KI溶液
(2)实验Ⅰ沉淀转化反应的离子方程式是_______ 。AgCl和AgI共存的悬浊液中,
_______ (保留一位小数)。[已知: ,
,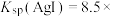
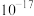 ]
]
(3)实验Ⅱ的步骤ⅰ中,B中石墨上的电极反应是_______ 。
(4)结合信息解释实验Ⅱ中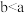 的原因:
的原因:_______ 。
(5)实验Ⅱ的现象能说明AgI转化为AgCl,理由是_______ 。
| 物质 | AgI | AgCl |
| 溶解度/g(20℃) |  | 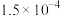 |

实验Ⅱ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:
 )。
)。| 装置 | 步骤 | 电压表读数 |
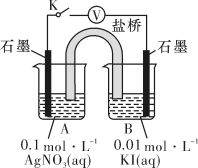 | ⅰ.按图连接装置并加入试剂,闭合K | a |
ⅱ.向B中滴入 (aq),至沉淀完全 (aq),至沉淀完全 | b | |
| ⅲ.再向B中投入一定量NaCl(s) | c | |
| ⅳ.重复ⅰ,再向B中加入与ⅲ等量的NaCl(s) | a |
请回答下列问题:
(1)实验Ⅰ证明了AgCl转化为AgI,甲溶液可以是
a.
 溶液 b.NaCl溶液 c.KI溶液
溶液 b.NaCl溶液 c.KI溶液(2)实验Ⅰ沉淀转化反应的离子方程式是

 ,
,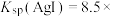
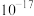 ]
](3)实验Ⅱ的步骤ⅰ中,B中石墨上的电极反应是
(4)结合信息解释实验Ⅱ中
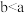 的原因:
的原因:(5)实验Ⅱ的现象能说明AgI转化为AgCl,理由是
您最近一年使用:0次
名校
解题方法
4 . 下列有关实验的现象和解释或结论都正确的是
| 实验操作 | 现象 | 解释或结论 | |
| A | 两支试管各盛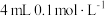 酸性高锰酸钾溶液,分别加入 酸性高锰酸钾溶液,分别加入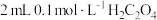 溶液和 溶液和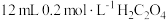 溶液 溶液 | 加入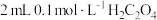 溶液的试管中,酸性高锰酸钾溶液褪色更快 溶液的试管中,酸性高锰酸钾溶液褪色更快 | 反应物浓度越大,反应速率越快 |
| B | 将稀硫酸酸化的 溶液滴入 溶液滴入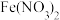 溶液中 溶液中 | 溶液变黄色 | 氧化性: 比 比 强 强 |
| C | 向盛有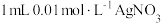 溶液的试管中滴加5滴 溶液的试管中滴加5滴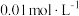 的 的 溶液,再滴加5滴 溶液,再滴加5滴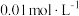 的 的 溶液 溶液 | 先有白色沉淀生成,后沉淀又转化为黄色沉淀 | 此温度下: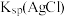 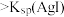 |
| D | 取 蔗糖溶液,加入3滴稀 蔗糖溶液,加入3滴稀 ,水浴加热 ,水浴加热 ,冷却后加入 ,冷却后加入 溶液调至碱性,再加入少量新制 溶液调至碱性,再加入少量新制 悬浊液,加热 悬浊液,加热 | 有砖红色沉淀产生 | 蔗糖发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 下列有关实验的现象和解释或结论都正确的是
| 实验操作 | 现象 | 解释或结论 | |
| A | 两支试管各盛4mL0.1mol·L-1酸性高锰酸钾溶液,分别加入2mL0.1mol·L-1H2C2O4溶液和2mL0.2mol·L-1H2C2O4溶液 | 加入2 mL 0.2 mol·L-1 H2C2O4溶液的试管中,酸性高锰酸钾溶液褪色更快 | 反应物浓度越大,反应速率越快 |
| B | 将稀硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中 | 溶液变黄色 | 氧化性:H2O2比Fe3+强 |
| C | 向盛有1mL0.01mol·L-1AgNO3溶液的试管中滴加5滴0.01mol·L-1的NaCl溶液,再滴加5滴0.01mol·L-1的NaI溶液 | 先有白色沉淀生成,后沉淀又转化为黄色沉淀 | 此温度下:Ksp(AgCl)>Ksp(AgI) |
| D | 取1mL蔗糖溶液,加入3滴稀H2SO4,水浴加热5min,冷却后加入NaOH溶液调至碱性,再加入少量新制Cu(OH)2悬浊液,加热 | 有砖红色沉淀产生 | 蔗糖发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 一种从废旧锂电池(主要含LiCoO2,及少量Al、Cu)中制备钴酸锂(LiCoO2)的工艺流程如下:

查阅资料:LiCoO2具有很强的氧化性
(1)LiCoO2中,Co的化合价为___________ 。
(2)写出“碱浸泡”发生反应的离子方程式:___________ ,为提高该物质的去除率可采取的措施有___________ (任写两条)。
(3)向“残渣”中加入稀硫酸和H2O2,放出大量气泡,写出LiCoO2与H2O2反应的化学方程式:___________ 。
(4)若废旧的锂电池拆解后先使用酸溶解,最终也可以得到Al(OH)3、CoSO4、Li2CO3。在酸浸中若Al3+浓度为0.1mol·L-1,则常温时pH>___________ 才能够开始形成氢氧化铝沉淀(已知氢氧化铝Ksp=1.3×10-33、1g4.26=0.6、 =2.35)。
=2.35)。
(5)RH萃取Cu2+的原理可表示为:Cu2++2HR CuR2+2H+。实验室进行萃取实验用到的两种玻璃仪器是
CuR2+2H+。实验室进行萃取实验用到的两种玻璃仪器是___________ ;向有机层中加入反萃取剂___________ (填化学式)可将Cu2+反萃取至水层。
(6)已知Li2CO3溶解度随着温度变化曲线如图。加入Na2CO3溶液后应进行的操作是___________ 。


查阅资料:LiCoO2具有很强的氧化性
(1)LiCoO2中,Co的化合价为
(2)写出“碱浸泡”发生反应的离子方程式:
(3)向“残渣”中加入稀硫酸和H2O2,放出大量气泡,写出LiCoO2与H2O2反应的化学方程式:
(4)若废旧的锂电池拆解后先使用酸溶解,最终也可以得到Al(OH)3、CoSO4、Li2CO3。在酸浸中若Al3+浓度为0.1mol·L-1,则常温时pH>
 =2.35)。
=2.35)。(5)RH萃取Cu2+的原理可表示为:Cu2++2HR
 CuR2+2H+。实验室进行萃取实验用到的两种玻璃仪器是
CuR2+2H+。实验室进行萃取实验用到的两种玻璃仪器是(6)已知Li2CO3溶解度随着温度变化曲线如图。加入Na2CO3溶液后应进行的操作是

您最近一年使用:0次
名校
解题方法
7 . 氧化钪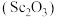 可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。从钛铁矿(主要成分为
可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。从钛铁矿(主要成分为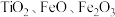 ,还含有
,还含有 等元素)中提取
等元素)中提取 的流程如下图。
的流程如下图。
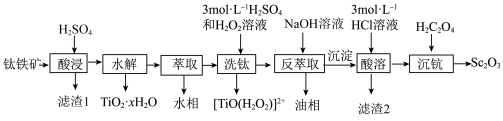
已知:
①当离子浓度减小至 时可认为沉淀完全。
时可认为沉淀完全。
②室温下 完全沉淀的
完全沉淀的 为1.05。
为1.05。
③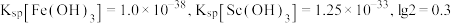 。
。
回答下列问题:
(1)“酸浸”后 元素转化为
元素转化为 ,其水解反应的离子方程式是
,其水解反应的离子方程式是_______ 。
(2) 既有氧化性又有还原性,还有弱酸性,请写出它的电离方程式
既有氧化性又有还原性,还有弱酸性,请写出它的电离方程式_______ 。
(3)萃取剂萃取 的反应原理为阳离子交换:
的反应原理为阳离子交换: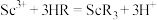 (
( 代表萃取剂)。在“反萃取”中反应生成含
代表萃取剂)。在“反萃取”中反应生成含 化合物的化学方程式是
化合物的化学方程式是_______ 。
(4)“酸溶”后滤液中存在的金属阳离子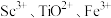 浓度均小于
浓度均小于 ,再用氨水调节溶液
,再用氨水调节溶液 使
使 、
、 沉淀完全而
沉淀完全而 不沉淀,则调
不沉淀,则调 应控制的范围是
应控制的范围是_______ 。
(5)由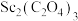 在空气中煅烧生成
在空气中煅烧生成 的化学反应方程式
的化学反应方程式_______ 。
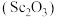 可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。从钛铁矿(主要成分为
可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。从钛铁矿(主要成分为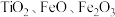 ,还含有
,还含有 等元素)中提取
等元素)中提取 的流程如下图。
的流程如下图。
已知:
①当离子浓度减小至
 时可认为沉淀完全。
时可认为沉淀完全。②室温下
 完全沉淀的
完全沉淀的 为1.05。
为1.05。③
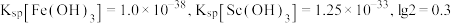 。
。回答下列问题:
(1)“酸浸”后
 元素转化为
元素转化为 ,其水解反应的离子方程式是
,其水解反应的离子方程式是(2)
 既有氧化性又有还原性,还有弱酸性,请写出它的电离方程式
既有氧化性又有还原性,还有弱酸性,请写出它的电离方程式(3)萃取剂萃取
 的反应原理为阳离子交换:
的反应原理为阳离子交换: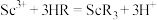 (
( 代表萃取剂)。在“反萃取”中反应生成含
代表萃取剂)。在“反萃取”中反应生成含 化合物的化学方程式是
化合物的化学方程式是(4)“酸溶”后滤液中存在的金属阳离子
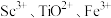 浓度均小于
浓度均小于 ,再用氨水调节溶液
,再用氨水调节溶液 使
使 、
、 沉淀完全而
沉淀完全而 不沉淀,则调
不沉淀,则调 应控制的范围是
应控制的范围是(5)由
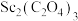 在空气中煅烧生成
在空气中煅烧生成 的化学反应方程式
的化学反应方程式
您最近一年使用:0次
2023-12-19更新
|
300次组卷
|
2卷引用:湖南省雅礼教育集团2023-2024学年高二上学期期中考试化学试题
名校
8 . 化学与生活密切相关。下列说法正确的是
| A.高锰酸钾溶液、“84”消毒液、酒精均具有强氧化性,可用于杀菌消毒 |
B.纯碱溶液可去油污,是由于 水解使溶液显碱性 水解使溶液显碱性 |
C.石灰石可减少煤燃烧的 排放,是由于石灰石可将 排放,是由于石灰石可将 转化为 转化为 |
D.用FeS作沉淀剂,可除去废水中的 和 和 |
您最近一年使用:0次
2023-12-26更新
|
204次组卷
|
2卷引用:湖南省常德市临澧县第一中学2023-2024学年高二下学期入学考试化学试题
9 . 三氯化六氨合钴(Ⅲ){[Co(NH3)6]Cl3}是合成其他含钴配合物的重要原料。工业上以水钻矿(主要成分为 Co2O3,还含有少量的 Fe2O3、Al2O3、MgO、CaO、SiO2)为原料制备三氯化六氨合钴晶体。

已知:①Co2O3具有很强的氧化性,其还原产物为Co(Ⅱ);碱性条件下,Co(Ⅱ)能被 O2氧化; 易溶于热水,难溶于冷水。
②25℃时相关物质的 Ksp如下表(当溶液中某离子浓度小于10-5mol/L 时,认为该离子沉淀完全):
下列说法错误的是

已知:①Co2O3具有很强的氧化性,其还原产物为Co(Ⅱ);碱性条件下,Co(Ⅱ)能被 O2氧化; 易溶于热水,难溶于冷水。
②25℃时相关物质的 Ksp如下表(当溶液中某离子浓度小于10-5mol/L 时,认为该离子沉淀完全):
| 物质 | Co(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 | Ca(OH)2 | MgF2 | CaF2 |
| Ksp | 1×10⁻13.8 | 1×10-16.3 | 1×10-38.6 | 1×10⁻32.3 | 1×10⁻11.2 | 1×10-7.8 | 1×10-10 | 5×10-11 |
A.“浸取”时主要反应的离子方程式为   |
| B.“氧化”时,是将Fe2+ 氧化为Fe3+,滤渣Ⅱ的成分是Fe(OH)3 |
| C.“除杂”时,CoF2可将Ca2+、Mg2+转化为沉淀过滤除去,若所得滤液中Mg2+刚好沉淀完全,则此时滤液中 c(Ca2+)=5×10-6mol/L |
D.“转化”时反应的离子方程式为  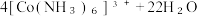 |
您最近一年使用:0次
名校
10 . 一种银铟矿主要成分为Au、Ag2S、CuS、ZnS、PbS、FeS、In2O3、Ga2O3等物质,从该矿获得稀有金属的工艺流程如图所示:

该工艺条件下,金属离子开始沉淀和完全沉淀的pH如表:
(1)“浸出”过程中金、银分别转化为AuCl 、AgCl
、AgCl 进入溶液,同时生成硫,写出Ag2S发生反应的离子方程式
进入溶液,同时生成硫,写出Ag2S发生反应的离子方程式____ 。
(2)高温水蒸气除铁利用了FeCl3易水解的性质,写出该反应的化学方程式____ 。
(3)“二次还原”得到的滤液中主要的阳离子有H+、Na+、Ca2+、Zn2+、Pb3+、In3+、____ 。
(4)“二次中和”得到的滤渣除少量Fe(OH)3外,主要成分还有____ (写化学式)。
(5)“分铅锌”步骤中,维持H2S饱和水溶液的浓度为0.1mol·L-1,为使Zn2+沉淀完全,需控制溶液的pH不小于____ 已知:lg3≈0.48;Ksp(ZnS)=3.0×10-25,Ka1(H2S)=1.0×10-7,Ka2(H2S)=1.0×10-13]。
(6)已知:氧化还原反应可看成由两个半反应组成,每个半反应具有一定的电极电势(用“φ”表示),φ越大则该物质的氧化性越强,φ越低则该物质的还原性越强。浸出步骤中金反应的两个半反应如下:
HClO+H++2e-=C1-+H2O φ=1.49+ lg
lg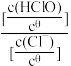
AuCl4-+3e-=4C1-+Au φ=0.994+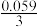 lg
lg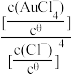
(φ与半反应式的系数无关,仅与浓度有关,cθ=1mol·L-1)
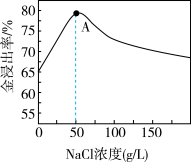
如图是Au的浸出率与NaCl溶液浓度的关系,请解释A点以后,金浸出率减小的原因是____ 。

该工艺条件下,金属离子开始沉淀和完全沉淀的pH如表:
| 金属离子 | Fe3+ | In3+ | Ga3+ | Cu2+ | Zn2+ | Pb2+ |
| 开始沉淀的pH | 2.2 | 2.1 | 2.6 | 4.6 | 6.24 | 7.1 |
| 完全沉淀(c=1.0×10-5mol·L-1)的pH | 3.2 | 3.4 | 4.3 | 6.6 | 8.24 | 9.1 |
(1)“浸出”过程中金、银分别转化为AuCl
 、AgCl
、AgCl 进入溶液,同时生成硫,写出Ag2S发生反应的离子方程式
进入溶液,同时生成硫,写出Ag2S发生反应的离子方程式(2)高温水蒸气除铁利用了FeCl3易水解的性质,写出该反应的化学方程式
(3)“二次还原”得到的滤液中主要的阳离子有H+、Na+、Ca2+、Zn2+、Pb3+、In3+、
(4)“二次中和”得到的滤渣除少量Fe(OH)3外,主要成分还有
(5)“分铅锌”步骤中,维持H2S饱和水溶液的浓度为0.1mol·L-1,为使Zn2+沉淀完全,需控制溶液的pH不小于
(6)已知:氧化还原反应可看成由两个半反应组成,每个半反应具有一定的电极电势(用“φ”表示),φ越大则该物质的氧化性越强,φ越低则该物质的还原性越强。浸出步骤中金反应的两个半反应如下:
HClO+H++2e-=C1-+H2O φ=1.49+
 lg
lg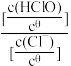
AuCl4-+3e-=4C1-+Au φ=0.994+
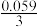 lg
lg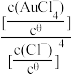
(φ与半反应式的系数无关,仅与浓度有关,cθ=1mol·L-1)
如图是Au的浸出率与NaCl溶液浓度的关系,请解释A点以后,金浸出率减小的原因是

您最近一年使用:0次
2022-04-27更新
|
715次组卷
|
5卷引用:湖南省永州市2022届高三高考第三次适应性考试化学试题
湖南省永州市2022届高三高考第三次适应性考试化学试题湖南省岳阳市一中2021-2022学年高三下学期第三次模拟考试试题江西省南昌市八一中学2022届高三下学期第三次模拟考试理科综合化学试题福建省厦门外国语学校2023届高三上学期期末检测化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(工业流程题)



