名校
1 . 菠菜营养丰富,素有“蔬菜之王”的美称。民间流传:菠菜豆腐同食,易得结石。某化学兴趣小组对“菠菜豆腐是否不能同食”等问题进行了探究。
【查阅资料】①菠菜含有丰富的铁、草酸盐、碳酸盐等,豆腐中含有丰富的蛋白质及钙盐。
②人体结石的主要成分:草酸钙( )
)
③醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐等。
【提出猜想】
(1) “菠菜豆腐不能同食”的原因可能是___________ 。
【探究一】菠菜中部分成分分析
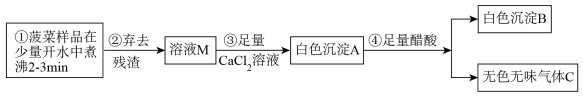
(2)步骤③中加入足量的 溶液的目的
溶液的目的___________ 。
(3)已知气体C能使澄清石灰水变浑浊,醋酸的化学式用HAc表示,写出步骤④的化学反应方程式___________ 。
(4)白色沉淀B的化学式为___________ ,由此可见菠菜豆腐不能同食。以下饮食观点正确的是___________ 。(填字母)
A.禁吃菠菜 B.高钙牛奶可与菠菜同食 C.菠菜烹饪时可用开水烫,可降低草酸盐含量
【探究二】某草酸钙晶体( )热分解研究。
)热分解研究。
按下图装置将草酸钙晶体样品高温加热,使其完全分解,对所得气体产物进行探究(假设装置中各试剂均足量)

(5)①反应开始前通入氮气的目的是___________ 。
②装置B中硫酸铜粉未变蓝,说明产物中有___________ ,C、F中澄清石灰水均变浑浊,E中CuO变红,说明产物还有___________ 和___________ ,经检验A中残留固体为氧化物。
③对上述装置从环保角度提一个改进建议___________ 。
(6)某研究所利用SDT Q600热分析仪对草酸钙晶体( )进行热分解,获得相关数据,绘制成固体质量—分解温度的关系如图。
)进行热分解,获得相关数据,绘制成固体质量—分解温度的关系如图。

①800℃以上时,固体成分的化学式为___________ 。
②计算 中的x
中的x___________ 。
③残留固体为 时的温度范围
时的温度范围___________ ,写出固体质量由12.8g变为10.0g时的化学方程式___________ 。
【查阅资料】①菠菜含有丰富的铁、草酸盐、碳酸盐等,豆腐中含有丰富的蛋白质及钙盐。
②人体结石的主要成分:草酸钙(
 )
)③醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐等。
【提出猜想】
(1) “菠菜豆腐不能同食”的原因可能是
【探究一】菠菜中部分成分分析

(2)步骤③中加入足量的
 溶液的目的
溶液的目的(3)已知气体C能使澄清石灰水变浑浊,醋酸的化学式用HAc表示,写出步骤④的化学反应方程式
(4)白色沉淀B的化学式为
A.禁吃菠菜 B.高钙牛奶可与菠菜同食 C.菠菜烹饪时可用开水烫,可降低草酸盐含量
【探究二】某草酸钙晶体(
 )热分解研究。
)热分解研究。按下图装置将草酸钙晶体样品高温加热,使其完全分解,对所得气体产物进行探究(假设装置中各试剂均足量)

(5)①反应开始前通入氮气的目的是
②装置B中硫酸铜粉未变蓝,说明产物中有
③对上述装置从环保角度提一个改进建议
(6)某研究所利用SDT Q600热分析仪对草酸钙晶体(
 )进行热分解,获得相关数据,绘制成固体质量—分解温度的关系如图。
)进行热分解,获得相关数据,绘制成固体质量—分解温度的关系如图。
①800℃以上时,固体成分的化学式为
②计算
 中的x
中的x③残留固体为
 时的温度范围
时的温度范围
您最近一年使用:0次
2023-05-26更新
|
84次组卷
|
3卷引用:安徽师范大学附属中学2022-2023学年高一上学期自主招生考试化学试题
安徽师范大学附属中学2022-2023学年高一上学期自主招生考试化学试题(已下线)云南师范大学附属中学2023-2024学年高一上学期开学考试化学试题云南师范大学附属中学2023-2024学年高一上学期开学考试化学试题
名校
解题方法
2 . 某钴矿石的主要成分有CoO、 、MnO、
、MnO、 、MgO和
、MgO和 等。由该矿石粉制备
等。由该矿石粉制备 固体的方法如下(部分催化剂已略)。
固体的方法如下(部分催化剂已略)。
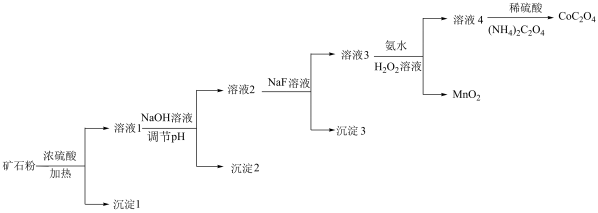
已知:金属离子沉淀的pH:
(1) 溶于浓硫酸,生成
溶于浓硫酸,生成 和一种可使带火星的木条复燃的气体,该气体是
和一种可使带火星的木条复燃的气体,该气体是___________ 。
(2)向溶液1中加入NaOH溶液将pH调至3,目的是___________ 。
(3)向溶液2中加入NaF溶液,去除的离子是___________ 。
(4)向溶液3中加入氨水和过氧化氢溶液,将 转化为
转化为 。补充完整下列离子方程式:
。补充完整下列离子方程式:_______
___________ +___________
+___________ ___________
___________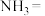 ___________
___________ ___________
___________
(5)溶液4中,若将1 mol 全部转化为
全部转化为 沉淀,需要消耗
沉淀,需要消耗
___________ mol。
(6)关于上述流程,下列说法正确的是___________ (填序号)。
a.若矿石粉中存在少量FeO,经上述流程也可制得纯度相同的
b.向溶液3中加入氨水,作用仅是调节溶液的pH
c.流程中,仅通过调节溶液的pH无法将金属元素完全分离
 、MnO、
、MnO、 、MgO和
、MgO和 等。由该矿石粉制备
等。由该矿石粉制备 固体的方法如下(部分催化剂已略)。
固体的方法如下(部分催化剂已略)。
已知:金属离子沉淀的pH:
 |  |  |  |  | |
| 开始沉淀时 | 1.5 | 6.3 | 8.9 | 8.2 | 7.4 |
| 完全沉淀时 | 2.8 | 8.3 | 10.9 | 10.2 | 9.4 |
 溶于浓硫酸,生成
溶于浓硫酸,生成 和一种可使带火星的木条复燃的气体,该气体是
和一种可使带火星的木条复燃的气体,该气体是(2)向溶液1中加入NaOH溶液将pH调至3,目的是
(3)向溶液2中加入NaF溶液,去除的离子是
(4)向溶液3中加入氨水和过氧化氢溶液,将
 转化为
转化为 。补充完整下列离子方程式:
。补充完整下列离子方程式:___________
 +___________
+___________ ___________
___________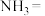 ___________
___________ ___________
___________(5)溶液4中,若将1 mol
 全部转化为
全部转化为 沉淀,需要消耗
沉淀,需要消耗
(6)关于上述流程,下列说法正确的是
a.若矿石粉中存在少量FeO,经上述流程也可制得纯度相同的

b.向溶液3中加入氨水,作用仅是调节溶液的pH
c.流程中,仅通过调节溶液的pH无法将金属元素完全分离
您最近一年使用:0次
2023-10-15更新
|
174次组卷
|
7卷引用:北京一零一中2021-2022学年高一下学期期末考试(等级考)化学试题
北京一零一中2021-2022学年高一下学期期末考试(等级考)化学试题北京市西城区2021届高三上学期期末考试化学试题(已下线)大题01 化学工艺流程题(一)-【考前抓大题】备战2021年高考化学(全国通用)(已下线)北京市第四中学2021-2022学年高三上学期期中考试化学试题北京市首都师范大学附属中学2023-2024学年高三上学期10月月考化学试题北京市清华大学附属中学2023-2024学年高三上学期10月统练(四)化学试题北京市顺义区第一中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
3 . 磷酸锌常用作氯化橡胶合成高分子材料的阻燃剂。工业上利用烧渣灰(主要含ZnO,还含少量FeO、Al2O3、CuO及SiO2)为原料制取磷酸锌的工艺流程如图所示:
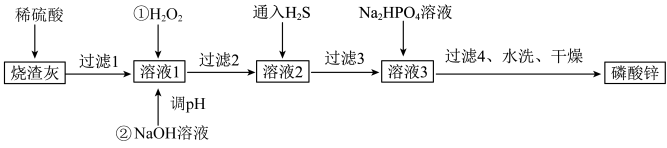
已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶液1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
(1)烧渣灰加入稀硫酸时,请写出ZnO与稀硫酸反应的离子方程式___________
(2)加入H2O2的作用___________
(3)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是___________ 。
(4)加入Na2HPO4溶液发生反应的离子方程式为___________ 。
(5)洗涤磷酸锌沉淀时应选用___________ (填“冷水”或“热水”),确认磷酸锌洗涤干净的操作是___________ 。
(6)通入H2S是为了除铜离子,25°C时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1 mol·L-1,此时溶液中c(Cu2+)=6.3×10-15mol·L-1,则CuS的溶度积Ksp=___________ (已知:25°C时,H2S的电离平衡常数Ka1=1×10-7 mol∙L-1,Ka2=1×10-15 mol∙L-1)。

已知:①[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶液1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.0 | 2.2 | 5.4 | 6.5 |
| 完全沉淀的pH | 5.0 | 3.6 | 6.7 | 8.5 |
(1)烧渣灰加入稀硫酸时,请写出ZnO与稀硫酸反应的离子方程式
(2)加入H2O2的作用
(3)经过滤2得到滤渣的主要成分是Fe(OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是
(4)加入Na2HPO4溶液发生反应的离子方程式为
(5)洗涤磷酸锌沉淀时应选用
(6)通入H2S是为了除铜离子,25°C时,当通入H2S达到饱和时测得溶液的pH=1,c(H2S)=0.1 mol·L-1,此时溶液中c(Cu2+)=6.3×10-15mol·L-1,则CuS的溶度积Ksp=
您最近一年使用:0次
2023-03-27更新
|
478次组卷
|
6卷引用:江西省丰城中学2022-2023学年高一下学期4月期中考试化学试题
名校
4 . 化学与生活、生产密切相关。下列说法错误的是
| A.空气中的水蒸气被冷凝成饮用水的过程是放热反应 |
B.用 可除去工业废水中的 可除去工业废水中的 等重金属离子 等重金属离子 |
| C.研发新型催化剂,使工业合成氨在温和条件下发生,可降低能耗 |
| D.回收利用废旧的铅酸蓄电池,既可以减少环境污染,又可以节约资源 |
您最近一年使用:0次
2022-10-23更新
|
264次组卷
|
3卷引用:四川省泸州市泸县第五中学2022-2023学年高一上学期期末考试化学试题
解题方法
5 . 下列实验操作、现象及结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将某气态混合烃通过酸性 溶液 溶液 | 溶液褪为无色 | 混合烃中含不饱和烃 |
| B | 向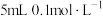 的KI溶液中滴加几滴 的KI溶液中滴加几滴 的 的 溶液,将所得溶液分成两份,分别滴加几滴 溶液,将所得溶液分成两份,分别滴加几滴 溶液和淀粉溶液 溶液和淀粉溶液 | 前者有黄色沉淀生成,后者溶液变蓝 |  与KI的反应为可逆反应 与KI的反应为可逆反应 |
| C | 将金属M和金属N用导线相连捕入同一溶液中 | M逐渐溶解,N上有气泡产生 | 金属M比金属N活泼 |
| D | 将淀粉和稀硫酸混合加热一段时间后,再加入新制的 ,加热 ,加热 | 产生砖红色沉淀 | 淀粉在稀硫酸、加热条件下水解为葡萄糖 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 化学无处不在,下列与化学知识有关的说法不正确的是
| A.可用三氯化铝对自来水进行杀菌消毒 |
B.处理锅炉水垢中的 ,可先用饱和 ,可先用饱和 溶液浸泡,后加盐酸除去 溶液浸泡,后加盐酸除去 |
C.实验室盛放 溶液的试剂瓶不能用磨口玻璃塞 溶液的试剂瓶不能用磨口玻璃塞 |
| D.用氯化铵浓溶液除去铁器表面的铁锈 |
您最近一年使用:0次
2023-01-11更新
|
104次组卷
|
2卷引用:山西省朔州市怀仁县阳高一中2023-2024学年高二上学期11月化学试卷
7 . ZnO是一种常用的化学添加剂,广泛应用于塑料、合成橡胶的化工生产中。一种以工业含锌废渣(主要成分为ZnO,还含有 、
、 、
、 及
及 等)制取氧化锌的工艺流程如图所示:
等)制取氧化锌的工艺流程如图所示:
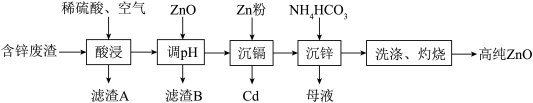
已知:相关金属离子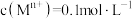 生成氢氧化物沉淀的pH如表所示:
生成氢氧化物沉淀的pH如表所示:
回答下列问题:
(1)“酸浸”时为了提高浸取速率,可以采取的措施是_______ (任写一种);该步骤中通入过量空气的作用是_______ 。
(2)滤渣B的主要成分为_______ ;“调pH”步骤时,应调节pH的范围是_______ ;若溶液碱性过强,可能导致的后果是_______ 。
(3)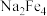 一种重要的净水剂,其基本原理是制得氢氧化铁,再将氢氧化铁与NaClO、烧碱在40℃反应,即可制备
一种重要的净水剂,其基本原理是制得氢氧化铁,再将氢氧化铁与NaClO、烧碱在40℃反应,即可制备 ,其中NaClO被还原成NaCl,请写出此法制备
,其中NaClO被还原成NaCl,请写出此法制备 的化学方程式:
的化学方程式:_______ 。
(4) 所含化学键的情况是
所含化学键的情况是_______ (填序号)。
①只含离子键 ②只含共价键 ③既有离子键,又有共价键
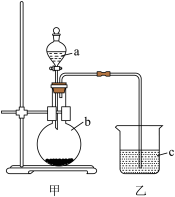
(5)Na、N、O三种元素形成的简单离子,半径由大到小的顺序是_______ (离子符号)。利用下图装置可比较C、N两元素的非金属性,b中发生反应的化学方程式为_______ 。
(6)碲( )的某化合物是常用的VCR光盘记录材料之一,可在激光照射下记录、储存信号。已知碲与O元素同主族,则碲及其化合物可能具有的性质为_______(填标号)。
)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下记录、储存信号。已知碲与O元素同主族,则碲及其化合物可能具有的性质为_______(填标号)。
 、
、 、
、 及
及 等)制取氧化锌的工艺流程如图所示:
等)制取氧化锌的工艺流程如图所示:
已知:相关金属离子
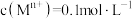 生成氢氧化物沉淀的pH如表所示:
生成氢氧化物沉淀的pH如表所示: |  |  |  |  | |
| 开始沉淀 | 6.5 | 2.7 | 3.4 | 6.5 | 7.4 |
| 沉淀完全 | 9.7 | 3.7 | 4.7 | 8.5 | 9.4 |
回答下列问题:
(1)“酸浸”时为了提高浸取速率,可以采取的措施是
(2)滤渣B的主要成分为
(3)
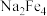 一种重要的净水剂,其基本原理是制得氢氧化铁,再将氢氧化铁与NaClO、烧碱在40℃反应,即可制备
一种重要的净水剂,其基本原理是制得氢氧化铁,再将氢氧化铁与NaClO、烧碱在40℃反应,即可制备 ,其中NaClO被还原成NaCl,请写出此法制备
,其中NaClO被还原成NaCl,请写出此法制备 的化学方程式:
的化学方程式:(4)
 所含化学键的情况是
所含化学键的情况是①只含离子键 ②只含共价键 ③既有离子键,又有共价键
(5)Na、N、O三种元素形成的简单离子,半径由大到小的顺序是

(6)碲(
 )的某化合物是常用的VCR光盘记录材料之一,可在激光照射下记录、储存信号。已知碲与O元素同主族,则碲及其化合物可能具有的性质为_______(填标号)。
)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下记录、储存信号。已知碲与O元素同主族,则碲及其化合物可能具有的性质为_______(填标号)。| A.单质碲在常温下是固体 | B. 比 比 稳定 稳定 |
C.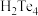 的酸性比 的酸性比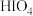 弱 弱 | D. 通入 通入 溶液中不发生反应 溶液中不发生反应 |
您最近一年使用:0次
8 . 明矾[ ]在造纸等方面应用广泛。工业上以废易拉罐(主要成分为Al和Fe)为原料制备明矾的工艺流程如图:
]在造纸等方面应用广泛。工业上以废易拉罐(主要成分为Al和Fe)为原料制备明矾的工艺流程如图:
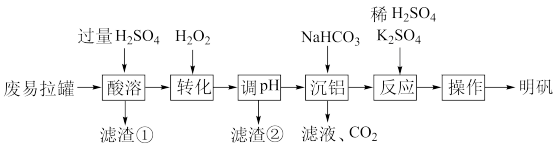
已知:不同温度 的溶解度:
的溶解度:
(1)“酸溶”中溶液中主要的金属离子有______ 、 、
、 。
。
(2)“转化”中 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为______ 。
(3)“调pH”约为3.7,滤渣②的主要成分是 ,“调pH”的目的是
,“调pH”的目的是______ 。
(4)“沉铝”中加入 目的是将
目的是将 转化为
转化为 ,补全该反应的离子方程式
,补全该反应的离子方程式______ 。
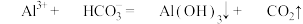
(5)“操作”包括______ 、______ 、过滤、洗涤、干燥可得到明矾晶体。
(6)某工厂用 kg废易拉罐(含Al 5.4%)制备
kg废易拉罐(含Al 5.4%)制备 (相对分子质量为474),最终得到产品
(相对分子质量为474),最终得到产品 kg,产率为
kg,产率为______ (列出计算式,不需运算)
 ]在造纸等方面应用广泛。工业上以废易拉罐(主要成分为Al和Fe)为原料制备明矾的工艺流程如图:
]在造纸等方面应用广泛。工业上以废易拉罐(主要成分为Al和Fe)为原料制备明矾的工艺流程如图:
已知:不同温度
 的溶解度:
的溶解度:温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
| 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
 、
、 。
。(2)“转化”中
 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为(3)“调pH”约为3.7,滤渣②的主要成分是
 ,“调pH”的目的是
,“调pH”的目的是(4)“沉铝”中加入
 目的是将
目的是将 转化为
转化为 ,补全该反应的离子方程式
,补全该反应的离子方程式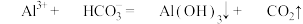
(5)“操作”包括
(6)某工厂用
 kg废易拉罐(含Al 5.4%)制备
kg废易拉罐(含Al 5.4%)制备 (相对分子质量为474),最终得到产品
(相对分子质量为474),最终得到产品 kg,产率为
kg,产率为
您最近一年使用:0次
名校
9 . 《本草备要》记载了化合物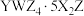 具有治喉痹、咳逆、敛疮毒等功效。W、X、Y、Z是元素周期表中前四周期元素,其中X、Z、W为短周期元素,原子序数依次增加,Y、X最外层电子数相同且质子数均为奇数,W、Z位于同一主族,Z的成对电子数与未成对电子数之比为3∶1,
具有治喉痹、咳逆、敛疮毒等功效。W、X、Y、Z是元素周期表中前四周期元素,其中X、Z、W为短周期元素,原子序数依次增加,Y、X最外层电子数相同且质子数均为奇数,W、Z位于同一主族,Z的成对电子数与未成对电子数之比为3∶1, 和生命活动密切相关。
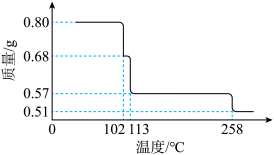
和生命活动密切相关。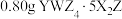 热重曲线如图所示。下列说法正确的是。
热重曲线如图所示。下列说法正确的是。
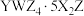 具有治喉痹、咳逆、敛疮毒等功效。W、X、Y、Z是元素周期表中前四周期元素,其中X、Z、W为短周期元素,原子序数依次增加,Y、X最外层电子数相同且质子数均为奇数,W、Z位于同一主族,Z的成对电子数与未成对电子数之比为3∶1,
具有治喉痹、咳逆、敛疮毒等功效。W、X、Y、Z是元素周期表中前四周期元素,其中X、Z、W为短周期元素,原子序数依次增加,Y、X最外层电子数相同且质子数均为奇数,W、Z位于同一主族,Z的成对电子数与未成对电子数之比为3∶1, 和生命活动密切相关。
和生命活动密切相关。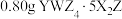 热重曲线如图所示。下列说法正确的是。
热重曲线如图所示。下列说法正确的是。
| A.W、Y、Z、X的单质熔点最高的是W |
B.210℃时固体物质的化学式为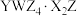 |
C.将258℃的固体产物用稀硫酸溶解,经浓缩、冷却,会析出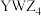 |
D. 的 的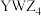 溶液中通入过量的 溶液中通入过量的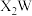 ,会产生沉淀 ,会产生沉淀 |
您最近一年使用:0次
2022-12-16更新
|
1013次组卷
|
4卷引用:山东省新泰市第一中学2022-2023学年高一下学期第一次阶段性考试检测化学试题
山东省新泰市第一中学2022-2023学年高一下学期第一次阶段性考试检测化学试题湖南省九校联盟2023届高三上学期第一次联考化学试题(已下线)专题07 元素周期律与元素周期表(测)-2023年高考化学二轮复习讲练测(新高考专用)湖南省九校联盟2023届高三上学期第一次联考化学试题
名校
解题方法
10 . 下列离子方程式书写正确的是
A.高锰酸钾与浓盐酸制氯气的反应: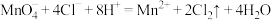 |
B. 悬浊液中滴入 悬浊液中滴入 溶液: 溶液: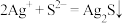 |
C.向 溶液中滴加 溶液中滴加 溶液: 溶液: |
D.向稀 中滴加 中滴加 溶液: 溶液: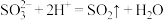 |
您最近一年使用:0次



