名校
1 . 软锰矿浆(主要成分 )可吸收烟气中的
)可吸收烟气中的 ,同时可制备
,同时可制备 ,工艺流程如下:
,工艺流程如下: 后的软锰矿浆中含有
后的软锰矿浆中含有 等阳离子:
等阳离子:
②金属离子沉淀的 如下表
如下表
(1)脱硫的产物是 ,软锰矿中
,软锰矿中 所起的作用是
所起的作用是___________ 。
(2)过程1向浆液中通入 的目的是
的目的是___________ 。
(3)滤渣1的成分是___________ ,过程2中发生反应的离子方程式为___________ 。
(4)写出制备 时发生反应的离子方程式
时发生反应的离子方程式___________ 。
(5)取 碳酸锰样品,加适量硫酸加热溶解后,用
碳酸锰样品,加适量硫酸加热溶解后,用 的
的 溶液测定,至反应完全时,消耗
溶液测定,至反应完全时,消耗 溶液的体积为
溶液的体积为 。 (已知:反应产物为
。 (已知:反应产物为 ,杂质不参与反应)
,杂质不参与反应)
样品中 质量分数的计算式为
质量分数的计算式为___________  。
。
 )可吸收烟气中的
)可吸收烟气中的 ,同时可制备
,同时可制备 ,工艺流程如下:
,工艺流程如下:
 后的软锰矿浆中含有
后的软锰矿浆中含有 等阳离子:
等阳离子:②金属离子沉淀的
 如下表
如下表| 金属离子 |  |  |  |  |  |
开始沉淀的 | 8.1 | 6.3 | 1.5 | 3.4 | 6.2 |
沉淀完全的 | 10.1 | 8.3 | 2.8 | 4.7 | 8.2 |
(1)脱硫的产物是
 ,软锰矿中
,软锰矿中 所起的作用是
所起的作用是(2)过程1向浆液中通入
 的目的是
的目的是(3)滤渣1的成分是
(4)写出制备
 时发生反应的离子方程式
时发生反应的离子方程式(5)取
 碳酸锰样品,加适量硫酸加热溶解后,用
碳酸锰样品,加适量硫酸加热溶解后,用 的
的 溶液测定,至反应完全时,消耗
溶液测定,至反应完全时,消耗 溶液的体积为
溶液的体积为 。 (已知:反应产物为
。 (已知:反应产物为 ,杂质不参与反应)
,杂质不参与反应)样品中
 质量分数的计算式为
质量分数的计算式为 。
。
您最近一年使用:0次
名校
2 . 软锰矿的主要成分MnO2,还含有Fe2O3、MgO、Al2O3、CaO、SiO2等杂质,工业上用软锰矿制取MnSO4•H2O的流程如图
部分金属阳离子完全沉淀时的pH如下表
(1)浸出渣的主要成分为___________ (填化学式)。
(2)Mn的价层电子排布式为_________________ 。
(3)“浸出”过程中MnO2转化为Mn2+的离子方程式为_________________ 。
(4)第1步除杂加双氧水的目的是_________________ 。
(5)调pH至5~6所加的试剂,可选择__________ 。(填字母)。
a.CaO b.MgO c.Al2O3 d.氨水
(6)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子方程式:_______________ ,该反应的平衡常数为___________ (结果保留一位小数)。

部分金属阳离子完全沉淀时的pH如下表
| 金属阳离子 | Fe3+ | Al3+ | Mn2+ | Mg2+ |
| 完全沉淀时的pH | 3.2 | 5.2 | 10.4 | 12.4 |
(1)浸出渣的主要成分为
(2)Mn的价层电子排布式为
(3)“浸出”过程中MnO2转化为Mn2+的离子方程式为
(4)第1步除杂加双氧水的目的是
(5)调pH至5~6所加的试剂,可选择
a.CaO b.MgO c.Al2O3 d.氨水
(6)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子方程式:
您最近一年使用:0次
3 . 实验室由硫铁矿烧渣(主要成分为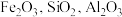 )制备软磁性材料
)制备软磁性材料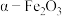 。主要转化流程如图:
。主要转化流程如图:

(1)制绿矾。烧渣到绿矾的工艺中涉及“酸浸”“还原”“除杂”“结晶”等实验流程。
①酸浸。
②还原。向“酸浸”后的溶液中加入过量铁粉,使 完全转化为
完全转化为 。该过程除生成
。该过程除生成 外,还会生成
外,还会生成_______ (填化学式);检验 是否还原完全的实验操作是
是否还原完全的实验操作是_______ 。
③除杂。向“还原”后滤液中加入 溶液,调节
溶液,调节 为
为_______ ,使 除去完全。[已知:
除去完全。[已知: 时
时 为沉淀完全,
为沉淀完全, 时
时 开始沉淀。]
开始沉淀。]
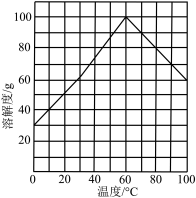
④结晶。结合题图所示的绿矾溶解度曲线,补充完整获得 晶体的实验操作。向
晶体的实验操作。向 溶液中再加入稀硫酸酸化,
溶液中再加入稀硫酸酸化,_______ ,过滤,少量冰水洗涤,低温干燥,得到 晶体。
晶体。
(2)制 。将
。将 溶液与氨水
溶液与氨水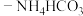 混合溶液中的一种加入三颈瓶中(装置见图),通过分液漏斗缓慢滴加另一种溶液,充分反应,过滤。
混合溶液中的一种加入三颈瓶中(装置见图),通过分液漏斗缓慢滴加另一种溶液,充分反应,过滤。
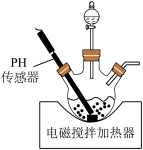
①分液漏斗中的溶液是_______ ;生成 的离子方程式为
的离子方程式为_______ 。
②生成的 沉淀需“洗涤完全”,检验方法是
沉淀需“洗涤完全”,检验方法是_______ 。
(3)制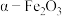 。将纯净的
。将纯净的 放入管式炉内煅烧
放入管式炉内煅烧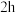 ,获得产品
,获得产品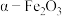 。图为其他条件相同时不同煅烧温度对产品中
。图为其他条件相同时不同煅烧温度对产品中 质量分数的影响,当煅烧温度高于
质量分数的影响,当煅烧温度高于 时,产品中
时,产品中 质量分数降低,铁元素质量分数升高,其可能原因是
质量分数降低,铁元素质量分数升高,其可能原因是_______ 。

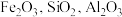 )制备软磁性材料
)制备软磁性材料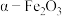 。主要转化流程如图:
。主要转化流程如图:
(1)制绿矾。烧渣到绿矾的工艺中涉及“酸浸”“还原”“除杂”“结晶”等实验流程。
①酸浸。
②还原。向“酸浸”后的溶液中加入过量铁粉,使
 完全转化为
完全转化为 。该过程除生成
。该过程除生成 外,还会生成
外,还会生成 是否还原完全的实验操作是
是否还原完全的实验操作是③除杂。向“还原”后滤液中加入
 溶液,调节
溶液,调节 为
为 除去完全。[已知:
除去完全。[已知: 时
时 为沉淀完全,
为沉淀完全, 时
时 开始沉淀。]
开始沉淀。]④结晶。结合题图所示的绿矾溶解度曲线,补充完整获得
 晶体的实验操作。向
晶体的实验操作。向 溶液中再加入稀硫酸酸化,
溶液中再加入稀硫酸酸化, 晶体。
晶体。
(2)制
 。将
。将 溶液与氨水
溶液与氨水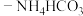 混合溶液中的一种加入三颈瓶中(装置见图),通过分液漏斗缓慢滴加另一种溶液,充分反应,过滤。
混合溶液中的一种加入三颈瓶中(装置见图),通过分液漏斗缓慢滴加另一种溶液,充分反应,过滤。
①分液漏斗中的溶液是
 的离子方程式为
的离子方程式为②生成的
 沉淀需“洗涤完全”,检验方法是
沉淀需“洗涤完全”,检验方法是(3)制
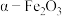 。将纯净的
。将纯净的 放入管式炉内煅烧
放入管式炉内煅烧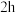 ,获得产品
,获得产品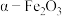 。图为其他条件相同时不同煅烧温度对产品中
。图为其他条件相同时不同煅烧温度对产品中 质量分数的影响,当煅烧温度高于
质量分数的影响,当煅烧温度高于 时,产品中
时,产品中 质量分数降低,铁元素质量分数升高,其可能原因是
质量分数降低,铁元素质量分数升高,其可能原因是
您最近一年使用:0次
4 . 某“变废为宝”学生探究小组设计如下工艺流程,对废锌(含铁和铜的氧化物杂质)和除氯后的卤水(含碘离子)联合应用,最终制得胆矾、 、碘等。
、碘等。
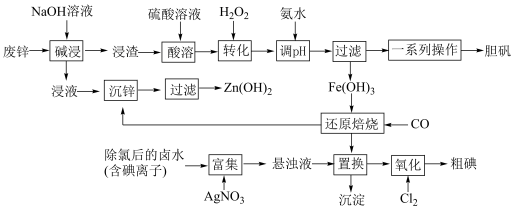
已知:①锌元素与铝元素的性质类似,例如氧化锌也能溶于强碱{生成 }。
}。
②本工艺条件下,相关金属离子形成氢氧化物沉淀的pH范围如下:
③还原性: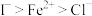
回答下列问题:
(1)“碱浸”中发生反应的化学方程式为____________________ 。
(2)“转化”中,加入足量H2O2的目的是____________________ 。
(3)“调pH”时需控制该溶液的pH范围为______ 之间。“调pH”之后,需要加热煮沸10 min,冷却后再“过滤”。煮沸10 min的作用是____________________ 。
(4)“还原焙烧”的气体产物可循环利用到“沉锌”中。若该气体不足,“沉锌”中发生反应的离子方程式为____________________ 。
(5)“氧化”过程中若反应物用量比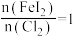 时,氧化产物为
时,氧化产物为______ (填化学式)
 、碘等。
、碘等。
已知:①锌元素与铝元素的性质类似,例如氧化锌也能溶于强碱{生成
 }。
}。②本工艺条件下,相关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 |
|
|
|
|
开始沉淀的pH | 6.2 | 6.3 | 1.5 | 4.7 |
沉淀完全的pH | 8.2 | 8.3 | 2.8 | 6.8 |
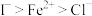
回答下列问题:
(1)“碱浸”中发生反应的化学方程式为
(2)“转化”中,加入足量H2O2的目的是
(3)“调pH”时需控制该溶液的pH范围为
(4)“还原焙烧”的气体产物可循环利用到“沉锌”中。若该气体不足,“沉锌”中发生反应的离子方程式为
(5)“氧化”过程中若反应物用量比
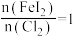 时,氧化产物为
时,氧化产物为
您最近一年使用:0次
名校
解题方法
5 . 下列实验操作、现象和解释与结论有错误的是
| 选项 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向硅酸钠溶液中通入适量 | 溶液变浑浊 | 酸性: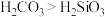 |
| B | 用 计测同温同浓度的 计测同温同浓度的 和 和 溶液的 溶液的 | 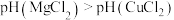 | 金属性: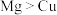 |
| C | 向足量含有 的 的 溶液中滴加2滴氯水 溶液中滴加2滴氯水 | 溶液变血红色 | 还原性: |
| D | 向NaCl和KI混合溶液中滴加 溶液 溶液 | 先产生黄色沉淀,后产生白色沉淀 | 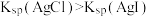 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 25℃时,某一元弱酸HX的电离平衡常数Ka=1.0×10-5,则:
(1)0.1mol/L的HX溶液中HX的电离度约为_______ 。
(2)若1L0.1mol/L的HX溶液中加入1mL0.1mol/LAgNO3溶液生成了AgX沉淀,则该温度下Ksp(AgX)≤______ (假设混合后溶液总体积仍为1L,且忽略因稀释导致的HX溶液电离平衡的移动);
(3)0.1mol/L的NaX溶液的pH值约为_____ ,该溶液中水电离的c(OH-)为_______ mol/L;
(4)若用0.1mol/L的NaOH标准溶液来滴定锥形瓶中未知浓度的HX溶液应选择的指示剂为_______ (选填:甲基橙、酚酞或紫色石蕊),若滴入的NaOH溶液恰好中和了一半,那么此时溶液中存在微粒的浓度由大到小的次序是_______ 。
(1)0.1mol/L的HX溶液中HX的电离度约为
(2)若1L0.1mol/L的HX溶液中加入1mL0.1mol/LAgNO3溶液生成了AgX沉淀,则该温度下Ksp(AgX)≤
(3)0.1mol/L的NaX溶液的pH值约为
(4)若用0.1mol/L的NaOH标准溶液来滴定锥形瓶中未知浓度的HX溶液应选择的指示剂为
您最近一年使用:0次
解题方法
7 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
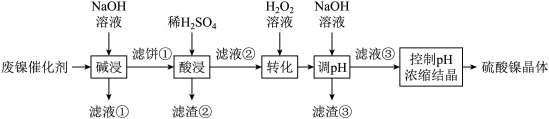
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是___________ 和洗去油脂。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式___________ 。
(2)“滤液②”中含有的金属离子是Ni2+和___________ 。
(3)“转化”中可替代H2O2的物质是___________ 。若工艺流程改为先“调pH”后“转化”,即
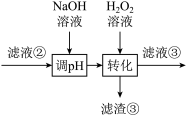
“滤液③”中可能含有的杂质离子为___________ 。
(4)硫酸镍溶液在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH.写出该反应的离子方程式___________ 。
(5)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是___________ 。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时的pH 沉淀完全时的pH | 7.2 8.7 | 3.7 4.7 | 2.2 3.2 | 7.5 9.0 |
(1)“碱浸”中NaOH的两个作用分别是
(2)“滤液②”中含有的金属离子是Ni2+和
(3)“转化”中可替代H2O2的物质是

“滤液③”中可能含有的杂质离子为
(4)硫酸镍溶液在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH.写出该反应的离子方程式
(5)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近一年使用:0次
8 . 利用某金属废屑(含Cu、Al、Fe及其少量氧化物)制备胆矾的工艺流程如图所示.
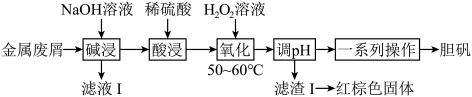
回答下列问题:
(1)“碱浸”工序Al发生反应的离子方程式为____________ .
(2)相关离子在溶液中的去除率随pH的变化如图所示.
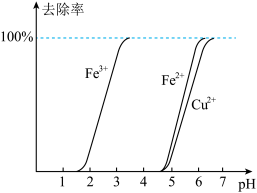
①“氧化”工序中 的作用是
的作用是__________ 、______________ (用离子方程式表示);“氧化”工序采取的加热方式为____________ ,温度不宜过高的原因是___________ .
②“调pH”时,应控制溶液pH的适宜范围为__________ (填标号).
A.2.0~3.0 B.3.0~4.0 C.4.0~5.0
(3)红棕色固体的用途有___________ (任写一种).“一系列操作”中包含__________ 、__________ 、过滤、洗涤、干燥.

回答下列问题:
(1)“碱浸”工序Al发生反应的离子方程式为
(2)相关离子在溶液中的去除率随pH的变化如图所示.

①“氧化”工序中
 的作用是
的作用是②“调pH”时,应控制溶液pH的适宜范围为
A.2.0~3.0 B.3.0~4.0 C.4.0~5.0
(3)红棕色固体的用途有
您最近一年使用:0次
9 . 处理某铜冶金污水(含 、
、 、
、 、
、 )的部分流程如下:
)的部分流程如下:
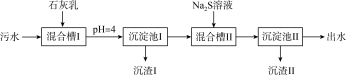
已知:①常温下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
②常温下, ,
, 。
。
下列说法错误的是
 、
、 、
、 、
、 )的部分流程如下:
)的部分流程如下:
已知:①常温下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
物质 |
|
|
开始沉淀时的pH | 1.8 | 3.5 |
沉淀完全时 | 3 | 4.6 |
 ,
, 。
。下列说法错误的是
A. |
B. 溶液呈碱性,其主要原因是 溶液呈碱性,其主要原因是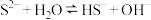 |
C.“沉淀池Ⅱ”中,当 和 和 完全沉淀时,溶液中 完全沉淀时,溶液中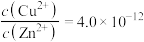 |
| D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水 |
您最近一年使用:0次
解题方法
10 . 用如图所示实验装置进行相应的实验,不能达到实验目的的是
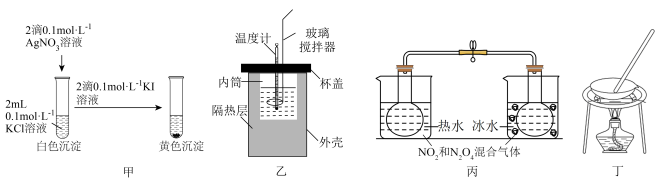

A.图甲:证明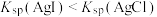 |
| B.图乙:测量盐酸和氢氧化钠反应的反应热 |
| C.图丙:验证温度对化学平衡的影响 |
D.图丁:由 固体制备无水氯化铁 固体制备无水氯化铁 |
您最近一年使用:0次



 的pH
的pH

