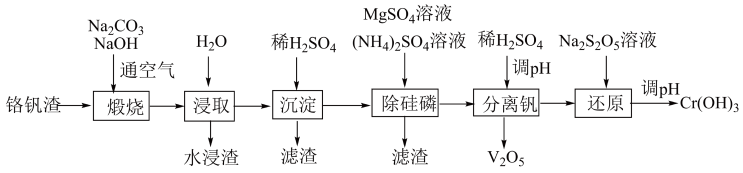
1 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:最高价铬酸根在酸性介质中以Cr2O 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为___________ (填化学式)。
(2)水浸渣中主要有SiO2和___________ (写化学式)。
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________ (写化学式)。
(4)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,还原Cr2O ,写出该反应的离子方程式为
,写出该反应的离子方程式为___________ 。
(5)已知25℃时Ksp[Cr(OH)3]=6.4×10-31,若除去废水中Cr3+,使其浓度小于6.4×10-7mol·L-1,此时溶液中的c(H+)<______ mol·L-1。
(6)已知:Cr(Ⅲ)的存在形态的物质的量分数随溶液pH的分布如图所示
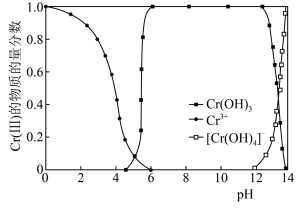
请补充完整由 溶液制得
溶液制得 的实验方案:取分离、提纯得到的
的实验方案:取分离、提纯得到的 溶液,
溶液,___________ ,低温烘干,得到高纯 晶体。[实验中
晶体。[实验中须使用 的试剂:2mol/LNaOH溶液、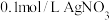 溶液、
溶液、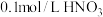 溶液、蒸馏水]
溶液、蒸馏水]

已知:最高价铬酸根在酸性介质中以Cr2O
 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(2)水浸渣中主要有SiO2和
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是
(4)“还原”步骤中加入焦亚硫酸钠(Na2S2O5)溶液,还原Cr2O
 ,写出该反应的离子方程式为
,写出该反应的离子方程式为(5)已知25℃时Ksp[Cr(OH)3]=6.4×10-31,若除去废水中Cr3+,使其浓度小于6.4×10-7mol·L-1,此时溶液中的c(H+)<
(6)已知:Cr(Ⅲ)的存在形态的物质的量分数随溶液pH的分布如图所示

请补充完整由
 溶液制得
溶液制得 的实验方案:取分离、提纯得到的
的实验方案:取分离、提纯得到的 溶液,
溶液, 晶体。[实验中
晶体。[实验中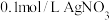 溶液、
溶液、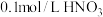 溶液、蒸馏水]
溶液、蒸馏水]
您最近一年使用:0次
2 .  是重要的化工原料,由软锰矿制备
是重要的化工原料,由软锰矿制备 的一种工艺流程如图:
的一种工艺流程如图:

资料:①软锰矿的主要成分为 ,主要杂质有
,主要杂质有 和
和
②金属离子沉淀的pH
③该工艺条件下, 与
与 反应。
反应。
(1)溶出
①溶出前,软锰矿需研磨。目的是_______ 。
②溶出时,Fe的氧化过程及得到 的主要途径如图所示:
的主要途径如图所示:

a.步骤Ⅱ是从软锰矿中溶出 的主要反应,反应的离子方程式是
的主要反应,反应的离子方程式是_______ 。
b.若 全部来自于反应
全部来自于反应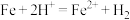 ,完全溶出
,完全溶出 所需Fe与
所需Fe与 的物质的量比值为2。而实际比值小于2,原因是
的物质的量比值为2。而实际比值小于2,原因是_______ 。
(2)纯化的目的是为了除去溶液中的杂质。已知:溶液pH越小, 的氧化性越强。纯化时先加入
的氧化性越强。纯化时先加入_______ ,后加入_______ (选填“氨水”、“ ”)调溶液pH
”)调溶液pH_______ ~_______ ,调pH到此范围的目的是_______ 。
(3)电解。 纯化液经电解得
纯化液经电解得 。生成
。生成 的电极反应式是
的电极反应式是_______ 。
(4)产品纯度测定。向0.45g产品中加入1.34g 和足量稀硫酸,加热至充分反应。再用0.1000mol·L
和足量稀硫酸,加热至充分反应。再用0.1000mol·L
 溶液滴定剩余
溶液滴定剩余 至终点,消耗
至终点,消耗 溶液的体积为20.00mL。
溶液的体积为20.00mL。
已知: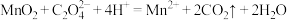 ,
,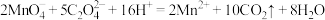 ,计算该产品的纯度。(写出计算过程)
,计算该产品的纯度。(写出计算过程)_______ 。
 是重要的化工原料,由软锰矿制备
是重要的化工原料,由软锰矿制备 的一种工艺流程如图:
的一种工艺流程如图:
资料:①软锰矿的主要成分为
 ,主要杂质有
,主要杂质有 和
和
②金属离子沉淀的pH
 |  |  |  | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
 与
与 反应。
反应。(1)溶出
①溶出前,软锰矿需研磨。目的是
②溶出时,Fe的氧化过程及得到
 的主要途径如图所示:
的主要途径如图所示:
a.步骤Ⅱ是从软锰矿中溶出
 的主要反应,反应的离子方程式是
的主要反应,反应的离子方程式是b.若
 全部来自于反应
全部来自于反应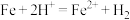 ,完全溶出
,完全溶出 所需Fe与
所需Fe与 的物质的量比值为2。而实际比值小于2,原因是
的物质的量比值为2。而实际比值小于2,原因是(2)纯化的目的是为了除去溶液中的杂质。已知:溶液pH越小,
 的氧化性越强。纯化时先加入
的氧化性越强。纯化时先加入 ”)调溶液pH
”)调溶液pH(3)电解。
 纯化液经电解得
纯化液经电解得 。生成
。生成 的电极反应式是
的电极反应式是(4)产品纯度测定。向0.45g产品中加入1.34g
 和足量稀硫酸,加热至充分反应。再用0.1000mol·L
和足量稀硫酸,加热至充分反应。再用0.1000mol·L
 溶液滴定剩余
溶液滴定剩余 至终点,消耗
至终点,消耗 溶液的体积为20.00mL。
溶液的体积为20.00mL。已知:
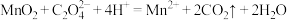 ,
,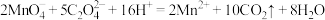 ,计算该产品的纯度。(写出计算过程)
,计算该产品的纯度。(写出计算过程)
您最近一年使用:0次
3 . 利用软锰矿(主要含 、
、 ,还含有少量
,还含有少量 等)制备电池材料
等)制备电池材料 的一种流程如下。
的一种流程如下。

(1)酸浸。
①写出酸浸过程中发生主要反应的离子方程式:_____ 。
②为提高锰元素浸出率可采取的措施有适当提高酸的浓度、_____ 等。(任填一种合理的措施)
③生成的硫附着在矿粉颗粒表面使上述反应受阻,加入 ,迅速分解产生的大量气体破除附着的硫。
,迅速分解产生的大量气体破除附着的硫。 迅速分解的原因是
迅速分解的原因是_____ 。
(2)除铁、铝。此条件下所得酸浸液中金属离子开始沉淀和完全沉淀时的pH如下表。
除铁、铝时需调节溶液的pH范围为_____ 。
(3)制备 。向
。向 溶液中加入氨水,产生含
溶液中加入氨水,产生含 和
和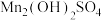 的沉淀,洗涤沉淀后加水混合并通入适量的
的沉淀,洗涤沉淀后加水混合并通入适量的 ,可得到
,可得到 ,过程中溶液的pH随时间的变化如图所示。请结合化学反应方程式分别解释其原因。
,过程中溶液的pH随时间的变化如图所示。请结合化学反应方程式分别解释其原因。
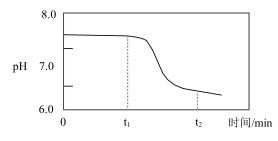
① 时段,溶液pH几乎不变:
时段,溶液pH几乎不变:_____ 。
② 时段,溶液pH明显降低:
时段,溶液pH明显降低:_____ 。
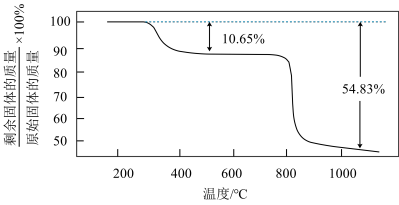
(4)在空气中加热分解 ,固体质量随温度变化如图所示。计算1100℃时的分解产物化学式为
,固体质量随温度变化如图所示。计算1100℃时的分解产物化学式为_____ (写出计算推理过程)。
 、
、 ,还含有少量
,还含有少量 等)制备电池材料
等)制备电池材料 的一种流程如下。
的一种流程如下。
(1)酸浸。
①写出酸浸过程中发生主要反应的离子方程式:
②为提高锰元素浸出率可采取的措施有适当提高酸的浓度、
③生成的硫附着在矿粉颗粒表面使上述反应受阻,加入
 ,迅速分解产生的大量气体破除附着的硫。
,迅速分解产生的大量气体破除附着的硫。 迅速分解的原因是
迅速分解的原因是(2)除铁、铝。此条件下所得酸浸液中金属离子开始沉淀和完全沉淀时的pH如下表。
 |  |  |  | |
| 开始沉淀 | 1.5 | 6.3 | 3.4 | 5.8 |
| 完全沉淀 | 2.8 | 8.3 | 4.7 | 7.8 |
(3)制备
 。向
。向 溶液中加入氨水,产生含
溶液中加入氨水,产生含 和
和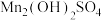 的沉淀,洗涤沉淀后加水混合并通入适量的
的沉淀,洗涤沉淀后加水混合并通入适量的 ,可得到
,可得到 ,过程中溶液的pH随时间的变化如图所示。请结合化学反应方程式分别解释其原因。
,过程中溶液的pH随时间的变化如图所示。请结合化学反应方程式分别解释其原因。
①
 时段,溶液pH几乎不变:
时段,溶液pH几乎不变:②
 时段,溶液pH明显降低:
时段,溶液pH明显降低:(4)在空气中加热分解
 ,固体质量随温度变化如图所示。计算1100℃时的分解产物化学式为
,固体质量随温度变化如图所示。计算1100℃时的分解产物化学式为
您最近一年使用:0次
名校
4 . 向 的含硫废水中加入适量
的含硫废水中加入适量 溶液,产生黑色沉淀且溶液的pH降低。
溶液,产生黑色沉淀且溶液的pH降低。 、
、 、
、 在水溶液中的物质的量含物分数随pH的分布曲线如图
在水溶液中的物质的量含物分数随pH的分布曲线如图

(1) 水溶液中存在电离平衡
水溶液中存在电离平衡 和
和 。下列关于
。下列关于 溶液的说法正确的是_____
溶液的说法正确的是_____
(2) 时,溶液中硫元素的主要存在形态为
时,溶液中硫元素的主要存在形态为_____
(3)用化学平衡移动原理解释向 的含硫废水中加入
的含硫废水中加入 溶液后pH降低的原因:
溶液后pH降低的原因:_____ 。
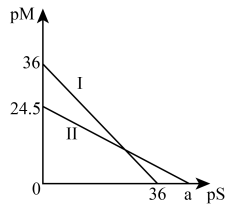
(4)某温度下,CuS和 饱和溶液中pS和pM的关系如图所示,其中
饱和溶液中pS和pM的关系如图所示,其中 ,
,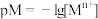 ,
, 为
为 或
或 ,下列说法错误的是____
,下列说法错误的是____
 的含硫废水中加入适量
的含硫废水中加入适量 溶液,产生黑色沉淀且溶液的pH降低。
溶液,产生黑色沉淀且溶液的pH降低。 、
、 、
、 在水溶液中的物质的量含物分数随pH的分布曲线如图
在水溶液中的物质的量含物分数随pH的分布曲线如图
(1)
 水溶液中存在电离平衡
水溶液中存在电离平衡 和
和 。下列关于
。下列关于 溶液的说法正确的是_____
溶液的说法正确的是_____| A.滴加新制氯水,平衡向左移动,溶液pH减小 |
| B.加水,平衡向右移动,溶液中氢离子浓度增大 |
C.通入过量 气体,平衡向左移动,溶液pH增大 气体,平衡向左移动,溶液pH增大 |
| D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子的浓度都减小 |
 时,溶液中硫元素的主要存在形态为
时,溶液中硫元素的主要存在形态为(3)用化学平衡移动原理解释向
 的含硫废水中加入
的含硫废水中加入 溶液后pH降低的原因:
溶液后pH降低的原因:(4)某温度下,CuS和
 饱和溶液中pS和pM的关系如图所示,其中
饱和溶液中pS和pM的关系如图所示,其中 ,
,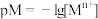 ,
, 为
为 或
或 ,下列说法错误的是____
,下列说法错误的是____
A.曲线Ⅱ代表的是 | B. |
C.此温度下CuS的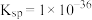 | D.此温度下的饱和溶液中 |
您最近一年使用:0次
5 . HA是一元弱酸,MA是难溶盐,且.M+不水解。在MA的饱和溶液中,经实验测定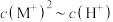 为线性关系,且y轴截距为
为线性关系,且y轴截距为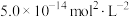 ,x轴截距为
,x轴截距为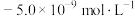 (实验曲线延长所得)。下列说法错误的是
(实验曲线延长所得)。下列说法错误的是
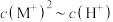 为线性关系,且y轴截距为
为线性关系,且y轴截距为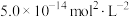 ,x轴截距为
,x轴截距为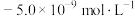 (实验曲线延长所得)。下列说法错误的是
(实验曲线延长所得)。下列说法错误的是A.该饱和溶液中,有 | B. |
| C.该线性关系仅在MA饱和时成立 | D.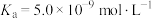 |
您最近一年使用:0次
6 . 探究卤族元素单质及其化合物的性质,下列方案设计、现象和结论都正确的是
实验方案 | 现象 | 结论 | |
A | 往碘的 溶液中加入等体积浓 溶液中加入等体积浓 溶液,振荡 溶液,振荡 | 分层,下层由紫红色变为浅粉红色,上层呈棕黄色 | 碘在浓 溶液中的溶解能力大于在 溶液中的溶解能力大于在 中的溶解能力 中的溶解能力 |
B | 用玻璃棒蘸取次氯酸钠溶液点在 试纸上 试纸上 | 试纸变白 | 次氯酸钠溶液呈中性 |
C | 向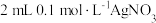 溶液中先滴加4滴 溶液中先滴加4滴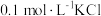 溶液,再滴加4滴 溶液,再滴加4滴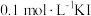 溶液 溶液 | 先产生白色沉淀,再产生黄色沉淀 |  转化为 转化为 , , 溶解度小于 溶解度小于 溶解度 溶解度 |
D | 取两份新制氯水,分别滴加 溶液和淀粉 溶液和淀粉 溶液 溶液 | 前者有白色沉淀,后者溶液变蓝色 | 氯气与水的反应存在限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-21更新
|
10389次组卷
|
20卷引用:四川省成都市第七中学2023-2024学年高一上学期12月月考化学试题
四川省成都市第七中学2023-2024学年高一上学期12月月考化学试题2023年高考浙江卷化学真题(6月)(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题11-16)(已下线)专题14 化学实验方案的设计与评价(已下线)专题14 化学实验方案的设计与评价(已下线)考点09 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点巩固卷12 化学实验基础(一)(3大考点67题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)2019年高考江苏卷化学试题变式题(不定项选择题)(已下线)第17讲实验方案的设计与评价(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)(已下线)广东省东莞市光正实验学校2023-2024学年高三上学期第二次月孝化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)河南省濮阳市油田第二高级中学2023-2024学年高三10月份阶段性考试化学试题四川省内江市第六中学2023-2024学年高三上学期入学考试化学试题(已下线)题型03 离子方程式正误判断 离子共存、检验和推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)选择题6-10题型15 沉淀溶解平衡及图像分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)2024届河北省实验中学高三年级上学期第一次月考化学试题四川省达州外国语学校2023-2024学年高二下学期3月月考化学试题
7 . 某温度下,CuS和 饱和溶液中pS和pM的关系如图所示,其中
饱和溶液中pS和pM的关系如图所示,其中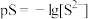 ,
,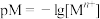 ,
, 为
为 或
或 ,下列说法错误的是
,下列说法错误的是
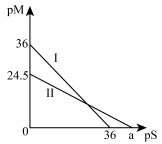
 饱和溶液中pS和pM的关系如图所示,其中
饱和溶液中pS和pM的关系如图所示,其中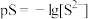 ,
,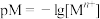 ,
, 为
为 或
或 ,下列说法错误的是
,下列说法错误的是
A.曲线Ⅱ代表的是 | B.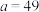 |
C.此温度下CuS的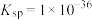 | D.此温度下的饱和溶液中 |
您最近一年使用:0次
解题方法
8 . 利用菱镁矿 (含杂质
(含杂质 、
、 )制取镁的工艺流程如图,下列说法正确的是
)制取镁的工艺流程如图,下列说法正确的是

 (含杂质
(含杂质 、
、 )制取镁的工艺流程如图,下列说法正确的是
)制取镁的工艺流程如图,下列说法正确的是
| A.“酸浸”时会发生氧化还原反应 | B.“氧化”时可用稀硝酸代替 溶液 溶液 |
C.沉淀混合物为 和 和 | D.电解 溶液可得到金属 溶液可得到金属 |
您最近一年使用:0次
9 . 实验室以FeCl2溶液为原料制备高密度磁记录材料Fe/Fe3O4复合物。
(1)在氩气气氛下,向装有50mL1mol·L-1FeCl2溶液的三颈烧瓶中逐滴加入100mL14mol·L-1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。
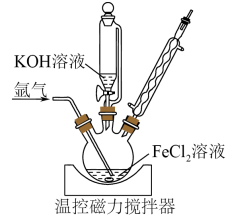
①三颈烧瓶发生反应的离子方程式为_______ 。
②检验反应是否进行完全的操作是_______ 。
(2)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品3.24g。
①焙烧需在隔绝空气条件下进行,原因是_______ 。
②计算实验所得产品的产率_______ (写出计算过程)。
(3)以FeCl2溶液为原料还可制备软磁性材料α−Fe2O3.已知:Fe(OH)2开始沉淀的pH=6.5。请补充完整实验方案:在搅拌下向FeCl2溶液中缓慢加入氨水-NH4HCO3混合溶液,控制溶液pH不大于6.5,_______ ,将固体干燥,得到纯净的FeCO3,将其放入管式炉内煅烧2h,获得产品α−Fe2O3(可选用的试剂:2mol•L−1盐酸、2mol•L−1硝酸、AgNO3溶液、蒸馏水)。
(1)在氩气气氛下,向装有50mL1mol·L-1FeCl2溶液的三颈烧瓶中逐滴加入100mL14mol·L-1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。

①三颈烧瓶发生反应的离子方程式为
②检验反应是否进行完全的操作是
(2)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品3.24g。
①焙烧需在隔绝空气条件下进行,原因是
②计算实验所得产品的产率
(3)以FeCl2溶液为原料还可制备软磁性材料α−Fe2O3.已知:Fe(OH)2开始沉淀的pH=6.5。请补充完整实验方案:在搅拌下向FeCl2溶液中缓慢加入氨水-NH4HCO3混合溶液,控制溶液pH不大于6.5,
您最近一年使用:0次
10 . 向 饱和溶液(有足量
饱和溶液(有足量 固体)中滴加氨水,发生反应
固体)中滴加氨水,发生反应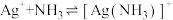 和
和 ,
,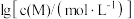 与
与 的关系如下图所示(其中M代表
的关系如下图所示(其中M代表 、
、 、
、 或
或 )。
)。

下列说法错误的是
 饱和溶液(有足量
饱和溶液(有足量 固体)中滴加氨水,发生反应
固体)中滴加氨水,发生反应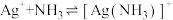 和
和 ,
,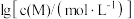 与
与 的关系如下图所示(其中M代表
的关系如下图所示(其中M代表 、
、 、
、 或
或 )。
)。 
下列说法错误的是
A.曲线I可视为 溶解度随 溶解度随 浓度变化曲线 浓度变化曲线 |
B. 的溶度积常数 的溶度积常数 |
C.反应 的平衡常数K的值为 的平衡常数K的值为 |
D.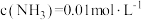 时,溶液中 时,溶液中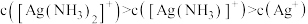 |
您最近一年使用:0次
2023-06-10更新
|
13855次组卷
|
14卷引用:湖北省恩施高中2023-2024学年高一下学期入学考试化学试题
湖北省恩施高中2023-2024学年高一下学期入学考试化学试题2023年高考新课标理综化学真题(已下线)T13-溶液中的离子平衡(已下线)2023年高考化学真题完全解读(新课标卷:适用安徽、云南、山西、吉林、黑龙江五省)(PPT+Word)(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)考点29 沉淀溶解平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)(已下线)实验03 探究外界条件对化学平衡移动的影响-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)(已下线)考点4 沉淀溶解平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型03 电解质溶液图像分析-2024年高考化学答题技巧与模板构建题型15 沉淀溶解平衡及图像分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型18 化学反应原理综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)



