名校
1 .  可用于制备补铁剂,也可制备铁红
可用于制备补铁剂,也可制备铁红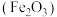 。以下是用磁铁矿(主要成分
。以下是用磁铁矿(主要成分 、含
、含 和
和 等杂质)制取
等杂质)制取 的工艺流程:
的工艺流程:
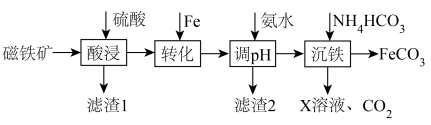
已知:① 不溶于水,也不与硫酸反应;
不溶于水,也不与硫酸反应;
②调 可将
可将 转化为沉淀与
转化为沉淀与 分离,但不能将
分离,但不能将 与
与 分离。
分离。
请回答下列问题:
(1)“酸浸”时 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)“转化”工序加入Fe的作用是(用离子方程式表示)___________ 。
(3)滤渣1的成分是___________ (填化学式)。
(4)产品 在空气中煅烧可制备铁红,写出反应的化学反应方程式
在空气中煅烧可制备铁红,写出反应的化学反应方程式___________ ;在实验室中完成本操作所用的主要仪器是___________ (填序号)。
A. B.
B. C.
C.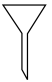
若起始时 的质量为ag,最终制得
的质量为ag,最终制得 为bg,则
为bg,则 产率为
产率为___________ 。(产率= ,用含a,b的代数式表示)。
,用含a,b的代数式表示)。
(5)现有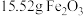 和
和 组成的固体混合物,用
组成的固体混合物,用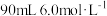 盐酸能恰好将之完全溶解。若将此固体混合物用
盐酸能恰好将之完全溶解。若将此固体混合物用 完全还原,则生成铁的物质的量为
完全还原,则生成铁的物质的量为___________ mol
 可用于制备补铁剂,也可制备铁红
可用于制备补铁剂,也可制备铁红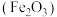 。以下是用磁铁矿(主要成分
。以下是用磁铁矿(主要成分 、含
、含 和
和 等杂质)制取
等杂质)制取 的工艺流程:
的工艺流程:
已知:①
 不溶于水,也不与硫酸反应;
不溶于水,也不与硫酸反应;②调
 可将
可将 转化为沉淀与
转化为沉淀与 分离,但不能将
分离,但不能将 与
与 分离。
分离。请回答下列问题:
(1)“酸浸”时
 发生反应的离子方程式为
发生反应的离子方程式为(2)“转化”工序加入Fe的作用是(用离子方程式表示)
(3)滤渣1的成分是
(4)产品
 在空气中煅烧可制备铁红,写出反应的化学反应方程式
在空气中煅烧可制备铁红,写出反应的化学反应方程式A.
 B.
B. C.
C.
若起始时
 的质量为ag,最终制得
的质量为ag,最终制得 为bg,则
为bg,则 产率为
产率为 ,用含a,b的代数式表示)。
,用含a,b的代数式表示)。(5)现有
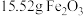 和
和 组成的固体混合物,用
组成的固体混合物,用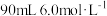 盐酸能恰好将之完全溶解。若将此固体混合物用
盐酸能恰好将之完全溶解。若将此固体混合物用 完全还原,则生成铁的物质的量为
完全还原,则生成铁的物质的量为
您最近一年使用:0次
名校
解题方法
2 . 锰酸锂离子蓄电池是第二代锂离子动力电池,性能优良。工业上用某软锰矿(主要成分为 ,还含有少量铁、铝及硅等氧化物)为原料制备锰酸锂(
,还含有少量铁、铝及硅等氧化物)为原料制备锰酸锂( )。流程如图:
)。流程如图:
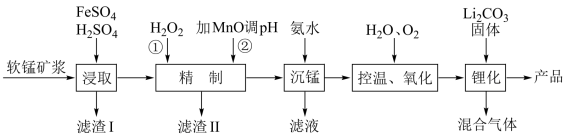
(1)“浸取”得到的浸取液中阳离子主要是Mn2+,生成Mn2+的离子方程式为___________ 。
(2)滤渣Ⅱ的主要成分是___________ ;“精制”中加入H2O2的量比理论值大得多,其主要原因是___________ 。
(3)工业上也可以将“精制”后的滤液加入 来合成MnO2。
来合成MnO2。 中S的化合价为+6价,加入
中S的化合价为+6价,加入 溶液合成MnO2发生反应的离子方程式为:
溶液合成MnO2发生反应的离子方程式为:___________ 。
(4)“锂化”是将MnO2和 按4:1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品。所得混合气体的成分是
按4:1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品。所得混合气体的成分是___________ 。
 ,还含有少量铁、铝及硅等氧化物)为原料制备锰酸锂(
,还含有少量铁、铝及硅等氧化物)为原料制备锰酸锂( )。流程如图:
)。流程如图:
(1)“浸取”得到的浸取液中阳离子主要是Mn2+,生成Mn2+的离子方程式为
(2)滤渣Ⅱ的主要成分是
(3)工业上也可以将“精制”后的滤液加入
 来合成MnO2。
来合成MnO2。 中S的化合价为+6价,加入
中S的化合价为+6价,加入 溶液合成MnO2发生反应的离子方程式为:
溶液合成MnO2发生反应的离子方程式为:(4)“锂化”是将MnO2和
 按4:1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品。所得混合气体的成分是
按4:1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品。所得混合气体的成分是
您最近一年使用:0次
3 . I.由硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、Al2O3和SiO2)得到绿矾(FeSO4·7H2O),然后制取透明氧化铁颜料的流程如下:
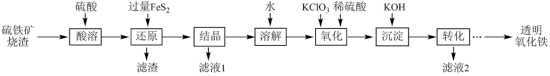
已知:①透明氧化铁又称纳米氧化铁,粒子直径微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
②Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)FeS2的电子式为___________ 。
(2)“滤渣”中的主要成分是___________ 。
(3)“还原”过程中涉及的离子方程式为___________ 。
(4)流程中“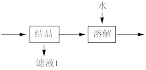 ”环节的目的是
”环节的目的是___________ 。
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以___________ 。
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示:
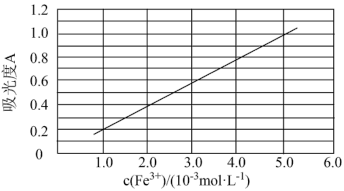
称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL。测得溶液吸光度A=0.8,则透明氧化铁中氧化铁红(Fe2O3)的质量分数为___________ %(保留小数点后一位)。
Ⅱ.氧化亚铜(Cu2O)用途广泛,干法生产Cu2O粉末的主要工艺流程如下:
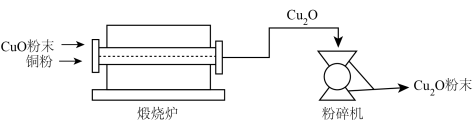
(7)粉碎机中,发生的变化属于___________ (填“物理变化”或“化学变化”)。
(8)800~900℃时,煅烧炉中发生化合反应,该反应的化学方程式为___________ 。
Ⅲ.运用热重分析法推测产物
称取 草酸亚铁晶体(
草酸亚铁晶体(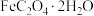 )加热分解,得到剩余固体质量随温度变化的曲线如图所示:
)加热分解,得到剩余固体质量随温度变化的曲线如图所示:
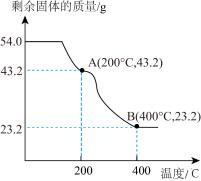
(9)已知B点时,固体只含有一种铁的氧化物,根据上图可知B点固体物质的化学式为_______ 。
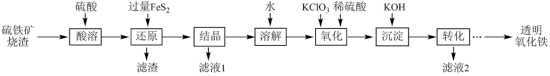
已知:①透明氧化铁又称纳米氧化铁,粒子直径微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
②Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)FeS2的电子式为
(2)“滤渣”中的主要成分是
(3)“还原”过程中涉及的离子方程式为
(4)流程中“
 ”环节的目的是
”环节的目的是(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示:

称取3.47g透明氧化铁,用稀硫酸溶解并定容至1L,准确移取该溶液10.00mL,加入足量KSCN溶液,再用蒸馏水定容至100mL。测得溶液吸光度A=0.8,则透明氧化铁中氧化铁红(Fe2O3)的质量分数为
Ⅱ.氧化亚铜(Cu2O)用途广泛,干法生产Cu2O粉末的主要工艺流程如下:

(7)粉碎机中,发生的变化属于
(8)800~900℃时,煅烧炉中发生化合反应,该反应的化学方程式为
Ⅲ.运用热重分析法推测产物
称取
 草酸亚铁晶体(
草酸亚铁晶体(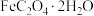 )加热分解,得到剩余固体质量随温度变化的曲线如图所示:
)加热分解,得到剩余固体质量随温度变化的曲线如图所示:
(9)已知B点时,固体只含有一种铁的氧化物,根据上图可知B点固体物质的化学式为
您最近一年使用:0次
名校
4 .  (相对分子质量为:168.5)微溶于水、不潮解、相对稳定,是一种无机抗菌剂。以菱镁矿(主要成分为
(相对分子质量为:168.5)微溶于水、不潮解、相对稳定,是一种无机抗菌剂。以菱镁矿(主要成分为 ,还含有少量
,还含有少量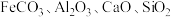 )为主要原料,制备
)为主要原料,制备 的工业流程如下图所示,请回答下列问题:
的工业流程如下图所示,请回答下列问题:

已知:①该工艺条件下,有关金属离子开始沉淀和沉淀完全的 见下表
见下表
②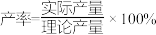
(1) 所属物质类别为
所属物质类别为___________ 盐(填“酸式”或“碱式”或“正”),该物质在稀硫酸溶液中具有杀菌、漂白作用,其原因是___________ (用离子方程式解释)。
(2)滤渣①的成分为___________ 。
(3)“氧化”时,不能在较高温度下进行,可能的原因是________ , 的作用是
的作用是_________ (用离子方程式表示)。
(4)“调 ”时,加入物质X将该溶液的
”时,加入物质X将该溶液的 范围应调节为
范围应调节为___________ ~9.5之间,最适宜使用的X是___________ (填标号)
A. B.
B. C.
C.
(5)“沉镁”后,得到的 产品还需洗涤,证明产品已洗涤干净的方法是
产品还需洗涤,证明产品已洗涤干净的方法是___________ 。
(6)某工厂用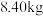 菱镁矿(
菱镁矿( 的质量分数为
的质量分数为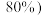 制备
制备 ,最终得到产品
,最终得到产品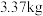 ,产率为
,产率为___________ 。
 (相对分子质量为:168.5)微溶于水、不潮解、相对稳定,是一种无机抗菌剂。以菱镁矿(主要成分为
(相对分子质量为:168.5)微溶于水、不潮解、相对稳定,是一种无机抗菌剂。以菱镁矿(主要成分为 ,还含有少量
,还含有少量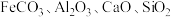 )为主要原料,制备
)为主要原料,制备 的工业流程如下图所示,请回答下列问题:
的工业流程如下图所示,请回答下列问题:
已知:①该工艺条件下,有关金属离子开始沉淀和沉淀完全的
 见下表
见下表| 金属氢氧化物 | 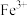 | 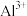 | 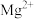 |
开始沉淀的 | 2.3 | 3.5 | 9.5 |
完全沉淀的 | 3.2 | 4.6 | 11.1 |
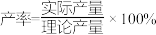
(1)
 所属物质类别为
所属物质类别为(2)滤渣①的成分为
(3)“氧化”时,不能在较高温度下进行,可能的原因是
 的作用是
的作用是(4)“调
 ”时,加入物质X将该溶液的
”时,加入物质X将该溶液的 范围应调节为
范围应调节为A.
 B.
B. C.
C.
(5)“沉镁”后,得到的
 产品还需洗涤,证明产品已洗涤干净的方法是
产品还需洗涤,证明产品已洗涤干净的方法是(6)某工厂用
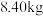 菱镁矿(
菱镁矿( 的质量分数为
的质量分数为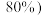 制备
制备 ,最终得到产品
,最终得到产品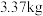 ,产率为
,产率为
您最近一年使用:0次
名校
解题方法
5 . 能正确表示下列化学反应的离子方程式的是
A.氢氧化钡溶液与硫酸的反应:Ba2++OH-+H++ =BaSO4+H2O =BaSO4+H2O |
B.Ca(OH)2溶液与少量的NaHCO3溶液反应: +Ca2++OH−=CaCO3↓+H2O +Ca2++OH−=CaCO3↓+H2O |
C.向饱和硫酸银溶液中滴加少量氯化钠溶液:Ag2SO4+2Cl-=2AgCl+ |
| D.向碳酸钙固体粉末中加入足量的醋酸:CaCO3+2H+=Ca2++CO2+H2O |
您最近一年使用:0次
名校
解题方法
6 . 常温下有浓度均为 的四种溶液:①
的四种溶液:① 溶液;②
溶液;② 溶液;③HCl溶液;④氨水
溶液;③HCl溶液;④氨水
(1)上述溶液中,溶质可发生水解的是___________ (填序号)。
(2)向④中加入少量氯化铵固体,此时氨水的电离平衡___________ 移动(填“向右”、“向左”、或“不”),溶液中 的值
的值___________ (填“增大”、“减小”或“不变”)。
(3)若将③和④混合后溶液恰好呈中性,则混合前③的体积___________ ④的体积(填“大于”、“小于”或“等于”),此时溶液中离子浓度由大到小的顺序是___________ 。
(4)取10mL③,加水稀释到500mL,则此时溶液中由水电离出的
___________ 。
(5)已知18℃时, 的
的 ,其饱和溶液中
,其饱和溶液中 的物质的量浓度是
的物质的量浓度是___________ 。
 的四种溶液:①
的四种溶液:① 溶液;②
溶液;② 溶液;③HCl溶液;④氨水
溶液;③HCl溶液;④氨水(1)上述溶液中,溶质可发生水解的是
(2)向④中加入少量氯化铵固体,此时氨水的电离平衡
 的值
的值(3)若将③和④混合后溶液恰好呈中性,则混合前③的体积
(4)取10mL③,加水稀释到500mL,则此时溶液中由水电离出的

(5)已知18℃时,
 的
的 ,其饱和溶液中
,其饱和溶液中 的物质的量浓度是
的物质的量浓度是
您最近一年使用:0次
名校
7 . 向 的
的 溶液中逐滴滴加
溶液中逐滴滴加 的
的 溶液,所得沉淀的物质的量与加入
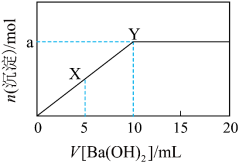
溶液,所得沉淀的物质的量与加入 溶液体积的关系如下图所示。下列说法正确的是
溶液体积的关系如下图所示。下列说法正确的是
 的
的 溶液中逐滴滴加
溶液中逐滴滴加 的
的 溶液,所得沉淀的物质的量与加入
溶液,所得沉淀的物质的量与加入 溶液体积的关系如下图所示。下列说法正确的是
溶液体积的关系如下图所示。下列说法正确的是
A.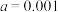 |
B.0~5 mL时,溶液中发生反应的离子方程式为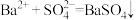 |
| C.Y点时,所得溶液呈中性 |
D.20 mL时,溶液中 和 和 的物质的量相等 的物质的量相等 |
您最近一年使用:0次
名校
8 . 在有AgCl沉淀存在的AgCl饱和溶液中达到如下平衡:AgCl(s) Ag+(aq)+Cl-(aq)。在下列条件下,AgCl沉淀的量如何变化?(填:增多、减少、不变)
Ag+(aq)+Cl-(aq)。在下列条件下,AgCl沉淀的量如何变化?(填:增多、减少、不变)
(1)加入KCl固体______ ;
(2)加入AgNO3溶液______ 。
(3)加压______ 。
 Ag+(aq)+Cl-(aq)。在下列条件下,AgCl沉淀的量如何变化?(填:增多、减少、不变)
Ag+(aq)+Cl-(aq)。在下列条件下,AgCl沉淀的量如何变化?(填:增多、减少、不变)(1)加入KCl固体
(2)加入AgNO3溶液
(3)加压
您最近一年使用:0次
名校
9 . 钛(Ti)的性质稳定,有良好的耐高温、抗酸碱、高强度、低密度等特性,工业上常用钛铁矿(主要含 和少量
和少量 、MgO、
、MgO、 、
、 等)通过如图所示工艺流程制取钛,并回收镁、铝、铁等。
等)通过如图所示工艺流程制取钛,并回收镁、铝、铁等。
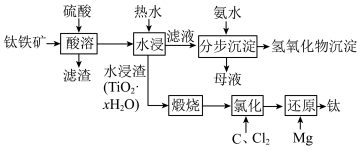
已知:① 易水解,只能存在于强酸性溶液中;
易水解,只能存在于强酸性溶液中;
②常温下,相关金属离子开始沉淀和沉淀完全的pH如表所示。
(1)为了提高“酸溶”的速率,可采取的措施有___________ (任写一点)
(2)“酸溶”后,钛主要以 形式存在,写出相应反应的离子方程式:
形式存在,写出相应反应的离子方程式:___________ 。
(3)“分步沉淀”时用氨水逐步调节pH至11.1,依次析出的金属离子是___________ (填离子符号);当 沉淀完全时,“母液”中
沉淀完全时,“母液”中 的浓度为
的浓度为___________  。
。
(4)“酸溶”后,加入热水进行水浸可得水浸渣( ),写出“水浸”过程的离子反应方程式
),写出“水浸”过程的离子反应方程式___________ 。
(5)“氯化”过程在高温下会生成一种有毒气体,写出“氯化”过程的化学方程式___________ 。
(6)“还原”在800~900℃及惰性气体的保护下进行,要在惰性气体的保护下进行的原因是___________ 。
 和少量
和少量 、MgO、
、MgO、 、
、 等)通过如图所示工艺流程制取钛,并回收镁、铝、铁等。
等)通过如图所示工艺流程制取钛,并回收镁、铝、铁等。
已知:①
 易水解,只能存在于强酸性溶液中;
易水解,只能存在于强酸性溶液中;②常温下,相关金属离子开始沉淀和沉淀完全的pH如表所示。
| 金属离子 |  |  |  |  |
| 开始沉淀的pH | 2.2 | 6.5 | 3.5 | 9.5 |
沉淀完全( )的pH )的pH | 3.2 | 9.7 | 4.7 | 11.1 |
(2)“酸溶”后,钛主要以
 形式存在,写出相应反应的离子方程式:
形式存在,写出相应反应的离子方程式:(3)“分步沉淀”时用氨水逐步调节pH至11.1,依次析出的金属离子是
 沉淀完全时,“母液”中
沉淀完全时,“母液”中 的浓度为
的浓度为 。
。(4)“酸溶”后,加入热水进行水浸可得水浸渣(
 ),写出“水浸”过程的离子反应方程式
),写出“水浸”过程的离子反应方程式(5)“氯化”过程在高温下会生成一种有毒气体,写出“氯化”过程的化学方程式
(6)“还原”在800~900℃及惰性气体的保护下进行,要在惰性气体的保护下进行的原因是
您最近一年使用:0次
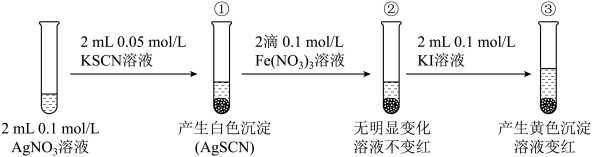
10 . 为研究沉淀的生成及转化,进行如下实验。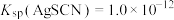
下列关于该实验的分析不正确 的是
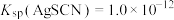
下列关于该实验的分析
A.①中产生白色沉淀的原因是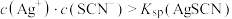 |
B.充分反应后①中 浓度为 浓度为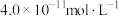 |
C.③中产生黄色沉淀可证明 向 向 沉淀转化 沉淀转化 |
D.②中加入KI溶液后一定发生了反应 |
您最近一年使用:0次
2024-01-01更新
|
303次组卷
|
8卷引用:四川省成都市第七中学2023-2024学年高一上学期12月月考化学试题
四川省成都市第七中学2023-2024学年高一上学期12月月考化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)辽宁省大连市第十二中学2023-2024学年高二上学期12月学情反馈化学试题江西省宜春市宜丰中学2023-2024学年高三上学期1月月考化学试题(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)江西省宜春市丰城市东煌学校2023-2024学年高二上学期1月期末化学试题



