名校
解题方法
1 . 下列实验操作、现象和解释与结论有错误的是
| 选项 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向硅酸钠溶液中通入适量 | 溶液变浑浊 | 酸性: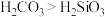 |
| B | 用 计测同温同浓度的 计测同温同浓度的 和 和 溶液的 溶液的 | 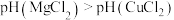 | 金属性: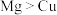 |
| C | 向足量含有 的 的 溶液中滴加2滴氯水 溶液中滴加2滴氯水 | 溶液变血红色 | 还原性: |
| D | 向NaCl和KI混合溶液中滴加 溶液 溶液 | 先产生黄色沉淀,后产生白色沉淀 | 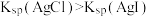 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 25℃时,某一元弱酸HX的电离平衡常数Ka=1.0×10-5,则:
(1)0.1mol/L的HX溶液中HX的电离度约为_______ 。
(2)若1L0.1mol/L的HX溶液中加入1mL0.1mol/LAgNO3溶液生成了AgX沉淀,则该温度下Ksp(AgX)≤______ (假设混合后溶液总体积仍为1L,且忽略因稀释导致的HX溶液电离平衡的移动);
(3)0.1mol/L的NaX溶液的pH值约为_____ ,该溶液中水电离的c(OH-)为_______ mol/L;
(4)若用0.1mol/L的NaOH标准溶液来滴定锥形瓶中未知浓度的HX溶液应选择的指示剂为_______ (选填:甲基橙、酚酞或紫色石蕊),若滴入的NaOH溶液恰好中和了一半,那么此时溶液中存在微粒的浓度由大到小的次序是_______ 。
(1)0.1mol/L的HX溶液中HX的电离度约为
(2)若1L0.1mol/L的HX溶液中加入1mL0.1mol/LAgNO3溶液生成了AgX沉淀,则该温度下Ksp(AgX)≤
(3)0.1mol/L的NaX溶液的pH值约为
(4)若用0.1mol/L的NaOH标准溶液来滴定锥形瓶中未知浓度的HX溶液应选择的指示剂为
您最近一年使用:0次
解题方法
3 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
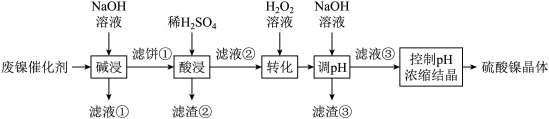
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是___________ 和洗去油脂。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式___________ 。
(2)“滤液②”中含有的金属离子是Ni2+和___________ 。
(3)“转化”中可替代H2O2的物质是___________ 。若工艺流程改为先“调pH”后“转化”,即
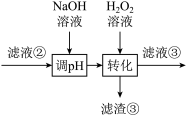
“滤液③”中可能含有的杂质离子为___________ 。
(4)硫酸镍溶液在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH.写出该反应的离子方程式___________ 。
(5)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是___________ 。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时的pH 沉淀完全时的pH | 7.2 8.7 | 3.7 4.7 | 2.2 3.2 | 7.5 9.0 |
(1)“碱浸”中NaOH的两个作用分别是
(2)“滤液②”中含有的金属离子是Ni2+和
(3)“转化”中可替代H2O2的物质是

“滤液③”中可能含有的杂质离子为
(4)硫酸镍溶液在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH.写出该反应的离子方程式
(5)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近一年使用:0次
4 . 利用某金属废屑(含Cu、Al、Fe及其少量氧化物)制备胆矾的工艺流程如图所示.
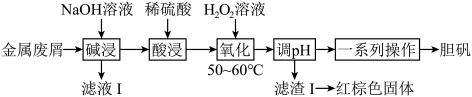
回答下列问题:
(1)“碱浸”工序Al发生反应的离子方程式为____________ .
(2)相关离子在溶液中的去除率随pH的变化如图所示.
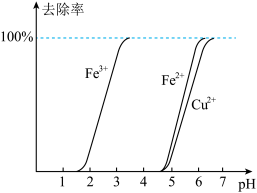
①“氧化”工序中 的作用是
的作用是__________ 、______________ (用离子方程式表示);“氧化”工序采取的加热方式为____________ ,温度不宜过高的原因是___________ .
②“调pH”时,应控制溶液pH的适宜范围为__________ (填标号).
A.2.0~3.0 B.3.0~4.0 C.4.0~5.0
(3)红棕色固体的用途有___________ (任写一种).“一系列操作”中包含__________ 、__________ 、过滤、洗涤、干燥.

回答下列问题:
(1)“碱浸”工序Al发生反应的离子方程式为
(2)相关离子在溶液中的去除率随pH的变化如图所示.

①“氧化”工序中
 的作用是
的作用是②“调pH”时,应控制溶液pH的适宜范围为
A.2.0~3.0 B.3.0~4.0 C.4.0~5.0
(3)红棕色固体的用途有
您最近一年使用:0次
5 . 处理某铜冶金污水(含 、
、 、
、 、
、 )的部分流程如下:
)的部分流程如下:
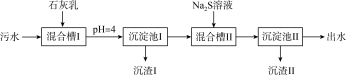
已知:①常温下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
②常温下, ,
, 。
。
下列说法错误的是
 、
、 、
、 、
、 )的部分流程如下:
)的部分流程如下:
已知:①常温下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
物质 |
|
|
开始沉淀时的pH | 1.8 | 3.5 |
沉淀完全时 | 3 | 4.6 |
 ,
, 。
。下列说法错误的是
A. |
B. 溶液呈碱性,其主要原因是 溶液呈碱性,其主要原因是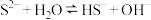 |
C.“沉淀池Ⅱ”中,当 和 和 完全沉淀时,溶液中 完全沉淀时,溶液中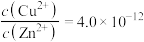 |
| D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水 |
您最近一年使用:0次
解题方法
6 . 用如图所示实验装置进行相应的实验,不能达到实验目的的是
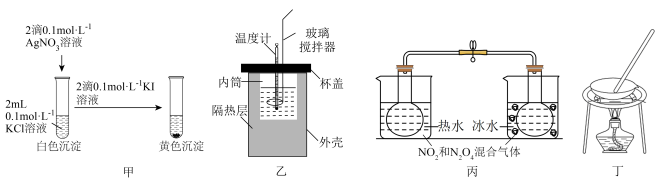

A.图甲:证明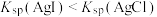 |
| B.图乙:测量盐酸和氢氧化钠反应的反应热 |
| C.图丙:验证温度对化学平衡的影响 |
D.图丁:由 固体制备无水氯化铁 固体制备无水氯化铁 |
您最近一年使用:0次
解题方法
7 . CO可用于合成甲醇,化学方程式为 。
。
(1)图1是在不同温度下CO的转化率随时间变化的曲线。
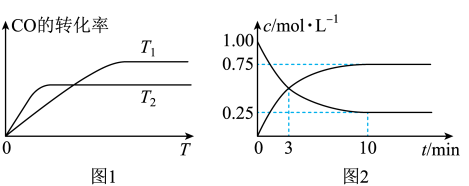
①判断图1中
______  (填“>”“=”或“<”,下同),反应
(填“>”“=”或“<”,下同),反应 的
的
______ 0。
②在某温度下,往体积为 的密闭容器中,充入
的密闭容器中,充入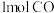 和
和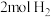 ,经测得CO和
,经测得CO和 的浓度随时间变化如图2所示。则达到平衡时
的浓度随时间变化如图2所示。则达到平衡时 的转化率为
的转化率为__________ 。
(2)在容积为 的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。
的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。
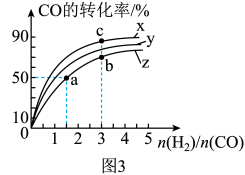
图3是上述三种温度下 和CO的起始组成比(起始时CO的物质的量均为
和CO的起始组成比(起始时CO的物质的量均为 )与CO平衡转化率的关系,则曲线z对应的温度是
)与CO平衡转化率的关系,则曲线z对应的温度是__________ ℃;曲线上a点对应反应的化学平衡常数
__________ 。曲线上a、b、c点对应的化学平衡常数分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为__________ 。
(3) 、
、 两种温度下,
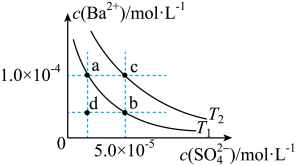
两种温度下, 在水中的沉淀溶解平衡曲线如图所示,回答下列问题:
在水中的沉淀溶解平衡曲线如图所示,回答下列问题:
①
______  (填“>”“<”或“=”),
(填“>”“<”或“=”), 时
时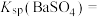
__________ 。
②根据 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是__________ (填字母)。
A.加入 可由a点变为b点
可由a点变为b点
B.在 曲线上方区域(不含曲线)的任意一点时,均有
曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成
C.蒸发溶剂可能由d点变为 曲线上a,b之间的某一点(不含a、b)
曲线上a,b之间的某一点(不含a、b)
D.升温可由b点变为d点
 。
。(1)图1是在不同温度下CO的转化率随时间变化的曲线。
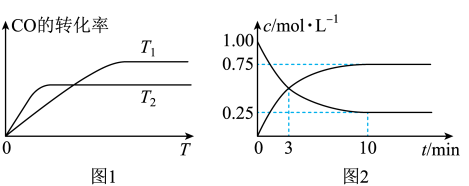
①判断图1中

 (填“>”“=”或“<”,下同),反应
(填“>”“=”或“<”,下同),反应 的
的
②在某温度下,往体积为
 的密闭容器中,充入
的密闭容器中,充入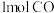 和
和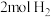 ,经测得CO和
,经测得CO和 的浓度随时间变化如图2所示。则达到平衡时
的浓度随时间变化如图2所示。则达到平衡时 的转化率为
的转化率为(2)在容积为
 的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。
的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。图3是上述三种温度下
 和CO的起始组成比(起始时CO的物质的量均为
和CO的起始组成比(起始时CO的物质的量均为 )与CO平衡转化率的关系,则曲线z对应的温度是
)与CO平衡转化率的关系,则曲线z对应的温度是
 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为
(3)
 、
、 两种温度下,
两种温度下, 在水中的沉淀溶解平衡曲线如图所示,回答下列问题:
在水中的沉淀溶解平衡曲线如图所示,回答下列问题:
①

 (填“>”“<”或“=”),
(填“>”“<”或“=”), 时
时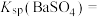
②根据
 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是A.加入
 可由a点变为b点
可由a点变为b点B.在
 曲线上方区域(不含曲线)的任意一点时,均有
曲线上方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成C.蒸发溶剂可能由d点变为
 曲线上a,b之间的某一点(不含a、b)
曲线上a,b之间的某一点(不含a、b)D.升温可由b点变为d点
您最近一年使用:0次
解题方法
8 . 化学与生活关系密切,下列说法正确的是
A.施肥时,草木灰(有效成分是 )与 )与 混合使用,K和N同时补充,效果较好 混合使用,K和N同时补充,效果较好 |
| B.钢管表面镀锌可以防止钢管被腐蚀,镀层破损后,钢管腐蚀会加速 |
C.水垢中的 ,可先用 ,可先用 溶液处理,而后用酸除去 溶液处理,而后用酸除去 |
| D.居民生活用气的天然气,燃烧时反应物的键能总和大于生成物的键能总和 |
您最近一年使用:0次
24-25高一上·全国·假期作业
9 . 下列指定反应的离子方程式正确的是
A. 悬浊液中通 悬浊液中通 : :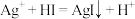 |
B. 溶液中 溶液中 的水解: 的水解: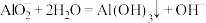 |
C.加入 将污水中的 将污水中的 氧化成 氧化成 : :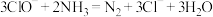 |
D. 溶液中通入 溶液中通入 : :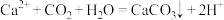 |
您最近一年使用:0次
名校
解题方法
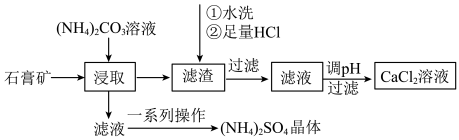
10 . 以石膏矿(主要含2CaSO4•H2O,还含有少量Al2O3、Fe2O3、SiO2)为原料制取CaCl2溶液和(NH4)2SO4晶体,一种工艺流程如下:___________ 。
(2)“浸取”时,发生反应:CaSO4(s)+CO (aq)
(aq) CaCO3(s)+SO
CaCO3(s)+SO (aq)。达到平衡时,溶液中
(aq)。达到平衡时,溶液中 =
=___________ 。[已知:Ksp(CaSO4)=4.8×10-5,Ksp(CaCO3)=3×10-9]
(3)将氨水和NH4HCO3溶液混合,可得到(NH4)2CO3溶液,其化学方程式为___________ ,浸取时控制反应温度在60~70℃,控温方法是___________ 。
(4)“滤渣”的主要成分是Al2O3、Fe2O3、___________ ;“一系列操作”为:加入适量稀硫酸,然后经过减压蒸发浓缩、___________ 、过滤、洗涤、干燥。
(5)已知:相关金属离子形成氢氧化物沉淀的pH范围如下:
则“调pH”中需要调节的pH范围___________ 。
(2)“浸取”时,发生反应:CaSO4(s)+CO
 (aq)
(aq) CaCO3(s)+SO
CaCO3(s)+SO (aq)。达到平衡时,溶液中
(aq)。达到平衡时,溶液中 =
=(3)将氨水和NH4HCO3溶液混合,可得到(NH4)2CO3溶液,其化学方程式为
(4)“滤渣”的主要成分是Al2O3、Fe2O3、
(5)已知:相关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Al3+ | Ca2+ |
| 开始沉淀的pH | 1.8 | 3.4 | 11.3 |
| 沉淀完全的pH | 3.2 | 4.8 | … |
| pH=8.3时,Al(OH)3开始溶解 | |||
您最近一年使用:0次
2024-03-13更新
|
88次组卷
|
2卷引用:广东省茂名市高州中学2023-2024学年高一下学期期中考试化学试题



 的pH
的pH

