1 . 下列说法正确的是
| A.向AgI沉淀中加入饱和KCl溶液,有白色沉淀生成,说明AgCl比AgI更难溶 |
B.向浓度均为 的 的 和 和 混合溶液中逐滴加入氨水,若先生成蓝色 混合溶液中逐滴加入氨水,若先生成蓝色 沉淀,则 沉淀,则 |
C.向 饱和溶液中加入饱和 饱和溶液中加入饱和 溶液,有白色沉淀产生,说明 溶液,有白色沉淀产生,说明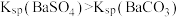 |
D.向1mL 的NaOH溶液中滴入1mL 的NaOH溶液中滴入1mL 的 的 溶液,产生白色沉淀后,再滴加2滴 溶液,产生白色沉淀后,再滴加2滴 的 的 溶液,又生成红褐色沉淀,说明在相同温度下的溶解度: 溶液,又生成红褐色沉淀,说明在相同温度下的溶解度: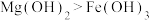 |
您最近一年使用:0次
2023-12-31更新
|
412次组卷
|
4卷引用:贵州省黔西南布依族苗族自治州2023-2024学年高一上学期1月期末化学试题
贵州省黔西南布依族苗族自治州2023-2024学年高一上学期1月期末化学试题陕西省名校协作体2023-2024学年高三上学期12月月考化学试题题型15 沉淀溶解平衡及图像分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
解题方法
2 . 五氧化二钒用作有机化工的催化剂。从废钒催化剂(主要成分为 、
、 、
、 、
、 、
、 和
和 )中回收
)中回收 ,既避免污染环境又有利于资源综合利用,该工艺流程如下:
,既避免污染环境又有利于资源综合利用,该工艺流程如下:
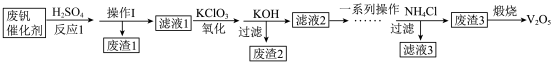
已知:金属钒的氧化物能与酸反应; 不溶于水也不溶于初中常见的酸。回答下列问题:
不溶于水也不溶于初中常见的酸。回答下列问题:
(1)实验室进行操作I时,需要用到的玻璃仪器有漏斗、烧杯和_______ 。
(2)加入 的作用是将
的作用是将 转化为
转化为 ,则写出该转化过程中相关的离子方程式
,则写出该转化过程中相关的离子方程式_______ 。
(3)加入 的作用之一是保证钒存在于溶液中时,把
的作用之一是保证钒存在于溶液中时,把 与
与 转化为沉淀,但
转化为沉淀,但 不宜过量,不然滤液2中引入
不宜过量,不然滤液2中引入 和
和_______ 杂质(填化学式)。
(4)滤渣3的成分是偏钒酸铵( )沉淀,煅烧偏钒酸铵(
)沉淀,煅烧偏钒酸铵( )还有氨气和水生成,写出“煅烧”过程中发生反应的化学方程式:
)还有氨气和水生成,写出“煅烧”过程中发生反应的化学方程式:_______ 。
(5) 时,取样进行实验分析,得到钒沉淀率和溶液
时,取样进行实验分析,得到钒沉淀率和溶液 之间关系如下表:
之间关系如下表:
结合上表,在实际生产中,加入氯化铵调节溶液的最佳 范围为
范围为_______ 。
 、
、 、
、 、
、 、
、 和
和 )中回收
)中回收 ,既避免污染环境又有利于资源综合利用,该工艺流程如下:
,既避免污染环境又有利于资源综合利用,该工艺流程如下:
已知:金属钒的氧化物能与酸反应;
 不溶于水也不溶于初中常见的酸。回答下列问题:
不溶于水也不溶于初中常见的酸。回答下列问题:(1)实验室进行操作I时,需要用到的玻璃仪器有漏斗、烧杯和
(2)加入
 的作用是将
的作用是将 转化为
转化为 ,则写出该转化过程中相关的离子方程式
,则写出该转化过程中相关的离子方程式(3)加入
 的作用之一是保证钒存在于溶液中时,把
的作用之一是保证钒存在于溶液中时,把 与
与 转化为沉淀,但
转化为沉淀,但 不宜过量,不然滤液2中引入
不宜过量,不然滤液2中引入 和
和(4)滤渣3的成分是偏钒酸铵(
 )沉淀,煅烧偏钒酸铵(
)沉淀,煅烧偏钒酸铵( )还有氨气和水生成,写出“煅烧”过程中发生反应的化学方程式:
)还有氨气和水生成,写出“煅烧”过程中发生反应的化学方程式:(5)
 时,取样进行实验分析,得到钒沉淀率和溶液
时,取样进行实验分析,得到钒沉淀率和溶液 之间关系如下表:
之间关系如下表: | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率/ | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
 范围为
范围为
您最近一年使用:0次
3 . 磁选后的炼铁高钛炉渣,主要成分有TiO2、SiO2、Al2O3、MgO、CaO以及少量的Fe2O3。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
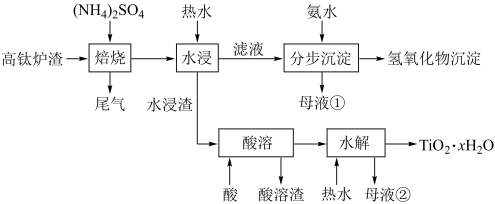
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表,回答下列问题:
(1)“焙烧”中,TiO2、SiO2几乎不发生反应,Al2O3、MgO、CaO、Fe2O3转化为相应的硫酸盐,Al2O3转化为NH4Al(SO4)2,写出向NH4Al(SO4)2中加入过量氨水的离子方程式:___________ 。
(2)pH约为2.0,在“分步沉淀时用氨水逐步调节pH至11.6,其中使Fe3+、Al3+完全沉淀的pH值范围:___________ 。
(3)根据表中信息,计算Mg(OH)2 的Ksp=___________ 。
(4)“水浸渣”在160℃ “酸溶”最适合的酸是___________ 。“酸溶渣”的成分是___________ 、___________ 。
(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO2·xH2O沉淀,该反应的离子方程式是:___________ 。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得___________ ,循环利用。

该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表,回答下列问题:
| 金属离子 | Fe3+ | Al3+ | Mg2+ | Ca2+ |
| 开始沉淀的pH | 2.2 | 3.5 | 9.5 | 12.4 |
| 沉淀完全(c=1.0×10-5mol·L-1)的pH | 3.2 | 4.7 | 11.0 | 13.8 |
(1)“焙烧”中,TiO2、SiO2几乎不发生反应,Al2O3、MgO、CaO、Fe2O3转化为相应的硫酸盐,Al2O3转化为NH4Al(SO4)2,写出向NH4Al(SO4)2中加入过量氨水的离子方程式:
(2)pH约为2.0,在“分步沉淀时用氨水逐步调节pH至11.6,其中使Fe3+、Al3+完全沉淀的pH值范围:
(3)根据表中信息,计算Mg(OH)2 的Ksp=
(4)“水浸渣”在160℃ “酸溶”最适合的酸是
(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO2·xH2O沉淀,该反应的离子方程式是:
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得
您最近一年使用:0次
2023-12-23更新
|
148次组卷
|
2卷引用:江西省宜春市宜丰中学2023-2024学年高一上学期1月期末化学试题
名校
4 . 某化学兴趣小组以含钴废渣(主要成分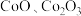 ,还含有
,还含有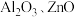 等杂质)为原料制备
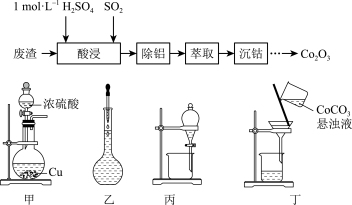
等杂质)为原料制备 的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
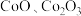 ,还含有
,还含有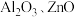 等杂质)为原料制备
等杂质)为原料制备 的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
A.将 固体放入蒸发血中灼烧制 固体放入蒸发血中灼烧制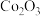 |
B.“酸浸”所需的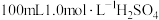 溶液用装置乙配制 溶液用装置乙配制 |
C.“萃取”的目的是除去 ,用装置丙,振荡时分液漏斗下口应倾斜向上 ,用装置丙,振荡时分液漏斗下口应倾斜向上 |
D.用装置甲制备“酸浸”所需的 ,“酸浸”时 ,“酸浸”时 为还原剂 为还原剂 |
您最近一年使用:0次
2023-12-18更新
|
302次组卷
|
3卷引用:江西省宜春市宜丰中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
5 . MnO2是重要化工原料,由软锰矿制备MnO2的一种工艺流程如下:

资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH:
③该工艺条件下,MnO2与H2SO4不反应。
(1)溶出
①溶出前,软锰矿需研磨,目的是___________ 。
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:
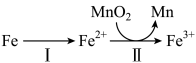
i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是___________ 。
ii.若I中Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2,而实际比值(0.9)小于2,原因是___________ 。
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2后加入NH3·H2O,调溶液pH,说明试剂加入顺序及调节pH的原因:___________ 。
(3)电解
Mn2+纯化液经电解得MnO2,生成1molMnO2电子转移的数目为___________ 。
(4)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,如热至充分反应,生成CO2,再滴加cmol/L KMnO4溶液至剩余Na2C2O4恰好完全反应,消耗KMnO4溶液的体积为dL,产品纯度为___________ (用质量分数表示)。[已知:MnO2及 均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]

资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH:
| Fe3+ | A13+ | Mn2+ | Fe2+ | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
(1)溶出
①溶出前,软锰矿需研磨,目的是
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:

i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是
ii.若I中Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2,而实际比值(0.9)小于2,原因是
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2后加入NH3·H2O,调溶液pH,说明试剂加入顺序及调节pH的原因:
(3)电解
Mn2+纯化液经电解得MnO2,生成1molMnO2电子转移的数目为
(4)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,如热至充分反应,生成CO2,再滴加cmol/L KMnO4溶液至剩余Na2C2O4恰好完全反应,消耗KMnO4溶液的体积为dL,产品纯度为
 均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
您最近一年使用:0次
2023-12-15更新
|
183次组卷
|
3卷引用:北京师范大学2023--2024学年附属实验中学高一上学期化学12月统练
名校
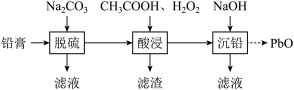
6 . 废旧铅蓄电池的铅膏中主要含有 、
、 。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法
。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法不正确 的是(已知常温下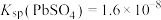 ,
,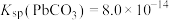 )
)
 、
、 。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法
。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法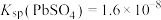 ,
,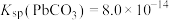 )
)
A.“铅膏”中 主要来源于该电池的正极材料 主要来源于该电池的正极材料 |
B.“脱硫”利用了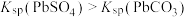 |
C.“酸浸”后溶液中的主要阳离子为 和 和 |
D.“沉铅”后的滤液中存在: |
您最近一年使用:0次
2023-12-13更新
|
180次组卷
|
2卷引用:四川省成都市第七中学2023-2024学年高一上学期12月月考化学试题
名校
7 . 硫酸锰是生产其他锰氧化物及锰盐产品的重要原料,由低品碳酸锰矿(主要成分是 ,含有少量
,含有少量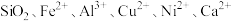 等)为原料制备高纯水合硫酸锰
等)为原料制备高纯水合硫酸锰 的流程如下:
的流程如下: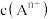 表示,
表示,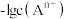 随溶液pH变化的图像如图所示:
随溶液pH变化的图像如图所示: 的电离平衡常数
的电离平衡常数 ;
;
③当离子浓度小于 可视为全部沉淀。
可视为全部沉淀。
(1)提高矿石浸出率的方法有_______ (写出两种);滤渣I的主要成分为_______ 。
(2)“氧化”时,主要发生反应的离子方程式为_______ 。
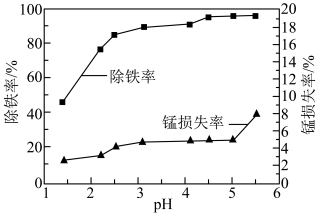
(3)下图为溶液pH对除铁的影响,则适合的pH为_______ ,此时Al3+是否沉淀完全?_______ (填字母)。
(4)向“除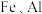 ”后的滤液中加入
”后的滤液中加入 溶液,使
溶液,使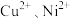 转化为沉淀除去,经过测定
转化为沉淀除去,经过测定 5.4效果最好。若溶液
5.4效果最好。若溶液 偏低,将会导致沉淀不完全,其原因是
偏低,将会导致沉淀不完全,其原因是_______ 。
(5)“系列操作”具体是指_______ 、过滤、洗涤、干燥。若所得晶体 不纯,应继续进行的提纯方法为
不纯,应继续进行的提纯方法为_______ 。
 ,含有少量
,含有少量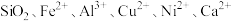 等)为原料制备高纯水合硫酸锰
等)为原料制备高纯水合硫酸锰 的流程如下:
的流程如下: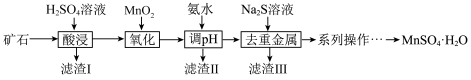
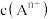 表示,
表示,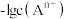 随溶液pH变化的图像如图所示:
随溶液pH变化的图像如图所示: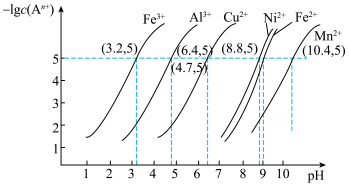
 的电离平衡常数
的电离平衡常数 ;
;③当离子浓度小于
 可视为全部沉淀。
可视为全部沉淀。(1)提高矿石浸出率的方法有
(2)“氧化”时,主要发生反应的离子方程式为
(3)下图为溶液pH对除铁的影响,则适合的pH为
(4)向“除
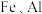 ”后的滤液中加入
”后的滤液中加入 溶液,使
溶液,使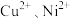 转化为沉淀除去,经过测定
转化为沉淀除去,经过测定 5.4效果最好。若溶液
5.4效果最好。若溶液 偏低,将会导致沉淀不完全,其原因是
偏低,将会导致沉淀不完全,其原因是(5)“系列操作”具体是指
 不纯,应继续进行的提纯方法为
不纯,应继续进行的提纯方法为
您最近一年使用:0次
2023-11-26更新
|
215次组卷
|
3卷引用:江西省宜春市宜丰中学2023-2024学年高一上学期12月月考化学试题
名校
8 . AlPO4的沉淀溶解平衡曲线如图所示(已知AlPO4溶解为吸热过程)。下列说法不正确的是
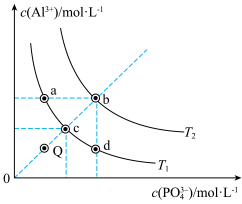

| A.T1>T2 | B.AlPO4在b点对应的溶解度大于c点 |
| C.T1下Q点溶液无AlPO4固体析出 | D.图中Ksp:a=c=d<b |
您最近一年使用:0次
2023-11-20更新
|
872次组卷
|
3卷引用:四川省成都市第七中学2023-2024学年高一上学期12月月考化学试题
9 . 实验室制备 的流程如图所示
的流程如图所示
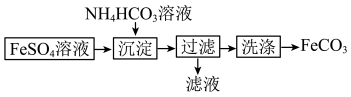
下列说法错误的是
 的流程如图所示
的流程如图所示
下列说法错误的是
A. 溶液保存时需加入Fe粉 溶液保存时需加入Fe粉 |
| B.过滤操作的常用玻璃仪器有烧杯、漏斗和玻璃棒 |
C.产品 在空气中高温分解可得到纯净的FeO 在空气中高温分解可得到纯净的FeO |
D. 溶液滴入几滴KSCN溶液,溶液不变红,说明 溶液滴入几滴KSCN溶液,溶液不变红,说明 溶液未变质 溶液未变质 |
您最近一年使用:0次
2023-11-14更新
|
634次组卷
|
3卷引用:陕西省西安交通大学附属中学2023-2024学年高一上学期期末考试化学试卷
陕西省西安交通大学附属中学2023-2024学年高一上学期期末考试化学试卷天津市部分区2023-2024学年高三上学期期中考试化学试题(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
名校
解题方法
10 . 下列离子方程式正确的是
A.石灰石与醋酸溶液的反应: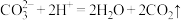 |
B.向澄清石灰水中加稀硫酸: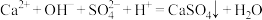 |
C. 溶液与足量 溶液与足量 溶液混合: 溶液混合: |
D.硫酸铜溶液遇到难溶的 转变为更难溶的 转变为更难溶的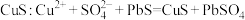 |
您最近一年使用:0次



