名校
解题方法
1 . 实验测得0.10
 溶液的pH随温度变化如图:
溶液的pH随温度变化如图:
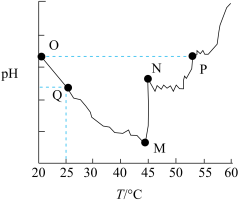
下列说法正确的是

 溶液的pH随温度变化如图:
溶液的pH随温度变化如图:
下列说法正确的是
A.OM段随温度升高溶液的pH减小,原因是 水解被抑制 水解被抑制 |
B.O点溶液和P点溶液中 相等 相等 |
| C.将N点溶液恢复到25℃,pH可能大于Q点 |
D.Q点、M点溶液中均有: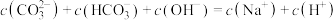 |
您最近一年使用:0次
名校
解题方法
2 . 某温度下重水中存在电离平衡D2O⇌D++OD-,D2O的离子积常数=1.0×10-12,若pD=-lgc(D+),该温度下有关分析不正确的是
| A.0.1 mol NaOD溶于重水制成1L溶液,pD=11 |
| B.将pD为4的DCl的重水溶液稀释10倍,所得溶液pD为5 |
| C.向30 mL 0.5mol•L-1NaOD的重水溶液中加入20 mL 0.5 mol•L-1DCl的重水溶液,所得溶液pD=10 |
| D.pD=10的NaOD的重水溶液中,由重水电离出的c(OD-)为1×10-10mol•L-1 |
您最近一年使用:0次
3 . 一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是
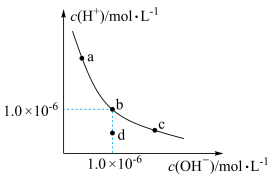

| A.升高温度,可能引起c向d的变化 |
| B.该温度下,水的离子积常数为1.0×10-13 |
| C.该温度下,a点时的溶液一定是一种酸的溶液 |
| D.该温度下,稀释溶液可能引起由c向b的变化 |
您最近一年使用:0次
名校
4 . I.水是一种很好的溶剂,也是物质发生化学反应的主要介质。
(1)某温度下纯水中的 ,则此时溶液中的
,则此时溶液中的
___________  。
。
A.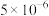 B.
B.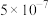 C.
C.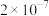 D.
D.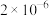
在该温度下,0.04 的NaOH溶液的pH=
的NaOH溶液的pH=___________ 。
(2)该温度下,某溶液中由水电离产生的 和
和 的乘积为
的乘积为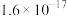 ,则该溶液的pH=
,则该溶液的pH=___________ 。
Ⅱ.室温下,在1 的某二元酸H2A溶液中,含A元素。组分的物质的量分数随pH变化的关系如图所示。
的某二元酸H2A溶液中,含A元素。组分的物质的量分数随pH变化的关系如图所示。

(3)写出H2A的电离方程式___________ 。
(4)根据图像,计算室温下HA-的电离平衡常数的数值Ka=___________ 。(写出计算过程)
(5)等物质的量浓度NaHA和Na2A溶液等体积混合,比较混合后的溶液中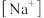 、
、 、
、 的大小正确的是___________。
的大小正确的是___________。
(1)某温度下纯水中的
 ,则此时溶液中的
,则此时溶液中的
 。
。A.
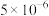 B.
B.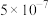 C.
C.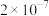 D.
D.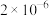
在该温度下,0.04
 的NaOH溶液的pH=
的NaOH溶液的pH=(2)该温度下,某溶液中由水电离产生的
 和
和 的乘积为
的乘积为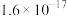 ,则该溶液的pH=
,则该溶液的pH=Ⅱ.室温下,在1
 的某二元酸H2A溶液中,含A元素。组分的物质的量分数随pH变化的关系如图所示。
的某二元酸H2A溶液中,含A元素。组分的物质的量分数随pH变化的关系如图所示。
(3)写出H2A的电离方程式
(4)根据图像,计算室温下HA-的电离平衡常数的数值Ka=
(5)等物质的量浓度NaHA和Na2A溶液等体积混合,比较混合后的溶液中
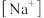 、
、 、
、 的大小正确的是___________。
的大小正确的是___________。A. | B. |
C.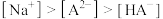 | D. |
您最近一年使用:0次
5 . 不同温度下水的离子积常数为Kw(25℃)=1.0×10﹣14,Kw(35℃)=2.1×10﹣14,则下列正确的是
| A.c(H+)随温度的升高而降低 |
| B.水的电离过程是吸热的 |
| C.水的离子积常数与浓度、温度有关 |
| D.在35℃时,c(H+)>c(OH﹣) |
您最近一年使用:0次
6 . 计算
(1)T℃时, ,当
,当 时,溶液的
时,溶液的
__________ (已知该温度下, )
)
(2)25℃时,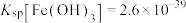 ,此温度下若在实验室中配制
,此温度下若在实验室中配制 溶液,为使配制过程中不出现浑浊现象,则至少需要加入
溶液,为使配制过程中不出现浑浊现象,则至少需要加入__________  的盐酸(忽略加入盐酸的体积)。
的盐酸(忽略加入盐酸的体积)。
(1)T℃时,
 ,当
,当 时,溶液的
时,溶液的
 )
)(2)25℃时,
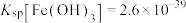 ,此温度下若在实验室中配制
,此温度下若在实验室中配制 溶液,为使配制过程中不出现浑浊现象,则至少需要加入
溶液,为使配制过程中不出现浑浊现象,则至少需要加入 的盐酸(忽略加入盐酸的体积)。
的盐酸(忽略加入盐酸的体积)。
您最近一年使用:0次
名校
解题方法
7 . 下列关于水的电离叙述正确的是
| A.温度升高,水中分子数减小 | B.水中 随温度升高而降低 随温度升高而降低 |
| C.水的pH随温度升高而升高 | D.水的电离过程是放热过程 |
您最近一年使用:0次
名校
8 . 常温下, 溶液加水稀释过程中,下列表达式的数据变大的是
溶液加水稀释过程中,下列表达式的数据变大的是
 溶液加水稀释过程中,下列表达式的数据变大的是
溶液加水稀释过程中,下列表达式的数据变大的是A. | B. | C.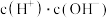 | D. |
您最近一年使用:0次
名校
解题方法
9 . 在不同温度下,水溶液中 与
与 有如图所示关系。下列关于离子共存说法中正确的是
有如图所示关系。下列关于离子共存说法中正确的是

 与
与 有如图所示关系。下列关于离子共存说法中正确的是
有如图所示关系。下列关于离子共存说法中正确的是
A.d点对应的溶液中可能大量存在: 、 、 、 、 、 、 |
B.b点对应的溶液中可能大量存在: 、 、 、 、 、 、 |
C.c点对应的溶液中可能大量存在: 、 、 、 、 、 、 |
D.a点对应的溶液中可能大量存在: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
10 . 水溶液中存在着各种各样的平衡,如弱电解质的电离、盐类水解等,它们的强度可以由对应的平衡常数K来衡量。
(1)已知Kw(298K)=1.0×10-14和Kw(308K)=2.1×10-14,下列有关纯水叙述正确的是_______。
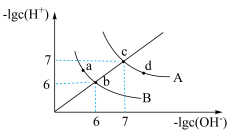
(2)已知水溶液在25℃与100℃时的电离平衡曲线如图所示,下列说法错误的是________。
(1)已知Kw(298K)=1.0×10-14和Kw(308K)=2.1×10-14,下列有关纯水叙述正确的是_______。
| A.308K时纯水pH<7 |
| B.298K时水的电离程度更大 |
| C.308K时c(H+)>c(OH-) |
| D.298K时向水中通入HCl(g),水的电离程度减小,Kw减小 |
(2)已知水溶液在25℃与100℃时的电离平衡曲线如图所示,下列说法错误的是________。

| A.曲线B为100℃时水溶液的电离平衡曲线 |
| B.只有纯水的电离符合直线bc |
| C.从b→a,水的电离可能被促进了 |
| D.从c→d,Kw不改变 |
您最近一年使用:0次



