解题方法
1 . 回答下列问题:
(1)常温下0.01mol/L HCl溶液:
①由水电离出的c(H+)=______ ;
②pH=______ ;
(2)现有常温下0.01mol/L NH4Cl溶液。
①你认为该溶液呈______ 性,原因是(用离子方程式表示):______ 。
②该溶液中离子浓度由大到小顺序为:______ 。
(3)已知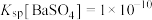 ,当溶液中
,当溶液中 时,
时, 约为
约为______  。
。
(1)常温下0.01mol/L HCl溶液:
①由水电离出的c(H+)=
②pH=
(2)现有常温下0.01mol/L NH4Cl溶液。
①你认为该溶液呈
②该溶液中离子浓度由大到小顺序为:
(3)已知
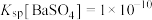 ,当溶液中
,当溶液中 时,
时, 约为
约为 。
。
您最近一年使用:0次
解题方法
2 . 室温下,下列各组离子在指定溶液中一定能大量共存的是
A.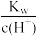 =1×10-13mol·L-1的溶液中K+、Na+、 =1×10-13mol·L-1的溶液中K+、Na+、 、 、 |
B.水电离的c(OH-)=1×10-13mol·L-1的溶液:Na+、 、Br-、Ba2+ 、Br-、Ba2+ |
C.pH=2的溶液: 、Cl-、Fe2+、 、Cl-、Fe2+、 |
D. =1012的溶液:Fe2+、Al3+、 =1012的溶液:Fe2+、Al3+、 、I- 、I- |
您最近一年使用:0次
解题方法
3 . 室温下,下列各组离子一定能大量共存的是
A.使甲基橙显红色的溶液中: 、 、 、 、 、 、 |
B. 的溶液: 的溶液: 、 、 、 、 、 、 |
C.水电离的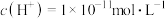 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.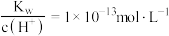 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
解题方法
4 . 电解质的水溶液跟日常生活、工农业生产和环境保护息息相关。完成下列问题:
(1)现有下列物质:① ;②酒精;③
;②酒精;③ 溶液;④
溶液;④ ;⑤冰醋酸;⑥熔融状态的
;⑤冰醋酸;⑥熔融状态的 。其中能导电的物质有
。其中能导电的物质有___________ (填序号)。
(2)用等物质的量浓度的盐酸和醋酸分别与NaOH进行中和反应反应热的测定,测得反应热的数值情况,盐酸___________ 醋酸(填“>”“<”或“=”),其原因是___________ 。
(3)已知25°C时, 的
的 ;
; 的:
的: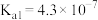
 ;HCN的
;HCN的 回答下列问题:
回答下列问题:
①25°C时,向NaCN溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为___________ 。
②用蒸馏水稀释 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是___________ 。
a. b.
b.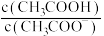 c.
c. d.电离度
d.电离度
③下列措施中能使醋酸的水溶液中 増大的同时
増大的同时 减小的是
减小的是___________ (填标号)。
A.加入 固体 B.加入固体
固体 B.加入固体 C.加入NaCN固体 D.升高温度
C.加入NaCN固体 D.升高温度
(4)常温时
 溶液,
溶液, 浓度为
浓度为___________ ,由水电离的 为
为___________ 。
(5)常温下, 的NaOH溶液与
的NaOH溶液与 的
的 溶液按体积比为1:9混合,所得溶液的pH值为
溶液按体积比为1:9混合,所得溶液的pH值为___________ 。(近似认为酸碱总体积就是混合液体积)
(6)化学中常用AG表示溶液的酸度 。室温下,向20.00mL 0.1000mol/L的氨水中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。
。室温下,向20.00mL 0.1000mol/L的氨水中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。
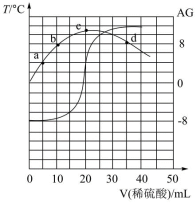
①根据图象可知,该稀硫酸的浓度为___________ 。
②恰好完全中和时AG___________ 0(填“>”、“<”或“=”)。
(1)现有下列物质:①
 ;②酒精;③
;②酒精;③ 溶液;④
溶液;④ ;⑤冰醋酸;⑥熔融状态的
;⑤冰醋酸;⑥熔融状态的 。其中能导电的物质有
。其中能导电的物质有(2)用等物质的量浓度的盐酸和醋酸分别与NaOH进行中和反应反应热的测定,测得反应热的数值情况,盐酸
(3)已知25°C时,
 的
的 ;
; 的:
的: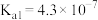
 ;HCN的
;HCN的 回答下列问题:
回答下列问题:①25°C时,向NaCN溶液中通入少量
 ,反应的离子方程式为
,反应的离子方程式为②用蒸馏水稀释
 的醋酸,下列各式表示的数值随水量的增加而增大的是
的醋酸,下列各式表示的数值随水量的增加而增大的是a.
 b.
b.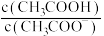 c.
c. d.电离度
d.电离度
③下列措施中能使醋酸的水溶液中
 増大的同时
増大的同时 减小的是
减小的是A.加入
 固体 B.加入固体
固体 B.加入固体 C.加入NaCN固体 D.升高温度
C.加入NaCN固体 D.升高温度(4)常温时

 溶液,
溶液, 浓度为
浓度为 为
为(5)常温下,
 的NaOH溶液与
的NaOH溶液与 的
的 溶液按体积比为1:9混合,所得溶液的pH值为
溶液按体积比为1:9混合,所得溶液的pH值为(6)化学中常用AG表示溶液的酸度
 。室温下,向20.00mL 0.1000mol/L的氨水中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。
。室温下,向20.00mL 0.1000mol/L的氨水中滴加未知浓度的稀硫酸溶液,混合溶液的温度与酸度AG随加入稀硫酸体积的变化如图所示。
①根据图象可知,该稀硫酸的浓度为
②恰好完全中和时AG
您最近一年使用:0次
5 . 已知水在25°C和100°C时,其电离平衡曲线如图所示,下列说法正确的
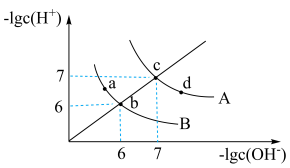

| A.b点溶液呈酸性 |
B.d点溶液中可大量存在 、 、 、 、 、 、 |
| C.B曲线对应的温度下,溶液中水的电离度:b点>a点 |
| D.A曲线对应的温度下,向纯水中加入少量金属Na,可使c点溶液变为d点溶液 |
您最近一年使用:0次
解题方法
6 . Ⅰ、
(1)室温下,试计算:
①pH=4的亚硫酸溶液中,c(H+)H2O=___________ 。
②pH=2的盐酸加水稀释到1000倍,溶液的pH=___________ 。
Ⅱ、某温度下的水溶液中,c(H+)=10-xmol·L-1,c(OH-)=10-ymol·L-1。x与y的关系如图所示:

(2)该温度下水的离子积为___________ (填具体数值);该温度___________ (填“高于”“低于”或“等于”)常温。
(3)该温度下0.01mol·L-1NaOH溶液的pH为___________ 。
(4)除了用pH外,科学家还建议用酸度(AG)来表示溶液的酸碱性:AG=lg 。则该温度下,0.01mol·L-1盐酸的酸度AG=
。则该温度下,0.01mol·L-1盐酸的酸度AG=___________ 。
(1)室温下,试计算:
①pH=4的亚硫酸溶液中,c(H+)H2O=
②pH=2的盐酸加水稀释到1000倍,溶液的pH=
Ⅱ、某温度下的水溶液中,c(H+)=10-xmol·L-1,c(OH-)=10-ymol·L-1。x与y的关系如图所示:

(2)该温度下水的离子积为
(3)该温度下0.01mol·L-1NaOH溶液的pH为
(4)除了用pH外,科学家还建议用酸度(AG)来表示溶液的酸碱性:AG=lg
 。则该温度下,0.01mol·L-1盐酸的酸度AG=
。则该温度下,0.01mol·L-1盐酸的酸度AG=
您最近一年使用:0次
7 . I.现有下列物质:①100℃的纯水②25℃0.1mol•L-1HCl溶液③25℃0.01mol•L-1Ba(OH)2溶液。
(1)这些物质与25℃纯水相比,能抑制水电离的是_______ (填序号,下同),③中水电离的c(OH-)是______ mol•L-1。
II.水的电离平衡曲线如图所示。

(2)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升高到100℃时,水的电离平衡状态到B点,则此时水的离子积从_______ 增加到_______ 。
(3)25℃时,pH=13的强碱溶液与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱溶液与强酸溶液的体积比是_______ 。
(4)100℃时,纯水中的c(H+)=_______ mol•L-1,这种水显_______ (填“酸”“碱”或“中”)性;若温度不变,滴入稀盐酸使c(H+)=5.0×10-6mol•L-1,则c(OH-)=_______ mol•L-1。
(1)这些物质与25℃纯水相比,能抑制水电离的是
II.水的电离平衡曲线如图所示。

(2)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升高到100℃时,水的电离平衡状态到B点,则此时水的离子积从
(3)25℃时,pH=13的强碱溶液与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱溶液与强酸溶液的体积比是
(4)100℃时,纯水中的c(H+)=
您最近一年使用:0次
解题方法
8 . 常温下,下列各组离子在指定条件下能大量共存的是
A.澄清透明的溶液中:Fe3+、 K+ 、SO 、Cl- 、Cl- |
B.使甲基橙变红色的溶液中:K+、Na+、HCO 、Cl- 、Cl- |
C. 的溶液中:K+、Na+、MnO 的溶液中:K+、Na+、MnO 、Cl- 、Cl- |
D.水电离出的 的溶液中:NH 的溶液中:NH 、Na+、S2-、Br- 、Na+、S2-、Br- |
您最近一年使用:0次
名校
解题方法
9 . 下列说法中正确 的是
| A.配制FeSO4溶液时,加入稀HNO3抑制Fe2+水解 |
| B.-10 ℃的液态水就会自动结冰成为固态,因为这是熵增的过程 |
| C.将纯水加热的过程中,Kw变大、pH变小 |
D.向0.1 mol/L氨水中加入少量水,溶液中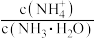 减小 减小 |
您最近一年使用:0次
名校
解题方法
10 . 常温时,下列叙述正确的是
| A.若1mLpH=1的盐酸与100mLNaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11 |
| B.醋酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则b=a+1 |
C. 盐酸的 盐酸的 , , 盐酸的 盐酸的 |
| D.在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
您最近一年使用:0次



