1 . 乙酸是典型的有机酸,在生产、生活中有广泛的应用。
(1)能证明 是弱酸的事实是
是弱酸的事实是___________ 。
A. 易挥发
易挥发
B.常温下, 溶液的
溶液的 大于7
大于7
C.醋酸不易腐蚀衣服
D. 的
的 溶液稀释10倍,溶液
溶液稀释10倍,溶液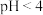
E.等体积等浓度的 溶液和盐酸,分别与足量镁粉反应,产生氢气一样多
溶液和盐酸,分别与足量镁粉反应,产生氢气一样多
F.将一定量的 溶液加入
溶液加入 溶液中,有气泡产生
溶液中,有气泡产生
(2) 时,
时, 溶液的
溶液的 ,则该温度下,水的离子积
,则该温度下,水的离子积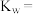
___________  ;该温度下,将
;该温度下,将 之和为13的
之和为13的 溶液和
溶液和 溶液等体积混合,所得溶液呈
溶液等体积混合,所得溶液呈___________ (填“酸”、“碱”或“中”)性。
(3)利用电催化还原 制备
制备 的装置如图所示。
的装置如图所示。___________ (填“正极”或“负极”);阴极的电极反应式为___________ 。
(4)常温下, 。
。
① 溶液中离子浓度大小关系为
溶液中离子浓度大小关系为___________ 。
②常温下,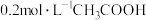 溶液和
溶液和 溶液等体积混合,所得混合溶液的
溶液等体积混合,所得混合溶液的
___________ 7(填“>”“<”或“=”)。
③某二元弱酸 的电离常数:
的电离常数: 。计算反应
。计算反应 的平衡常数为
的平衡常数为___________ (保留小数点后1位),由此说明该反应___________ (填“能发生”或“不能发生”)。
(1)能证明
 是弱酸的事实是
是弱酸的事实是A.
 易挥发
易挥发B.常温下,
 溶液的
溶液的 大于7
大于7C.醋酸不易腐蚀衣服
D.
 的
的 溶液稀释10倍,溶液
溶液稀释10倍,溶液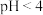
E.等体积等浓度的
 溶液和盐酸,分别与足量镁粉反应,产生氢气一样多
溶液和盐酸,分别与足量镁粉反应,产生氢气一样多F.将一定量的
 溶液加入
溶液加入 溶液中,有气泡产生
溶液中,有气泡产生(2)
 时,
时, 溶液的
溶液的 ,则该温度下,水的离子积
,则该温度下,水的离子积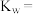
 ;该温度下,将
;该温度下,将 之和为13的
之和为13的 溶液和
溶液和 溶液等体积混合,所得溶液呈
溶液等体积混合,所得溶液呈(3)利用电催化还原
 制备
制备 的装置如图所示。
的装置如图所示。
(4)常温下,
 。
。①
 溶液中离子浓度大小关系为
溶液中离子浓度大小关系为②常温下,
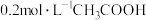 溶液和
溶液和 溶液等体积混合,所得混合溶液的
溶液等体积混合,所得混合溶液的
③某二元弱酸
 的电离常数:
的电离常数: 。计算反应
。计算反应 的平衡常数为
的平衡常数为
您最近一年使用:0次
解题方法
2 . 设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.1mol冰晶体中所含氢键的数目为 |
B.56g聚乙烯中含有碳碳双键的数目为 |
C.某温度下 , , 的NaOH溶液中 的NaOH溶液中 数目为 数目为 |
D.1mol基态碳原子中未成对电子的数目为 |
您最近一年使用:0次
解题方法
3 . 下列有关电解质溶液的说法中正确的是
| A.在100℃时,pH约为6的纯水呈酸性 |
B.将1mL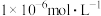 盐酸稀释到1000mL,所得溶液pH为9 盐酸稀释到1000mL,所得溶液pH为9 |
C.在常温下,当水电离出的 为 为 时,此溶液的pH可能为2或12 时,此溶液的pH可能为2或12 |
| D.将pH=12的氨水和氢氧化钠溶液各1mL稀释至100mL,所得氢氧化钠溶液pH略大 |
您最近一年使用:0次
解题方法
4 . 硫酸是中学阶段常见的强酸之一,对于常温下0.05 mol·L-1 H2SO4溶液。
(1)若将溶液升高温度到100 ℃,溶液中的c(OH-)=1×10-11 mol·L-1,则100 ℃时水的离子积是___________ 。
(2)常温下该溶液中硫酸电离出的c(H+)与H2O电离出的c(H+)之比为___________ 。
(3)将该溶液放入烧杯中滴入几滴酚酞,插入两个电极与直流电源连接形成闭合回路。
①向烧杯中逐滴加入同浓度的氢氧化钡溶液,灯泡逐渐变暗,后熄灭。该过程中发生反应的离子方程式为___________ 。
②向熄灭后的烧杯中再逐滴加入氢氧化钡溶液,观察到灯泡逐渐变亮,还观察到溶液颜色___________ ,此过程中水的电离程度___________ (填“增大”“减小”或“不确定”)。
(4)将该H2SO4溶液加水稀释,水的电离平衡___________ (填“向左”“向右”或“不”)移动。向水中滴加几滴稀硫酸,水的电离平衡___________ (填“向左”“向右”或“不”)移动。
(5)常温下0.05 mol·L-1 H2SO4溶液的pH为___________ ;0.06mol·L-1的氢氧化钡溶液中H+浓度约为___________ mol·L-1;将两溶液等体积混合后,混合溶液的pH为___________ 。
(1)若将溶液升高温度到100 ℃,溶液中的c(OH-)=1×10-11 mol·L-1,则100 ℃时水的离子积是
(2)常温下该溶液中硫酸电离出的c(H+)与H2O电离出的c(H+)之比为
(3)将该溶液放入烧杯中滴入几滴酚酞,插入两个电极与直流电源连接形成闭合回路。
①向烧杯中逐滴加入同浓度的氢氧化钡溶液,灯泡逐渐变暗,后熄灭。该过程中发生反应的离子方程式为
②向熄灭后的烧杯中再逐滴加入氢氧化钡溶液,观察到灯泡逐渐变亮,还观察到溶液颜色
(4)将该H2SO4溶液加水稀释,水的电离平衡
(5)常温下0.05 mol·L-1 H2SO4溶液的pH为
您最近一年使用:0次
解题方法
5 . 室温时,分别以HCl气体或NaOH固体粉末调节H2R溶液的pH,配制一组c(H2R)+c(HR-)+c(R2-)=0.10 mol/L的混合溶液(操作过程中溶液的体积不变),溶液中H2R、HR-、R2-的分布分数 [如
[如 ]随pH的变化如图所示。下列说法错误的是
]随pH的变化如图所示。下列说法错误的是

 [如
[如 ]随pH的变化如图所示。下列说法错误的是
]随pH的变化如图所示。下列说法错误的是
| A.室温时,H2R的Ka1=10-1.8 |
B.pH从 时, 时, 始终减小 始终减小 |
| C.室温下,Na2R的溶液中,水电离出的c(H+)·c(OH-)>10-14 |
| D.c(Na+)=0.10 mol/L时,c(HR-)>c(H2R)>c(R2-) |
您最近一年使用:0次
6 . 类别万千的酸碱溶液共同构筑了化学世界的丰富多彩。
(1)现有常温下pH=2的盐酸(甲)、pH=2的醋酸溶液(乙)和0.1mo1/L (丙),请根据下列操作回答:
(丙),请根据下列操作回答:
①常温下,将丙溶液加水稀释,下列数值一定变小的是___________ (填字母)。
A. B.
B. C.
C. D.
D.
②常温下,取甲、乙各1mL分别稀释至100mL,稀释后,水的电离程度:乙___________ 甲(填“>”“<”或“=”)。
(2)①某温度时,测得0.01mol/L NaOH溶液pH为11,则该温度___________ 25℃。(填“>”“<”或“=”)
②相同条件下,取等体积、等pH的 、NaOH和
、NaOH和 三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 、
、 、
、 ,则三者的由大到小关系为
,则三者的由大到小关系为___________ 。
③某温度下,水的离子积常数 ,将
,将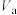 L pH=4的HCl溶液和
L pH=4的HCl溶液和 L pH=9的
L pH=9的 溶液混合均匀,测得溶液的pH=7,则
溶液混合均匀,测得溶液的pH=7,则
___________ 。
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
①将 通入氨水中,当
通入氨水中,当 降至
降至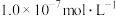 时,溶液中的
时,溶液中的
___________ 。
②下列微粒在溶液中不能大量共存的是___________ 。
A. 、
、 B.
B. 、
、 C.
C. 、
、 D.HClO、
D.HClO、
(1)现有常温下pH=2的盐酸(甲)、pH=2的醋酸溶液(乙)和0.1mo1/L
 (丙),请根据下列操作回答:
(丙),请根据下列操作回答:①常温下,将丙溶液加水稀释,下列数值一定变小的是
A.
 B.
B. C.
C. D.
D.
②常温下,取甲、乙各1mL分别稀释至100mL,稀释后,水的电离程度:乙
(2)①某温度时,测得0.01mol/L NaOH溶液pH为11,则该温度
②相同条件下,取等体积、等pH的
 、NaOH和
、NaOH和 三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 、
、 、
、 ,则三者的由大到小关系为
,则三者的由大到小关系为③某温度下,水的离子积常数
 ,将
,将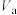 L pH=4的HCl溶液和
L pH=4的HCl溶液和 L pH=9的
L pH=9的 溶液混合均匀,测得溶液的pH=7,则
溶液混合均匀,测得溶液的pH=7,则
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表有下表:
| 弱电解质 |  |  | HClO |  |
| 电离平衡常数 |   |   | 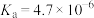 |  |
 通入氨水中,当
通入氨水中,当 降至
降至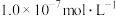 时,溶液中的
时,溶液中的
②下列微粒在溶液中不能大量共存的是
A.
 、
、 B.
B. 、
、 C.
C. 、
、 D.HClO、
D.HClO、
您最近一年使用:0次
名校
7 . 某温度下,由H2CO3与HCl或NaOH配制一组总含碳微粒浓度为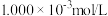 的混合溶液,混合体系中部分物种的浓度的负对数
的混合溶液,混合体系中部分物种的浓度的负对数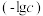 与pH关系如图所示。下列说法错误的是
与pH关系如图所示。下列说法错误的是

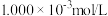 的混合溶液,混合体系中部分物种的浓度的负对数
的混合溶液,混合体系中部分物种的浓度的负对数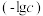 与pH关系如图所示。下列说法错误的是
与pH关系如图所示。下列说法错误的是
A.该溶液的温度为 |
B. 时,混合体系中浓度最高的含碳物种为 时,混合体系中浓度最高的含碳物种为 |
C.该条件下,H2CO3的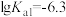 |
D. 的溶液中: 的溶液中: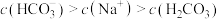 |
您最近一年使用:0次
2024-03-01更新
|
188次组卷
|
3卷引用:河南省沁阳一中2023—2024学年高二下学期开学考试 化学试卷
名校
8 . 常温下,下列各组离子一定能大量共存的是
A.由水电离出的c(H+)=1×10-11 mol/L的溶液中:Mg2+、 、 、 、 、 |
B.在含大量Fe3+的溶液中: 、Na+、Cl-、SCN-、 、Na+、Cl-、SCN-、 |
C.与Al反应能放出H2溶液中: 、Ba2+、Cl-、 、Ba2+、Cl-、 |
D.在Kw/c(H+)=1×10-12 mol/L的溶液中:Na+、K+、Br-、 |
您最近一年使用:0次
9 . 查阅资料获得25℃时部分弱电解质的电离平衡常数数据:
回答下列问题:
(1) 的电离方程式为
的电离方程式为___________ 。
(2)物质的量浓度相同的HF、HClO、 、
、 中,
中, 由大到小的顺序是
由大到小的顺序是___________ 。
(3)常温下, 的氨水的pH约为
的氨水的pH约为___________ ( )。
)。
(4)常温下, 的水溶液的pH
的水溶液的pH___________ 7(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(5)常温下,在 的
的 溶液中,水电离出来的
溶液中,水电离出来的 为
为___________  。
。
| 化学式 | HF | HClO |  |  |  |
| 电离常数 | 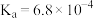 | 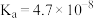 | 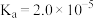 | 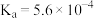 | 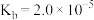 |
(1)
 的电离方程式为
的电离方程式为(2)物质的量浓度相同的HF、HClO、
 、
、 中,
中, 由大到小的顺序是
由大到小的顺序是(3)常温下,
 的氨水的pH约为
的氨水的pH约为 )。
)。(4)常温下,
 的水溶液的pH
的水溶液的pH ”、“
”、“ ”或“
”或“ ”)。
”)。(5)常温下,在
 的
的 溶液中,水电离出来的
溶液中,水电离出来的 为
为 。
。
您最近一年使用:0次
名校
10 . K、 、
、 分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是
分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是
 、
、 分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是
分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是A.25℃时,pH均为4的盐酸和 溶液中 溶液中 不相等 不相等 |
| B.在500℃时,在5L密闭容器中进行合成氨的反应,使用催化剂后K增大 |
C.相同温度下 ,说明酸性: ,说明酸性: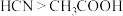 |
D. 达平衡后,改变某一条件时K不变, 达平衡后,改变某一条件时K不变, 的转化率可能增大 的转化率可能增大 |
您最近一年使用:0次



