1 . 常温下,往 溶液中滴入
溶液中滴入 溶液,溶液中由水电离出的
溶液,溶液中由水电离出的 的负对数
的负对数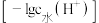 与所加
与所加 溶液体积的关系如图所示,下列说法错误的是
溶液体积的关系如图所示,下列说法错误的是 。
。
 溶液中滴入
溶液中滴入 溶液,溶液中由水电离出的
溶液,溶液中由水电离出的 的负对数
的负对数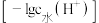 与所加
与所加 溶液体积的关系如图所示,下列说法错误的是
溶液体积的关系如图所示,下列说法错误的是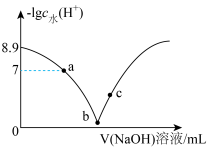
 。
。A.a点溶液中, |
B.b点溶液中, |
C.c点溶液中,由水电离出的 和由水电离出的 和由水电离出的 的乘积为 的乘积为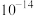 |
D.往碳酸钠溶液中加入足量的 溶液,一定无气泡产生 溶液,一定无气泡产生 |
您最近一年使用:0次
解题方法
2 . 回答下列问题:
(1)已知25℃时,10mL0.1mol/LHCl与10mL0.2mol/LNaOH混合,该混合溶液的pH值为_______ 。(lg2=0.3)
(2)常温下,将1mLpH=1的H2SO4溶液加水稀释到100mL,稀释后的溶液中pH值为_______ 。
(3)某温度时,测得0.01mol•L-1的NaOH溶液的pH为11,则该温度下水的离子积常数Kw=______ ,该温度_______ (填“高于”或“低于”)25℃;在该温度下将pH=a的NaOH溶液VaL与pH=b的硫酸VbL混合,若所得混合液为中性,且a=12、b=2,则Va:Vb=______ 。
(4)写出碱性电解质溶液中甲烷燃料电池负极上发生的电极反应式是_______ 。
(1)已知25℃时,10mL0.1mol/LHCl与10mL0.2mol/LNaOH混合,该混合溶液的pH值为
(2)常温下,将1mLpH=1的H2SO4溶液加水稀释到100mL,稀释后的溶液中pH值为
(3)某温度时,测得0.01mol•L-1的NaOH溶液的pH为11,则该温度下水的离子积常数Kw=
(4)写出碱性电解质溶液中甲烷燃料电池负极上发生的电极反应式是
您最近一年使用:0次
解题方法
3 . 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.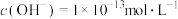 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.使甲基橙呈红色的溶液: 、 、 、 、 、 、 |
C. 的溶液: 的溶液: 、 、 、 、 、 、 |
D.无色透明的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
4 . 常温下,下列叙述正确的是
A. 的 的 溶液中由水电离的 溶液中由水电离的 |
B.将 的盐酸稀释1000倍后,溶液的 的盐酸稀释1000倍后,溶液的 |
C.将 的强碱溶液与 的强碱溶液与 的强酸溶液混合,若所得混合液的 的强酸溶液混合,若所得混合液的 ,则强碱与强酸的体积比是 ,则强碱与强酸的体积比是 |
D.向 的醋酸中逐滴滴加氢氧化钠溶液,当由水电离的 的醋酸中逐滴滴加氢氧化钠溶液,当由水电离的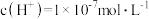 时,溶液可能呈中性也可能呈碱性 时,溶液可能呈中性也可能呈碱性 |
您最近一年使用:0次
5 . 实验测得 溶液、
溶液、 溶液以及
溶液以及 的
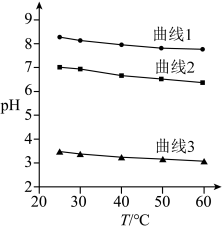
的 随温度变化的曲线如图所示。下列说法错误的是
随温度变化的曲线如图所示。下列说法错误的是
 溶液、
溶液、 溶液以及
溶液以及 的
的 随温度变化的曲线如图所示。下列说法错误的是
随温度变化的曲线如图所示。下列说法错误的是
A.随温度升高,纯水中 增大 增大 |
B.随温度升高, 溶液的 溶液的 增大 增大 |
C.随温度升高, 溶液的 溶液的 变化是 变化是 改变与水解平衡移动共同作用的结果 改变与水解平衡移动共同作用的结果 |
D.随温度升高,曲线1和曲线3的 均降低是因为水解平衡移动方向不同 均降低是因为水解平衡移动方向不同 |
您最近一年使用:0次
6 . 测定 溶液先升温再降温过程中的pH,数据如下表:
溶液先升温再降温过程中的pH,数据如下表:
实验过程中,取①、④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。下列说法错误的是
 溶液先升温再降温过程中的pH,数据如下表:
溶液先升温再降温过程中的pH,数据如下表:| 时刻 | ① | ② | ③ | ④ |
| 温度/℃ | 25 | 30 | 40 | 25 |
| pH | 9.66 | 9.52 | 9.37 | 9.2 |
A.①与④的 值相等 值相等 |
B.④产生的白色沉淀是 |
C.④的pH与①不同,是由于 浓度减小造成的 浓度减小造成的 |
D.①→③的过程中,温度对水解平衡的影响比 的影响更大 的影响更大 |
您最近一年使用:0次
名校
解题方法
7 . 已知25℃时,三种酸的电离平衡常数:
回答下列问题:
(1)下列方法中,可以使0.10mol•L-1CH3COOH溶液中CH3COOH电离程度增大的是______ 。
a.通入少量HCl气体
b.加入少量冰醋酸
c.加入少量醋酸钠固体
d.加入少量水
(2)下列反应不能发生的是______(填序号)。
(3)某温度时,某水溶液中的 ,
, ,x和y的关系如图所示:
,x和y的关系如图所示:

①该温度下,若盐酸中 ,则由水电离产生的
,则由水电离产生的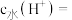
______  。
。
②该温度下,将pH=a的 溶液
溶液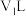 与
与 的
的 溶液
溶液 混合(忽略体积变化)。若所得混合溶液呈中性,且a=12,b=3,则
混合(忽略体积变化)。若所得混合溶液呈中性,且a=12,b=3,则
______ 。
| 化学式 |  |  |  |
| 电离平衡常数 |  |   |  |
(1)下列方法中,可以使0.10mol•L-1CH3COOH溶液中CH3COOH电离程度增大的是
a.通入少量HCl气体
b.加入少量冰醋酸
c.加入少量醋酸钠固体
d.加入少量水
(2)下列反应不能发生的是______(填序号)。
A. |
B.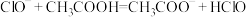 |
C. |
D. |
 ,
, ,x和y的关系如图所示:
,x和y的关系如图所示:
①该温度下,若盐酸中
 ,则由水电离产生的
,则由水电离产生的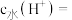
 。
。②该温度下,将pH=a的
 溶液
溶液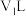 与
与 的
的 溶液
溶液 混合(忽略体积变化)。若所得混合溶液呈中性,且a=12,b=3,则
混合(忽略体积变化)。若所得混合溶液呈中性,且a=12,b=3,则
您最近一年使用:0次
解题方法
8 . 常温下,① 的硫酸溶液,②0.0001mol/L的醋酸,③溶液中的
的硫酸溶液,②0.0001mol/L的醋酸,③溶液中的 ,④
,④ ,则此四种溶液的酸性由强到弱的顺序为
,则此四种溶液的酸性由强到弱的顺序为
 的硫酸溶液,②0.0001mol/L的醋酸,③溶液中的
的硫酸溶液,②0.0001mol/L的醋酸,③溶液中的 ,④
,④ ,则此四种溶液的酸性由强到弱的顺序为
,则此四种溶液的酸性由强到弱的顺序为| A.①③④② | B.④①③② | C.④③①② | D.①④③② |
您最近一年使用:0次
名校
解题方法
9 . 水溶液广泛存在于生命体及其赖以生存的环境中。其中,弱电解质的电离平衡和盐类的水解平衡都与生命活动、工农业生产息息相关。请回答下列问题:
(1)某温度下,纯水中的c(H+)=4.0×10-7mol·L-1,此时c(OH-)=______ mol·L-1,这种水显_____ (填“酸”“碱”或“中”)性;若温度不变,向水中滴入稀盐酸,用pH试纸测得溶液的pH=3,则溶液中c(OH-)=___________ mol·L-1。
(2)25 ℃时,在等体积的①pH=1的H2SO4溶液、②0.5 mol·L-1的Ba(OH)2溶液、③pH=5的NH4Cl溶液中,发生电离的水的物质的量之比是___________ 。
(3)已知某二元酸H2A在水溶液中存在以下电离: H2A = H++HA-、HA- H++A2-,则0.1 mol·L-1 H2A溶液中所有离子浓度的大小顺序为
H++A2-,则0.1 mol·L-1 H2A溶液中所有离子浓度的大小顺序为___________ 。
(4)利用TiCl4的水解制备TiO2,反应的化学方程式为___________ ,制备时为使反应趋于完全,采取的措施是___________ ,所得的TiO2·xH2O经___________ 得到TiO2。
(1)某温度下,纯水中的c(H+)=4.0×10-7mol·L-1,此时c(OH-)=
(2)25 ℃时,在等体积的①pH=1的H2SO4溶液、②0.5 mol·L-1的Ba(OH)2溶液、③pH=5的NH4Cl溶液中,发生电离的水的物质的量之比是
(3)已知某二元酸H2A在水溶液中存在以下电离: H2A = H++HA-、HA-
 H++A2-,则0.1 mol·L-1 H2A溶液中所有离子浓度的大小顺序为
H++A2-,则0.1 mol·L-1 H2A溶液中所有离子浓度的大小顺序为(4)利用TiCl4的水解制备TiO2,反应的化学方程式为
您最近一年使用:0次
名校
解题方法
10 . 在25℃和100℃时,某溶液的pH和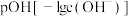 的关系如图所示。
的关系如图所示。
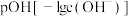 的关系如图所示。
的关系如图所示。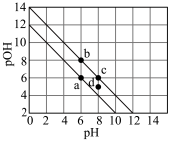
A.100℃时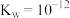 |
| B.c点对应溶液显碱性 |
| C.若将b点溶液稀释,可沿所在的线移到c点 |
| D.某温度下,d点对应的溶液可能是碱溶液或盐溶液 |
您最近一年使用:0次
2023-12-24更新
|
487次组卷
|
7卷引用:陕西省西安市第八十三中学2023-2024学年高二上学期12月月考化学试题



