回答下列问题:
(1)常温下0.01mol/L HCl溶液:
①由水电离出的c(H+)=______ ;
②pH=______ ;
(2)现有常温下0.01mol/L NH4Cl溶液。
①你认为该溶液呈______ 性,原因是(用离子方程式表示):______ 。
②该溶液中离子浓度由大到小顺序为:______ 。
(3)已知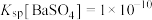 ,当溶液中
,当溶液中 时,
时, 约为
约为______  。
。
(1)常温下0.01mol/L HCl溶液:
①由水电离出的c(H+)=
②pH=
(2)现有常温下0.01mol/L NH4Cl溶液。
①你认为该溶液呈
②该溶液中离子浓度由大到小顺序为:
(3)已知
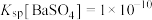 ,当溶液中
,当溶液中 时,
时, 约为
约为 。
。
更新时间:2024-05-03 17:29:43
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】溶液中的化学反应大多是离子反应。根据要求回答下列问题:
(1)Na2CO3溶液显碱性的原因,用离子反应方程式表示_____________________________ ;CuSO4溶液呈酸性的原因,用离子反应方程式表示:___________________________ 。
(2)25 ℃时,pH为9的CH3COONa溶液中c(OH-)=________ 。
(3)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显________ (填“酸”“碱”或“中”)性。用含a的代数式表示NH3·H2O的电离常数Kb=___________ 。
(1)Na2CO3溶液显碱性的原因,用离子反应方程式表示
(2)25 ℃时,pH为9的CH3COONa溶液中c(OH-)=
(3)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】电离平衡常数(Ka、Kb)、水的离子积常数(Kw)、盐的水解常数(Kh)、溶度积(Ksp)是电解质溶液中的四大平衡常数,对于我们分析溶液起到了很大的作用。
(1)某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合。
①若所得混合液为中性,则a∶b=________ 。
②若所得混合液pH=2,则a∶b=________ 。
(2)已知常温下Ka(HCN)=5×10-10,则常温下,含等物质的量浓度的HCN与NaCN的混合溶液中c(CN-)_____ c(HCN) (填“>”、“<”或“=”),其理由是__________ 。
(3)已知常温下二元酸发生电离:H2A=H++HA-;HA-⇌H++A2-(Ka=1×10﹣4),常温下pH=2的H2A溶液中c(A2-)与c(HA-)的浓度比为_____________ 。
(4)已知常温下H2C2O4的电离平衡常数为Ka1=5.9×10-2,Ka2=6.4×10-5。则常温下NaHC2O4溶液显_______ 性
学法题:电离平衡常数(Ka)、水的离子积常数(Kw)、盐的水解常数(Kh)之间有什么关系,请写出它们的关系式___________________________________
(5)已知25 ℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=4.9×10-13,Ksp(Ag2CrO4)=1.9×10-12。现用0.001 mol·L-1 AgNO3溶液滴定浓度均为0.001 mol·L-1 KCl、 K2CrO4、KBr的混合溶液,则Cl-、Br-、CrO 三种离子沉淀的先后顺序为
三种离子沉淀的先后顺序为__________ 。
(1)某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合。
①若所得混合液为中性,则a∶b=
②若所得混合液pH=2,则a∶b=
(2)已知常温下Ka(HCN)=5×10-10,则常温下,含等物质的量浓度的HCN与NaCN的混合溶液中c(CN-)
(3)已知常温下二元酸发生电离:H2A=H++HA-;HA-⇌H++A2-(Ka=1×10﹣4),常温下pH=2的H2A溶液中c(A2-)与c(HA-)的浓度比为
(4)已知常温下H2C2O4的电离平衡常数为Ka1=5.9×10-2,Ka2=6.4×10-5。则常温下NaHC2O4溶液显
学法题:电离平衡常数(Ka)、水的离子积常数(Kw)、盐的水解常数(Kh)之间有什么关系,请写出它们的关系式
(5)已知25 ℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=4.9×10-13,Ksp(Ag2CrO4)=1.9×10-12。现用0.001 mol·L-1 AgNO3溶液滴定浓度均为0.001 mol·L-1 KCl、 K2CrO4、KBr的混合溶液,则Cl-、Br-、CrO
 三种离子沉淀的先后顺序为
三种离子沉淀的先后顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据下列化合物:①NaOH,②H2SO4,③CH3COOH,④NaCl,⑤CH3COONa,⑥NH4Cl,⑦CH3COONH4,⑧NH4HSO4,⑨NH3·H2O,请回答下列问题:
(1)若浓度均为0.1mol·L-1、等体积的NaOH和NH3·H2O分别加水稀释m倍、n倍,
稀释后两种溶液的pH都变成9,则m_______ n (填“>”、“<”或“=”)。
(2)已知水存在如下平衡:H2O+H2O H3O++OH-△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是
H3O++OH-△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是_______ 。
A.向水中加入NaHSO4固体 B.向水中加NaHCO3固体
C.加热至100℃ [其中c (H+) =1×10-6mol·L-1] D.向水中加入NH4Cl固体
(3)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=_______ ;在pH=3的CH3COOH溶液中,水电离出来的c(H+)=_______ 。
(4)NH4Cl溶液中离子浓度大小顺序为______________ 。
(5)物质的量浓度相同的⑥、⑦、⑧、⑨四种稀溶液中,NH4+浓度由大到小的顺序是(填序号)_______ 。
(6)已知t℃时,Kw=1×10-12,在该温度时将pH=9的NaOH溶液a L与pH=2的H2SO4溶液bL混和(忽略混合后溶液体积的变化),若所得混合溶液的pH=3,则出a∶b=_______ 。
(1)若浓度均为0.1mol·L-1、等体积的NaOH和NH3·H2O分别加水稀释m倍、n倍,
稀释后两种溶液的pH都变成9,则m
(2)已知水存在如下平衡:H2O+H2O
 H3O++OH-△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是
H3O++OH-△H>0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是A.向水中加入NaHSO4固体 B.向水中加NaHCO3固体
C.加热至100℃ [其中c (H+) =1×10-6mol·L-1] D.向水中加入NH4Cl固体
(3)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=
(4)NH4Cl溶液中离子浓度大小顺序为
(5)物质的量浓度相同的⑥、⑦、⑧、⑨四种稀溶液中,NH4+浓度由大到小的顺序是(填序号)
(6)已知t℃时,Kw=1×10-12,在该温度时将pH=9的NaOH溶液a L与pH=2的H2SO4溶液bL混和(忽略混合后溶液体积的变化),若所得混合溶液的pH=3,则出a∶b=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知水在25℃和95℃时,其电离平衡曲线如图所示。

(1)25℃时水的电离平衡曲线应为______ (填“A”或“B”),请说明理由____________
(2)95℃时,若100体积 的某强酸溶液与1体积
的某强酸溶液与1体积 的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是__________ 。

(1)25℃时水的电离平衡曲线应为
(2)95℃时,若100体积
 的某强酸溶液与1体积
的某强酸溶液与1体积 的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中由水电离出的c(H+)=10-9 mol·L-1,则该电解质可能是_______ (填序号)。
A.CuSO4 B.Na2CO3 C.HCl D.NaOH E.K2SO4
(2)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性。
①c(OH-)=1.0×10-3 mol·L-1的氨水b L;
②浓度为1.0×10-3 mol·L-1的氨水c L;
③c(OH-)=1.0×10-3 mol·L-1的氢氧化钡溶液d L。
则a、b、c、d之间的关系是_______ 。
(3)已知室温时,0.1 mol·L-1的某一元酸HA在水中有0.1%发生电离,回答下列各问题:
①该溶液的pH=_______ 。
②升高温度时,K将_______ (填“增大”、“减小”或“不变”),pH将_______ (填“增大”、“减小”或“不变”)。
③由HA电离出的c(H+)约为水电离出的c(H+)的_______ 倍。
(4)某学生用0.1 mol/LKOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00 mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3 cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
①正确操作的顺序是_______ 。(用序号字母填写)
②上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是_______ (填“偏大”、“偏小”、“不变”)。判断到达终点的现象是_______ 。
(1)水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中由水电离出的c(H+)=10-9 mol·L-1,则该电解质可能是
A.CuSO4 B.Na2CO3 C.HCl D.NaOH E.K2SO4
(2)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性。
①c(OH-)=1.0×10-3 mol·L-1的氨水b L;
②浓度为1.0×10-3 mol·L-1的氨水c L;
③c(OH-)=1.0×10-3 mol·L-1的氢氧化钡溶液d L。
则a、b、c、d之间的关系是
(3)已知室温时,0.1 mol·L-1的某一元酸HA在水中有0.1%发生电离,回答下列各问题:
①该溶液的pH=
②升高温度时,K将
③由HA电离出的c(H+)约为水电离出的c(H+)的
(4)某学生用0.1 mol/LKOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00 mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3 cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
①正确操作的顺序是
②上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.
查阅资料可知,常温下,部分弱酸的电离平衡常数如表:
(1)相同物质的量浓度的NaClO、 、
、 碱性最强的是
碱性最强的是___________ (填化学式)
(2)由上可知 的酸性强于HClO,能否
的酸性强于HClO,能否___________ (填“能”或“否”)用 制取HClO。
制取HClO。
Ⅱ.已知 和
和 的水溶液中存在如下平衡:
的水溶液中存在如下平衡:
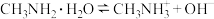 ,
,
 ,
,
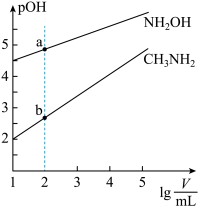
常温下,10mL浓度均为 的两种溶液,分别加水进行稀释,所得曲线如图所示[V表示溶液的体积,
的两种溶液,分别加水进行稀释,所得曲线如图所示[V表示溶液的体积,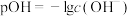 ],回答下列问题:
],回答下列问题:
(3)写出 水解的离子方程式
水解的离子方程式___________
(4)
___________ ,等物质的量浓度的 溶液与
溶液与 溶液比较,酸性较弱的是
溶液比较,酸性较弱的是___________ (填化学式)。
(5)a、b两点比较,溶液中水的电离程度较大的是___________ (填“a”或“b”)。
(6)常温下,浓度均为 的
的 与
与 的混合液显
的混合液显___________ (填“酸”、“碱”或“中”)性,写出溶液中除水之外的微粒浓度由大到小的顺序___________ 。
(7)常温下,若 溶液与bmol/LNaOH溶液等体积混合后溶液为中性,则c=
溶液与bmol/LNaOH溶液等体积混合后溶液为中性,则c=___________ (用含b的式子表示)。
查阅资料可知,常温下,部分弱酸的电离平衡常数如表:
| 弱酸 | HClO |  |  |
| 电离平衡常数(25℃) |  |   | 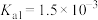 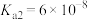 |
 、
、 碱性最强的是
碱性最强的是(2)由上可知
 的酸性强于HClO,能否
的酸性强于HClO,能否 制取HClO。
制取HClO。Ⅱ.已知
 和
和 的水溶液中存在如下平衡:
的水溶液中存在如下平衡: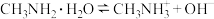 ,
,
 ,
,
常温下,10mL浓度均为
 的两种溶液,分别加水进行稀释,所得曲线如图所示[V表示溶液的体积,
的两种溶液,分别加水进行稀释,所得曲线如图所示[V表示溶液的体积,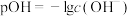 ],回答下列问题:
],回答下列问题:
(3)写出
 水解的离子方程式
水解的离子方程式(4)

 溶液与
溶液与 溶液比较,酸性较弱的是
溶液比较,酸性较弱的是(5)a、b两点比较,溶液中水的电离程度较大的是
(6)常温下,浓度均为
 的
的 与
与 的混合液显
的混合液显(7)常温下,若
 溶液与bmol/LNaOH溶液等体积混合后溶液为中性,则c=
溶液与bmol/LNaOH溶液等体积混合后溶液为中性,则c=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知25℃时电离常数:
(1)H2CO3、CH3COOH、HCN三种酸中酸性最弱的是_______ 。常温下,pH均为10的Na2CO3、CH3COONa、NaCN、NaHCO3四种溶液中,物质的量浓度最大的是_______ 。
(2)常温下,向20mL0.01mol·L-1CH3COOH溶液中逐滴加入0.01mol·L-1KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:
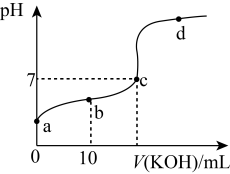
①若想观察滴定终点,滴定过程中宜选用_______ 作指示剂(填“酚酞”、“石蕊”或“甲基橙”)。
②b点时,溶液中离子浓度由大到小的顺序是_______ 。
(3)常温下,向NaCN溶液中通入少量 CO2发生反应的化学方程式为:_______ 。
(4)在一定条件下,Na2CO3溶液中存在CO +H2O
+H2O HCO
HCO +OH-平衡,下列说法不正确的是_______。
+OH-平衡,下列说法不正确的是_______。
| 酸 | H2CO3 | CH3COOH | HCN |
| Ka | Ka1=4.5×10-7Ka2=5.6×10-11 | 1.75×10-5 | 6.2×10-10 |
(2)常温下,向20mL0.01mol·L-1CH3COOH溶液中逐滴加入0.01mol·L-1KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:

①若想观察滴定终点,滴定过程中宜选用
②b点时,溶液中离子浓度由大到小的顺序是
(3)常温下,向NaCN溶液中通入
(4)在一定条件下,Na2CO3溶液中存在CO
 +H2O
+H2O HCO
HCO +OH-平衡,下列说法不正确的是_______。
+OH-平衡,下列说法不正确的是_______。A.稀释溶液,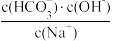 增大 增大 | B.通入CO2,溶液pH减小 |
| C.升高温度,水解平衡常数增大 | D.加入Na2O固体,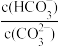 减小 减小 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)氨气的水溶液称为氨水,其中主要存在的溶质微粒是NH3·H2O。
已知: a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O。则CH3COONH4溶液呈__ (填“酸”“碱”或“中”,下同)性,NH4HCO3溶液呈__ 性,NH4HCO3溶液中物质的量浓度最大的离子是____ (填化学式)。
(2)99 ℃时,KW=1.0×10-12,该温度下测得0.1 mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为_______________ 。
②该温度下,将0.01 mol·L-1H2A溶液稀释到20倍后,溶液的pH=____ 。
③体积相等、pH均为1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气__ (填字母序号)。
A. 盐酸多 B.H2A多 C.一样多 D.无法确定
④将0.1 mol·L-1H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为______________________ 。
已知: a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O。则CH3COONH4溶液呈
(2)99 ℃时,KW=1.0×10-12,该温度下测得0.1 mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为
②该温度下,将0.01 mol·L-1H2A溶液稀释到20倍后,溶液的pH=
③体积相等、pH均为1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气
A. 盐酸多 B.H2A多 C.一样多 D.无法确定
④将0.1 mol·L-1H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】常温下,已知H2A的电离平衡常数为: K1=1.3×10-7 K2=7.1×10-15现有常温下的0.1mol/L NaHA溶液。
(1)请写出H2A的电离方程式______
(2)已知NaHA溶液pH>7,请解释原因_________
(3)请写出NaHA溶液中的电荷守恒式__________
(4)NaHA溶液中粒子之间的关系式中正确的是________
A.c(A2-)+c(HA-)=0.1mol/L B.c(H+)=c(OH-)+c(A2-)
C.c(HA-)>c(OH-)>c(A2-) D.c(A2-)>c(H2A)
(5)如果H2A为H2S,则向NaHS溶液中滴加硫酸铝溶液,发生反应的离子方程式________
(1)请写出H2A的电离方程式
(2)已知NaHA溶液pH>7,请解释原因
(3)请写出NaHA溶液中的电荷守恒式
(4)NaHA溶液中粒子之间的关系式中正确的是
A.c(A2-)+c(HA-)=0.1mol/L B.c(H+)=c(OH-)+c(A2-)
C.c(HA-)>c(OH-)>c(A2-) D.c(A2-)>c(H2A)
(5)如果H2A为H2S,则向NaHS溶液中滴加硫酸铝溶液,发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ.运用化学反应原理,研究硫、磷化合物的反应具有重要意义。
(1)已知 (次磷酸)的水溶液中存在
(次磷酸)的水溶液中存在 分子。
分子。 与足量
与足量 溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为
溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为_______ ,该盐属于_______ (填“正盐”或“酸式盐”)。 易被氧化为
易被氧化为 ,已知常温下
,已知常温下 的电离常数为
的电离常数为 ,
,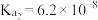 ,
, 请利用以上数据计算推测
请利用以上数据计算推测 溶液呈
溶液呈_______ 性。
(2)常温下,用 溶液吸收
溶液吸收 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡_______ (填“向左”“向右”或“不”)移动。试计算该溶液中
_______ (常温下, 的电离平衡常数
的电离平衡常数 )。
)。
(3)化工生产中常用 作沉淀剂除去工业废水中的
作沉淀剂除去工业废水中的 ,其反应原理为
,其反应原理为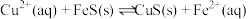 。下列有关叙述正确的是_______。
。下列有关叙述正确的是_______。
Ⅱ.在氯化铁溶液中存在平衡: 。回答下列问题:
。回答下列问题:
(4)加热 稀溶液,溶液颜色会不断加深,可得到一种红褐色透明液体,向这种液体中加入
稀溶液,溶液颜色会不断加深,可得到一种红褐色透明液体,向这种液体中加入 溶液,产生的现象为
溶液,产生的现象为_______ 。
(5)不断加热 溶液,蒸干水分并灼烧,最终得到的固体是
溶液,蒸干水分并灼烧,最终得到的固体是_______ (写化学式)。
(6)为防止配制 溶液时出现浑浊,正确操作是
溶液时出现浑浊,正确操作是_______ 。
(1)已知
 (次磷酸)的水溶液中存在
(次磷酸)的水溶液中存在 分子。
分子。 与足量
与足量 溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为
溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为 易被氧化为
易被氧化为 ,已知常温下
,已知常温下 的电离常数为
的电离常数为 ,
,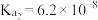 ,
, 请利用以上数据计算推测
请利用以上数据计算推测 溶液呈
溶液呈(2)常温下,用
 溶液吸收
溶液吸收 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡
 的电离平衡常数
的电离平衡常数 )。
)。(3)化工生产中常用
 作沉淀剂除去工业废水中的
作沉淀剂除去工业废水中的 ,其反应原理为
,其反应原理为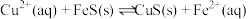 。下列有关叙述正确的是_______。
。下列有关叙述正确的是_______。A. |
B.达到平衡时 |
C.溶液中加入少量 固体后,溶液中 固体后,溶液中 都减小 都减小 |
D.该反应平衡常数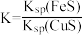 |
Ⅱ.在氯化铁溶液中存在平衡:
 。回答下列问题:
。回答下列问题:(4)加热
 稀溶液,溶液颜色会不断加深,可得到一种红褐色透明液体,向这种液体中加入
稀溶液,溶液颜色会不断加深,可得到一种红褐色透明液体,向这种液体中加入 溶液,产生的现象为
溶液,产生的现象为(5)不断加热
 溶液,蒸干水分并灼烧,最终得到的固体是
溶液,蒸干水分并灼烧,最终得到的固体是(6)为防止配制
 溶液时出现浑浊,正确操作是
溶液时出现浑浊,正确操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题
(1)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙做指示剂。请填写下列空白:
①用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化,直至当___________ 时,即确定达到滴定终点。
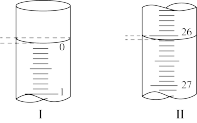
②若滴定开始和结束时,酸式滴定管中的液面如图所示所用盐酸溶液的体积为___________  。
。
(2) 两种温度下
两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题:
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题:
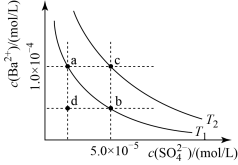
①
___________  (填“>”“<”“=”),
(填“>”“<”“=”), 时
时
___________ 。
②根据 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是___________ (填字母)。
A.加入 可由a点变为b点
可由a点变为b点
B.在 曲线下方区域(不含曲线)的任意一点时,均有
曲线下方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成
C.蒸发溶剂可能由d点变为 曲线上a、b之间的某一点(不含a、b)
曲线上a、b之间的某一点(不含a、b)
D.升温可由b点变为d点
(3)已知 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
①物质的量浓度均为 的四种溶液:
的四种溶液: 由小到大排列的顺序是
由小到大排列的顺序是___________ (用编号填写)
a. b.
b. c.
c.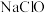 d.
d.
②常温下, 溶液加水稀释过程中,下列表达式的数据变大的是
溶液加水稀释过程中,下列表达式的数据变大的是___________ (填字母)。
A. B.
B. C.
C.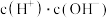 D.
D.
(4)已知 水溶液呈碱性。
水溶液呈碱性。
①用离子方程式表示该水溶液呈碱性的原因___________ 。
②在该水溶液中各离子浓度的大小关系是___________ 。
(5)下列4种混合溶液,分别由等体积 的两种溶液混合而成:①
的两种溶液混合而成:① 与
与 (混合溶液呈中性)②
(混合溶液呈中性)② 与
与 ③
③ 与
与 ④
④ 与
与 (混合溶液呈碱性)。
(混合溶液呈碱性)。 浓度由小到大排序(用序号填写)
浓度由小到大排序(用序号填写)___________ 。
(1)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙做指示剂。请填写下列空白:
①用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化,直至当
②若滴定开始和结束时,酸式滴定管中的液面如图所示所用盐酸溶液的体积为
 。
。
(2)
 两种温度下
两种温度下 在水中的沉淀溶解平衡曲线如图所示,请回答下列问题:
在水中的沉淀溶解平衡曲线如图所示,请回答下列问题:
①

 (填“>”“<”“=”),
(填“>”“<”“=”), 时
时
②根据
 温度时
温度时 的沉淀溶解平衡曲线,判断下列说法正确的是
的沉淀溶解平衡曲线,判断下列说法正确的是A.加入
 可由a点变为b点
可由a点变为b点B.在
 曲线下方区域(不含曲线)的任意一点时,均有
曲线下方区域(不含曲线)的任意一点时,均有 沉淀生成
沉淀生成C.蒸发溶剂可能由d点变为
 曲线上a、b之间的某一点(不含a、b)
曲线上a、b之间的某一点(不含a、b)D.升温可由b点变为d点
(3)已知
 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:| 化学式 |  |  |  |
| 电离平衡常数 |  | 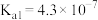  | 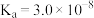 |
 的四种溶液:
的四种溶液: 由小到大排列的顺序是
由小到大排列的顺序是a.
 b.
b. c.
c.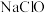 d.
d.
②常温下,
 溶液加水稀释过程中,下列表达式的数据变大的是
溶液加水稀释过程中,下列表达式的数据变大的是A.
 B.
B. C.
C.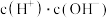 D.
D.
(4)已知
 水溶液呈碱性。
水溶液呈碱性。①用离子方程式表示该水溶液呈碱性的原因
②在该水溶液中各离子浓度的大小关系是
(5)下列4种混合溶液,分别由等体积
 的两种溶液混合而成:①
的两种溶液混合而成:① 与
与 (混合溶液呈中性)②
(混合溶液呈中性)② 与
与 ③
③ 与
与 ④
④ 与
与 (混合溶液呈碱性)。
(混合溶液呈碱性)。 浓度由小到大排序(用序号填写)
浓度由小到大排序(用序号填写)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】燃料的使用和防污染是社会发展中一个无法回避的矛盾话题,科技工作者在研究如何减少能源污染。
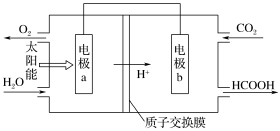
(1)如将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以 和
和 为原料制备
为原料制备 和
和 的原理示意图。电极a、b表面发生电极反应。其中b电极反应式为:
的原理示意图。电极a、b表面发生电极反应。其中b电极反应式为:___________ 。
(2)如果用100mL 1.5mol/L的 溶液吸收2.24L(标准状况)的二氧化碳气体所得溶液中各离子浓度由大到小的顺序为
溶液吸收2.24L(标准状况)的二氧化碳气体所得溶液中各离子浓度由大到小的顺序为___________ (用离子浓度符号表示)。
(3)燃料除硫中可用到 ,它是一种难溶物质,其
,它是一种难溶物质,其 。
。
①石灰石 石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙及鼓入的空气反应生成石膏(
石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙及鼓入的空气反应生成石膏( )。写出该反应的化学方程式:
)。写出该反应的化学方程式:___________ 。
②有一纯碱溶液的浓度为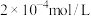 ,现将其与等体积的
,现将其与等体积的 溶液混合,则生成沉淀所需
溶液混合,则生成沉淀所需 溶液的最小浓度为
溶液的最小浓度为____ 。
(1)如将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以
 和
和 为原料制备
为原料制备 和
和 的原理示意图。电极a、b表面发生电极反应。其中b电极反应式为:
的原理示意图。电极a、b表面发生电极反应。其中b电极反应式为:
(2)如果用100mL 1.5mol/L的
 溶液吸收2.24L(标准状况)的二氧化碳气体所得溶液中各离子浓度由大到小的顺序为
溶液吸收2.24L(标准状况)的二氧化碳气体所得溶液中各离子浓度由大到小的顺序为(3)燃料除硫中可用到
 ,它是一种难溶物质,其
,它是一种难溶物质,其 。
。①石灰石
 石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙及鼓入的空气反应生成石膏(
石膏湿法烟气脱硫工艺技术的工作原理是烟气中的二氧化硫与浆液中的碳酸钙及鼓入的空气反应生成石膏( )。写出该反应的化学方程式:
)。写出该反应的化学方程式:②有一纯碱溶液的浓度为
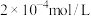 ,现将其与等体积的
,现将其与等体积的 溶液混合,则生成沉淀所需
溶液混合,则生成沉淀所需 溶液的最小浓度为
溶液的最小浓度为
您最近一年使用:0次



