名校
解题方法
1 . 某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选甲基橙作指示剂。
(1)配制250mL 0.2000 mol/L盐酸标准溶液,所需玻璃仪器有______ 、______ 量筒、烧杯、玻璃棒。
(2)盛装0.2000 mol/L盐酸标准液应该用______ 式滴定管。(填“酸”或“碱”)
(3)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视_________ ,直到加入一滴盐酸后,溶液由_________ ,即到终点。
(4)滴定操作可分解为如下几步:
①检查滴定管是否漏水;
②取一定体积的待测液于锥形瓶中;
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管;
④装标准溶液和待测液并调整液面(记录初始读数);
⑤用蒸馏水洗涤玻璃仪器;⑥滴定操作
正确的操作顺序为:_________ 。
(5)有关数据记录如下:
则NaOH溶液的物质的量浓度为__________ mol/L。
(6)若滴定时锥形瓶未干燥,则测定结果____________ ;若滴定前平视读数,滴定终点时仰视读数,则所测碱的浓度值_________ 。(填“无影响”、“偏高”或“偏低”)。
(1)配制250mL 0.2000 mol/L盐酸标准溶液,所需玻璃仪器有
(2)盛装0.2000 mol/L盐酸标准液应该用
(3)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视
(4)滴定操作可分解为如下几步:
①检查滴定管是否漏水;
②取一定体积的待测液于锥形瓶中;
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管;
④装标准溶液和待测液并调整液面(记录初始读数);
⑤用蒸馏水洗涤玻璃仪器;⑥滴定操作
正确的操作顺序为:
(5)有关数据记录如下:
| 实验序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.60 | 20.70 |
| 2 | 20.00 | 6.00 | 25.90 |
| 3 | 20.00 | 1.40 | 23.20 |
则NaOH溶液的物质的量浓度为
(6)若滴定时锥形瓶未干燥,则测定结果
您最近一年使用:0次
2020-06-06更新
|
108次组卷
|
2卷引用:云南省普洱市2017-2018学年高二下学期期末考试理科综合化学试题
名校
解题方法
2 . Ⅰ.下列有关实验操作中,合理的是_________ (选填字母)。
A.用托盘天平称取11.70g食盐
B.用量筒量取12.36ml盐酸
C.用酸式滴定管量取21.20ml0.10mol·L-1H2SO4溶液
D.用200ml容量瓶配制100ml0.1mol·L-1NaCl溶液
Ⅱ.现用物质的量浓度为amol·L-1的标准盐酸去测定VmLNaOH溶液的物质的量浓度,请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,还应该进行的操作是_________ 。
(2)如图是酸式滴定管中液面在滴定前后的读数:
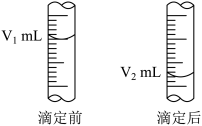
c(NaOH)=_________ mol/L。
(3)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度_________ 。(选填“偏大”、“偏小”、“无影响”)
III.t℃时,某稀硫酸溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知:a+b=12。
(4)该温度下水的离子积常数KW的数值为_________ 。
(5)该温度下(t℃),将100mL0.1mol·L-1的稀H2SO4与100mL0.4mol·L-1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=_________ 。
A.用托盘天平称取11.70g食盐
B.用量筒量取12.36ml盐酸
C.用酸式滴定管量取21.20ml0.10mol·L-1H2SO4溶液
D.用200ml容量瓶配制100ml0.1mol·L-1NaCl溶液
Ⅱ.现用物质的量浓度为amol·L-1的标准盐酸去测定VmLNaOH溶液的物质的量浓度,请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,还应该进行的操作是
(2)如图是酸式滴定管中液面在滴定前后的读数:

c(NaOH)=
(3)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度
III.t℃时,某稀硫酸溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知:a+b=12。
(4)该温度下水的离子积常数KW的数值为
(5)该温度下(t℃),将100mL0.1mol·L-1的稀H2SO4与100mL0.4mol·L-1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=
您最近一年使用:0次
名校
3 . 下列有关实验操作的说法正确的是
| A.用苯萃取溴水中的溴,分液时应从下口放出溴的苯溶液 |
| B.中和热测定时环形玻璃搅拌棒要不断地顺时针搅拌,目的是为了混合均匀,充分反应 |
| C.用滴定管量取溶液体积,若读数时放出液体前仰视,放出液体后俯视,则测量值小于真实值 |
| D.用已知质量分数和密度的浓硫酸配制100 mL 1 mol· L-1H2SO4溶液,通常按计算值称量所需浓硫酸的质量. |
您最近一年使用:0次
名校
4 . I、乙二酸俗名草酸,为了测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资料,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,学习小组的同学设计了滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4。
③用浓度为0.1000 mol·L-1的酸性KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL。
(1)滴定时,将酸性KMnO4标准液装在____________ 滴定管(填“酸式”或“碱式”)。
(2)本实验滴定达到终点的标志是__________________________ 。
(3)通过上述数据,求得x=________ 。
讨论:
①若滴定终点时俯视滴定管刻度,则由此测得的x值会________ (填“偏大”“偏小”或“不变”,下同)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会________ 。
II、(1)25℃时将amol•L-1的氨水与0.01mol•L-1的盐酸等体积混合所得溶液中c(NH4+)=c(Cl-),用含a的代数式表示NH3•H2O的电离平衡常数Kb=______
(2)25℃时,H2SO3 ⇌ HSO3-+ H+的电离常数Ka = 1×10-2mol•L-1,则该温度下pH=3、
c(HSO3-)= 0.1mol•L-1的NaHSO3 溶液中c(H2SO3)=______ .
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4。
③用浓度为0.1000 mol·L-1的酸性KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL。
(1)滴定时,将酸性KMnO4标准液装在
(2)本实验滴定达到终点的标志是
(3)通过上述数据,求得x=
讨论:
①若滴定终点时俯视滴定管刻度,则由此测得的x值会
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会
II、(1)25℃时将amol•L-1的氨水与0.01mol•L-1的盐酸等体积混合所得溶液中c(NH4+)=c(Cl-),用含a的代数式表示NH3•H2O的电离平衡常数Kb=
(2)25℃时,H2SO3 ⇌ HSO3-+ H+的电离常数Ka = 1×10-2mol•L-1,则该温度下pH=3、
c(HSO3-)= 0.1mol•L-1的NaHSO3 溶液中c(H2SO3)=
您最近一年使用:0次
5 . 化学学习小组进行如下实验。
[探究反应速率的影响因素]设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol·L-1H2C2O4溶液、0.010 mol·L-1KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
(1)上述实验①、②是探究__________ 对化学反应速率的影响;若上述实验②、③是探究浓度对化学反应速率的影响,则a为__________ ;乙是实验需要测量的物理量,则表格中“乙”应填写__________ 。
[测定H2C2O4·xH2O 中x值] 已知:M(H2C2O4)=90 g·mol-1
①称取1.260 g纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液;
②取25.00mL 待测液放入锥形瓶中,再加入适的稀H2SO4;
③用浓度为0.05 000 mol·L-1的KMnO4标准溶液进行滴定。
(2)请写出与滴定有关反应的离子方程式_____________________ 。
(3)某学生的滴定方式(夹持部分略去)如图,最合理的是___________ (选填 a、b)。
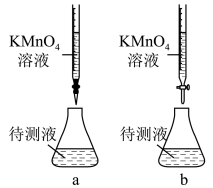
(4)由图可知消耗KMnO4溶液体积为________________ mL。
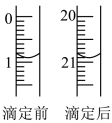
(5)滴定过程中眼睛应注视______ 。
(6)通过上述数据,求得x=_______ 。以标准KMnO4溶液滴定样品溶液的浓度,未用标准KMnO4溶液润洗滴定管,引起实验结果_____________ (偏大、偏小或没有影响) 。
[探究反应速率的影响因素]设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol·L-1H2C2O4溶液、0.010 mol·L-1KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
| 物理量 | V(0.20mol∙L-1H2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010mol∙L-1KMnO4溶液)/mL | T/℃ | 乙 |
| ① | 2.0 | 0 | 4.0 | 50 | |
| ② | 2.0 | 0 | 4.0 | 25 | |
| ③ | 1.0 | a | 4.0 | 25 |
(1)上述实验①、②是探究
[测定H2C2O4·xH2O 中x值] 已知:M(H2C2O4)=90 g·mol-1
①称取1.260 g纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液;
②取25.00mL 待测液放入锥形瓶中,再加入适的稀H2SO4;
③用浓度为0.05 000 mol·L-1的KMnO4标准溶液进行滴定。
(2)请写出与滴定有关反应的离子方程式
(3)某学生的滴定方式(夹持部分略去)如图,最合理的是

(4)由图可知消耗KMnO4溶液体积为

(5)滴定过程中眼睛应注视
(6)通过上述数据,求得x=
您最近一年使用:0次
2020-02-11更新
|
62次组卷
|
2卷引用:云南省绥江县第三中学2019-2020学年高二上学期期末考试化学试题
名校
6 . 化学学习小组进行实验测定H2C2O4·xH2O 中x值。已知:M(H2C2O4)=90 g·mol-1
①称取 1.260 g 纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液;
②取25.00mL 待测液放入锥形瓶中,再加入适量稀H2SO4;
③用浓度为 0.05 000 mol·L-1的 KMnO4标准溶液进行滴定。
(1)请写出与滴定有关反应的离子方程式__________ 。
(2)某学生的滴定方式(夹持部分略去)如下,最合理的是__________ (选填 a、b)。
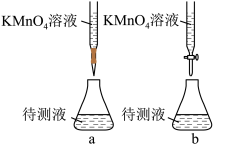
(3)由图可知消耗KMnO4溶液体积为_______ mL。
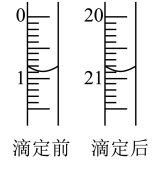
(4)滴定过程中眼睛应注视________ 。
(5)通过上述数据,求得x=______ 。以标准KMnO4溶液滴定样品溶液的浓度,未用标准KMnO4溶液润洗滴定管,引起实验结果______ (偏大、偏小或没有影响) 。
①称取 1.260 g 纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液;
②取25.00mL 待测液放入锥形瓶中,再加入适量稀H2SO4;
③用浓度为 0.05 000 mol·L-1的 KMnO4标准溶液进行滴定。
(1)请写出与滴定有关反应的离子方程式
(2)某学生的滴定方式(夹持部分略去)如下,最合理的是

(3)由图可知消耗KMnO4溶液体积为

(4)滴定过程中眼睛应注视
(5)通过上述数据,求得x=
您最近一年使用:0次
2020-02-05更新
|
92次组卷
|
2卷引用:云南省普洱市普洱第二中学2019—2020学年高二上学期期末考试化学试题
名校
7 . 草酸又名乙二酸,广泛存在于植物源食品中,它的用途非常广泛。测定某草酸晶体(组成为H2C2O4·nH2O)中H2C2O4的质量分数,进行下列实验:①取 w g 草酸晶体配成 250mL 溶液;②取 25.00mL 所配草酸溶液置于锥形瓶中, 加入适量稀H2SO4 后,在锥形瓶底部垫一张白纸,用浓度为 0.100mol·L-1KMnO4 溶液滴定。滴定时,所发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。
请回答下列问题:
(1)上述反应的还原剂是_____ (填化学式)。
(2)步骤①中为配制准确浓度的草酸溶液,所需用到的仪器有:天平(含砝码)、烧杯、药匙、250ml 容量瓶和___________ 、_______________ 。
(3)在锥形瓶底部垫一张白纸的作用是_____ 。
(4)滴定管应选用_______ 式滴定管(填“酸”或“碱”),判断滴定结束的标准是_________ 。
(5)三次滴定所用 KMnO 溶液体积平均为 20.00mL,则实验测得所配草酸溶液的物质的量浓度为______________ mol·L-1;草酸晶体中 H2C2O4 的质量分数为_______________ ;在实验过程中,锥形瓶用蒸馏水洗净之后,再用草酸溶液润洗,对测定结果造成的影响是_______ (填“偏大”、“偏小”或“无影响)
请回答下列问题:
(1)上述反应的还原剂是
(2)步骤①中为配制准确浓度的草酸溶液,所需用到的仪器有:天平(含砝码)、烧杯、药匙、250ml 容量瓶和
(3)在锥形瓶底部垫一张白纸的作用是
(4)滴定管应选用
(5)三次滴定所用 KMnO 溶液体积平均为 20.00mL,则实验测得所配草酸溶液的物质的量浓度为
您最近一年使用:0次
2019-12-11更新
|
90次组卷
|
2卷引用:云南省普洱市西盟佤族自治县第一中学2021-2022学年高二上学期12月月考化学试题
名校
解题方法
8 . 用标准浓度氢氧化钠的溶液来滴定未知浓度的盐酸,下列操作中会使盐酸测定的浓度偏大的是( )
①碱式滴定管用蒸馏水洗净后未用标准溶液润洗
②锥形瓶中盛有少量蒸馏水,再加待测液
③酸式滴定用蒸馏水洗净后,未用盐酸润洗
④滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
⑤滴定后观察碱式滴定管读数时,俯视刻度线
①碱式滴定管用蒸馏水洗净后未用标准溶液润洗
②锥形瓶中盛有少量蒸馏水,再加待测液
③酸式滴定用蒸馏水洗净后,未用盐酸润洗
④滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
⑤滴定后观察碱式滴定管读数时,俯视刻度线
| A.①④ | B.①③ | C.②③ | D.④⑤ |
您最近一年使用:0次
2019-11-30更新
|
238次组卷
|
11卷引用:云南省玉溪市玉溪一中2017-2018学年高二上学期第二次月考化学试题
云南省玉溪市玉溪一中2017-2018学年高二上学期第二次月考化学试题河北省邯郸市第二中学2017-2018学年高二上学期期中考试化学试题湖北省黄冈市2019-2020学年高二10月月考化学试题吉林省吉林市蛟河市第一中学2019-2020学年高二上学期期中考试化学试题吉林省长春市实验中学2019-2020学年高二上学期期中考试化学试题安徽省滁州市明光中学2019-2020学年高二上学期期中考试化学试题备考突破2020高三化学专题强化集训——酸碱中和滴定及其拓展江西省新余市第一中学2019-2020学年高二上学期第二次段考试化学试题湖北省黄冈市黄梅国际育才高级中学2019-2020学年高二上学期10月月考化学试题湖北省华中师范大学潜江附属中学2021-2022学年高二上学期10月月考化学试题广东省化州市第一中学2020-2021学年高二上学期10月月考化学试题
10-11高二上·江西上饶·期中
名校
9 . 乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4·xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。该组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O,学习小组的同学设计了滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4。
③用浓度为0.1000 mol·L-1的酸性KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL。
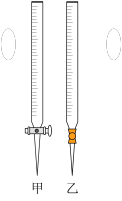
(1)滴定时,将酸性KMnO4标准液装在如图中的________ (填“甲”或“乙”)滴定管中。
(2)本实验滴定达到终点的标志是___________________ 。
(3)通过上述数据,求得x=________ 。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会________ (填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会________ 。
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4。
③用浓度为0.1000 mol·L-1的酸性KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL。
(1)滴定时,将酸性KMnO4标准液装在如图中的

(2)本实验滴定达到终点的标志是
(3)通过上述数据,求得x=
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会
您最近一年使用:0次
2019-11-19更新
|
764次组卷
|
30卷引用:云南省玉溪市通海县第一中学2021-2022学年高二上学期期末考试化学试题
云南省玉溪市通海县第一中学2021-2022学年高二上学期期末考试化学试题(已下线)2010年江西省德兴市四校联考高二上学期期中考试化学试卷(已下线)2011-2012学年山东省济宁市曲阜一中高二上学期期末模拟化学试卷(已下线)2011-2012学年福建省罗源一中高二上学期期末考试化学试卷2014-2015浙江省杭州市西湖中学高二12月月考化学试卷2014-2015学年浙江省江山实验中学高二4月教学质量检测化学试卷2015-2016学年山西省太原五中高二上12月月考化学试卷12015-2016学年山西省太原五中高二上12月月考化学试卷22015-2016学年福建省长泰县第一中学高二上学期期末化学试卷2015-2016学年河南省南阳一中高二下期末模拟化学试卷广西桂林市第十八中学2016-2017学年高二下学期期中考试化学试题湖北省荆门市2016-2017学年高二下学期期末质量检测化学试题河南省豫北重点中学2017-2018学年高二12月联考化学试题【全国百强校】贵州省思南中学2018-2019学年高二上学期第二次月考化学试题(已下线)2019年1月2日 《每日一题》人教选修4-酸碱中和滴定陕西省黄陵中学2018-2019学年高二(普通班)上学期期末考试化学试题步步为赢 高二化学暑假作业:作业十 水溶液中的离子平衡浙江省宁波市北仑中学2019-2020学年高二上学期期中考试化学(2-10班)试题(已下线)2019年12月27日 《每日一题》人教版(选修4)——酸碱中和滴定江苏省宿豫中学2019-2020学年度高二下学期调研测试(奥赛班)化学试题广西桂林市第十八中学2019-2020学年高二下学期开学考试化学试题四川省成都市第七中学2019-2020学年高二下学期零诊模拟考试化学人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 易错疑难集训(二)辽宁省沈阳市第八十三中学2021-2022学年高二上学期期初考试化学试题(已下线)高中化学《新教材变化解读与考法剖析》第三章 水溶液中的离子反应与平衡(人教版2019选择性必修1)江西省抚州市南城县第二中学2021-2022年高二上学期第二次月考化学试题河北省保定市博野中学2021-2022学年高二上学期期中考试化学试题河南省温县第一高级中学2022-2023学年高二上学期第二次月考化学试题河南省鹤壁市高中2022-2023学年高二上学期10月居家测试化学(宏奥班)试题河南省南阳市第一中学校2023-2024学年高二上学期12月月考化学试题
名校
解题方法
10 . 下列实验误差分析错误的是
| A.滴定管未润洗直接加入标准液,则待测溶液浓度偏大 |
| B.用容量瓶配制溶液,定容时仰视刻度线,所配溶液浓度偏小 |
| C.用润湿的pH试纸测稀酸溶液的pH,测定值偏小 |
| D.测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小 |
您最近一年使用:0次
2019-11-18更新
|
533次组卷
|
4卷引用:云南省楚雄彝族自治州民族中学2021-2022学年高二下学期3月月考化学试题



