名校
解题方法
1 . 常温下,向20mL0.1mol/L一元碱MOH溶液中滴加等浓度的一元酸HX溶液,滴定过程中溶液pH值的变化曲线如下图所示,已知4<m<6,下列说法不正确的是

| A.该滴定过程中应选用酚酞作指示剂 | B.一元酸HX的Ka=5×10-5 |
| C.溶液中水的电离程度:b>c>a | D.c点溶液中:c(M+)>c(X-)>c(H+)>c(OH-) |
您最近一年使用:0次
2024-01-15更新
|
340次组卷
|
4卷引用:湖南省常德市第一中学2023-2024学年高二上学期期末考试化学试题
湖南省常德市第一中学2023-2024学年高二上学期期末考试化学试题2024届陕西省宝鸡市高考模拟监测(一) 理科综合试题(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)广东省梅州市大埔县虎山中学2023-2024学年高二下学期4月期中考试化学试题
2 . 下列实验方案能达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 探究葡萄糖的还原性 | 在一支试管中先加入2mL10%NaOH溶液,滴入5滴 溶液,再加入2mL10%葡萄糖溶液,加热,观察实验现象 溶液,再加入2mL10%葡萄糖溶液,加热,观察实验现象 |
B | 探究过氧化氢能否将亚硫酸盐氧化 | 向过氧化氢和氯化钡混合液中滴加亚硫酸钠溶液,观察是否产生白色沉淀 |
C | 验证草酸为二元弱酸 | 用0.1mol/LNaOH标准溶液滴定等浓度草酸溶液,使用酚酞作指示剂,到达滴定终点时消耗NaOH的体积为草酸的2倍 |
D | 探究水解程度: | 用pH计分别测定饱和 和 和 溶液的pH,前者pH大 溶液的pH,前者pH大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 用0.100mol·L-1的NaOH溶液分别滴定体积均为10.00mL、浓度均为0.100mol·L-1的HCl和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率(电导率越大表示溶液导电性越强)变化如图所示。下列说法正确的是


| A.曲线①代表向HCl中滴加NaOH | B.A点溶液的pH小于C点溶液的pH |
| C.A、B两点水的电离程度:A>B | D.C→D发生了反应:H++OH-=H2O |
您最近一年使用:0次
2022-07-23更新
|
1324次组卷
|
10卷引用:湖南省株洲市九方中学2021-2022学年高二下学期期末考试化学试题
湖南省株洲市九方中学2021-2022学年高二下学期期末考试化学试题北京市房山区2022届高三第二次模拟测试化学试题北京市一零一中学2022届高三三模化学试题(已下线)2022年浙江1月高考真题变式题(11-20)北京市第一七一中学2022届高三下学期三模化学试题(已下线)第23讲 弱电解质的电离平衡(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)易错点24 水的电离平衡-备战2023年高考化学考试易错题黑龙江省哈尔滨师范大学附属中学2022-2023学年高二上学期期中考试化学试题北京市顺义一中2023届高三下学期保温练习模拟考试化学试题(已下线)考点2 水的电离与溶液的pH (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
4 . 无水FeCl2为黄绿色晶体,在空气中易被氧化和易吸水,不溶于氯仿等有机溶剂。回答下列问题:
I.FeCl2的制备及产率测定:制备反应原理为2FeCl3+C6H5Cl 2FeCl2+C6H4Cl2+HCl(C6H5Cl为氯苯,沸点132℃),产率通过测定HCl的量进行计算。制备装置如图所示(夹持及加热装置略去):
2FeCl2+C6H4Cl2+HCl(C6H5Cl为氯苯,沸点132℃),产率通过测定HCl的量进行计算。制备装置如图所示(夹持及加热装置略去):
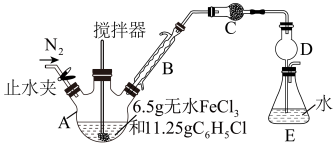
(1)仪器A的名称是____ ,仪器B的作用是____ ,装置C中的试剂是____ (填化学式)。
(2)为测定FeCl2的产率,用1.00mol·L-1NaOH溶液滴定溶于水的HCl,达到滴定终点时消耗NaOH溶液19.00mL,则FeCl2的产率为____ 。下列操作中,导致产率测定值偏低的是____ 。
a.滴定终点时俯视读数
b.滴定管未用NaOH标准溶液润洗
c.配制NaOH标准溶液时,转移溶液未洗涤烧杯
d.滴定前滴定管内无气泡,滴定结束后有气泡
II.FeCl2性质探究:将FeCl2晶体配成溶液后进行如表实验。
已知:Ba2+与SCN-可在溶液中大量共存;SCN-易被氧化为SO 。
。
(3)对实验ⅰ中溶液为浅红色的原因,甲同学提出以下假设:
假设1:加入氯水的量少,生成的Fe3+浓度低;
假设2:氯水氧化性强,____ 。
取实验ⅰ中浅红色溶液,____ (填实验操作),溶液浅红色消失,从而排除了假设1;向2mL水中滴加0.5mL0.1mol·L-1KSCN溶液,滴加0.5mL饱和氯水,加入____ ,产生白色沉淀,说明假设2正确。
(4)分析实验ⅱ“一段时间后,溶液褪为无色”的原因是____ (用离子方程式表示,已知SCN-中C元素为+4价)。
I.FeCl2的制备及产率测定:制备反应原理为2FeCl3+C6H5Cl
 2FeCl2+C6H4Cl2+HCl(C6H5Cl为氯苯,沸点132℃),产率通过测定HCl的量进行计算。制备装置如图所示(夹持及加热装置略去):
2FeCl2+C6H4Cl2+HCl(C6H5Cl为氯苯,沸点132℃),产率通过测定HCl的量进行计算。制备装置如图所示(夹持及加热装置略去):
(1)仪器A的名称是
(2)为测定FeCl2的产率,用1.00mol·L-1NaOH溶液滴定溶于水的HCl,达到滴定终点时消耗NaOH溶液19.00mL,则FeCl2的产率为
a.滴定终点时俯视读数
b.滴定管未用NaOH标准溶液润洗
c.配制NaOH标准溶液时,转移溶液未洗涤烧杯
d.滴定前滴定管内无气泡,滴定结束后有气泡
II.FeCl2性质探究:将FeCl2晶体配成溶液后进行如表实验。
| 序号 | 装置 | 试剂 | 实验现象 | |
| 实验ⅰ | 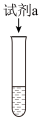 | 0.5mL0.1mol·L-1 KSCN溶液、1mL0.1mol·L-1 FeCl2(pH=1)溶液 | 0.5mL饱和氯水 | 溶液立即变为浅红色 |
| 实验ⅱ | 1mLl.5mol·L-1 HNO3溶液 | 滴入硝酸后,溶液变为红色,一段时间后,溶液褪为无色,且溶液中产生无色气泡,试管上方呈红棕色。 | ||
 。
。(3)对实验ⅰ中溶液为浅红色的原因,甲同学提出以下假设:
假设1:加入氯水的量少,生成的Fe3+浓度低;
假设2:氯水氧化性强,
取实验ⅰ中浅红色溶液,
(4)分析实验ⅱ“一段时间后,溶液褪为无色”的原因是
您最近一年使用:0次
2022-05-11更新
|
483次组卷
|
3卷引用:湖南省益阳市第一中学2021-2022学年高二下学期期末考试化学试题
解题方法
5 . 298K时,向20 mL 0.1000 mol·L-1 CH3COOH溶液中滴入0.1000 mol·L-1NaOH溶液,滴定曲线如图所示(忽略温度变化)。下列说法正确的是


| A.该滴定过程应该选择石蕊溶液做指示剂 |
| B.由c点数值可求醋酸的电离平衡常数为1.66×10-5 mol·L-1 |
| C.b点溶液中各微粒浓度关系为2c(H+)+c(CH3COOH) =c(CH3COO-)+2c(OH-) |
| D.中和同体积同pH的醋酸和盐酸所用氢氧化钠的物质的量,后者多 |
您最近一年使用:0次
2020-05-09更新
|
408次组卷
|
2卷引用:湖南省邵阳市新邵县2019-2020学年高二下学期期末考试化学试题
名校
解题方法
6 . 准确称量8.2g 含有少量中性易溶杂质的烧碱样品,配成500mL 待测溶液。用0.1000mol⋅L−1的硫酸溶液进行中和滴定测定该烧碱样品的纯度,试根据试验回答下列问题:
(1)滴定过程中,眼睛应注视____________ ,若用酚酞作指示剂达到滴定终点的标志是____________ 。
(2)根据表数据,计算烧碱样品的纯度是_______________ (用百分数表示,保留小数点后两位)
(3)下列实验操作会对滴定结果产生什么后果?(填“偏高”“偏低”或“无影响”)
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果________ 。
②若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果________ 。
(1)滴定过程中,眼睛应注视
(2)根据表数据,计算烧碱样品的纯度是
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL)) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果
②若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果
您最近一年使用:0次
解题方法
7 . 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)滴定终点的判断:溶液由_____________ 。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是( )
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为_________ mL。

(4)某学生根据3次实验分别记录有关数据如表:
②依据上表数据计算该NaOH溶液的物质的量浓度________ (计算结果取4位有效数)。
(1)滴定终点的判断:溶液由
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为

(4)某学生根据3次实验分别记录有关数据如表:
| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000 mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 平均耗用盐酸 体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.15 | ①V= |
| 第二次 | 25.00 | 0.56 | 30.30 | |
| 第三次 | 25.00 | 0.20 | 26.35 | |
您最近一年使用:0次
2019-12-13更新
|
101次组卷
|
2卷引用:湖南省长沙市长沙县第九中学2018-2019学年高二下学期期末考试化学试题
8 . NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的Ka1=1.1×10−3 ,Ka2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是
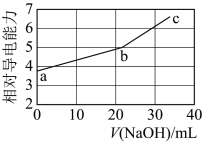

| A.混合溶液的导电能力与离子浓度和种类有关 |
| B.Na+与A2−的导电能力之和大于HA−的 |
| C.b点的混合溶液pH=7 |
| D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−) |
您最近一年使用:0次
2019-06-09更新
|
21039次组卷
|
67卷引用:湖南省长沙市天心区雅礼中学2018-2019学年高二下学期期末考试化学试题
湖南省长沙市天心区雅礼中学2018-2019学年高二下学期期末考试化学试题湖南省长沙市雅礼中学2019-2020学年高二上学期期末考试化学试题湖南省株洲市茶陵二中2020届高三上学期第二次月考化学试题福建省莆田第二十五中学2020届高三上学期期末考试化学试题湖北省沙市中学2021-2022学年高二上学期期末考试化学试题河北省秦皇岛市第一中学2021-2022学年高二下学期期末考试化学试题湖南省永州市宁远县第一中学2022-2023学年高二上学期期中考试化学试题2018-2019学年度耀华实验学校第二学期高二实验化学期末试卷2019年全国统一考试化学试题(新课标Ⅰ)(已下线)专题10 水溶液中的离子平衡——2019年高考真题和模拟题化学分项汇编安徽省阜阳市颍上二中等三校2020届高三上学期入学考试化学试题(已下线)专题8.1 弱电解质的电离平衡(讲)-《2020年高考一轮复习讲练测》2020届高考化学小题狂练(全国通用版)专练15 弱电解质的电离平衡和溶液酸碱性云南师范大学附属中学2019-2020学年高二上学期期中考试化学试题江苏省海安高级中学2019-2020学年高二12月月考化学试题专题2.3 水溶液中的离子平衡(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升天津市海河中学2020届高三第二学期化学测试(二)试卷(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训辽宁省本溪市2019-2020学年高二下学期寒假验收考试化学试题江苏省南通市2020届高三第二次模拟考试(5月) 化学 试题黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题北京市海淀区育英学校2020届高三三模化学试题天津市第一中学2020届高三下学期第五次月考化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3章 综合检测高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三章素养检测(已下线)3.3.2+影响盐类水解的主要因素和盐类水解的应用-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 高考帮(已下线)第03章 水溶液中的离子反应与平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过高考 3年真题强化闯关第25讲 弱电解质的电离平衡(精讲)-2021年高考化学一轮复习讲练测(已下线)【浙江新东方】【2020】【高三上】【一模】【HD-LP416】【化学】(已下线)【浙江新东方】112(已下线)小题必刷31 酸碱中和滴定及拓展应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)小题必刷30 水的电离与溶液的酸碱性——2021年高考化学一轮复习小题必刷(通用版本)(已下线)小题必刷29 弱电解质的电离平衡——2021年高考化学一轮复习小题必刷(通用版本)(已下线)小题必刷33 粒子浓度大小比较——2021年高考化学一轮复习小题必刷(通用版本)福建省连城县第一中学2021届高三上学期第二次月考化学试题(已下线)专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题重庆市育才中学2021届高三下学期入学考试化学试题(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)专题07 电解质溶液——备战2021年高考化学纠错笔记(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)天津市南开中学2021届高三上学期第五次月考化学试卷(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)选择性必修1(SJ)专题3专题培优专练(已下线)考点23 弱电解质的电离-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时39 弱电解质的电离平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第21讲 电离平衡(讲)-2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第6讲 离子平衡坐标图像-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)重庆育才中学2021-2022学年高二上学期第四次定时练习化学试题山西省太原市第五中学2021-2022学年高二上学期12月月考化学试题(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-练习鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第4节 离子反应(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)浙江省绍兴市柯桥区2022届高考及选考科目5月适应性考试化学试题(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)天津市咸水沽第一中学2023届高三上学期第一次模拟考试化学试题(已下线)第21讲 电离平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题06 水溶液中的离子平衡(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)第八章 水溶液中的离子反应与平衡 第46讲 弱电解质的电离平衡(已下线)题型134 导电能力与酸碱中和滴定图像广东省汕头市金山中学2022-2023学年高二下学期期中考试化学试题(已下线)专题16 水溶液中的离子平衡(已下线)T11-电解质溶液(已下线)第31讲盐类的水解
9 . 用0.1 mol·L−1的盐酸滴定20 mL约0.1 mol·L−1氨水,滴定曲线如图所示,下列说法正确的是


| A.a点溶液中:c(H+)=c(OH−)+c(NH3·H2O) |
| B.滴定过程中,当溶液的pH=7时,两者恰好中和 |
| C.用酚酞作指示剂比用甲基橙作指示剂,滴定误差更小 |
| D.当滴入盐酸为30 mL时,溶液中:c(NH4+)+c(H+)<c(OH−)+c(Cl−) |
您最近一年使用:0次
2018-01-27更新
|
547次组卷
|
3卷引用:湖南省怀化市2018届高三上学期期末教育质量监测化学试题
10-11高二下·云南昆明·期末
名校
10 . 在25mL 0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是


| A.在A、B间任一点(不含A、B点),溶液中可能有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+) |
| C.在C点,c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| D.在D点,c(CH3COO-)+c(CH3COOH)=c(Na+) |
您最近一年使用:0次
2016-12-09更新
|
591次组卷
|
9卷引用:2011-2012年湖南株洲市南方中学高二上学期期末考试理科化学试卷
(已下线)2011-2012年湖南株洲市南方中学高二上学期期末考试理科化学试卷(已下线)2012-2013学年湖南省益阳市一中高二上学期期末考试理科化学试卷(已下线)2010—2011学年云南省昆明三中高二下学期期末考试化学试卷(已下线)2012-2013学年吉林省白山市第一中学高二下学期期末考试化学试卷2014-2015学年湖北省枣阳市白水高级中学高二下学期期末化学试卷吉林省长春市实验中学2019-2020学年高二上学期期末考试化学试题(已下线)2011-2012学年辽宁省沈阳四校协作体高二上学期期中考试化学试卷山西省朔州市应县第一中学校2019-2020学年高二上学期第三次月考化学试题2020届高三化学选修4二轮专题练——混合溶液中微粒浓度大小的比较专题【精编23题】



