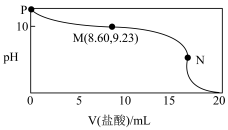
1 . 常温常压下,某同学向20.00mLc0mol•L-1氨水中逐滴加入0.1000mol•L-1的盐酸,实验测得溶液的pH随加入盐酸体积的变化如图所示,其中N点为反应终点(此时盐酸与氨水恰好完全反应),此时消耗盐酸的体积为17.20mL。下列说法中正确的是

| A.选择甲基橙作指示剂,比选用酚酞作指示剂的误差大 |
B.M点的溶液中存在:c(NH3•H2O)>c(Cl-)>c(NH ) ) |
| C.N点溶液中:c(H+)-c(OH-)<c(Cl-)-c(NH3•H2O) |
| D.P、M、N三点对应溶液中水的电离程度最大的为M点 |
您最近一年使用:0次
解题方法
2 . 25℃时,用0.1000mol·L-1的盐酸分别滴定20.00mL 0.1000mol·L-1氨水和20.00mL 0.1000mol·L-1 NaOH溶液,滴定曲线如图所示。下列说法不正确的是


| A.25℃,Kb(NH3·H2O)的数量级为10-5 |
B.N点处的溶液中:c(NH )>c(NH3·H2O) )>c(NH3·H2O) |
| C.曲线II滴定终点时所选的指示剂为酚酞 |
| D.Q点所加盐酸的体积为b mL,则b=20 |
您最近一年使用:0次
3 . 25 °C时,用浓度为0.1000 mol/L的NaOH溶液滴定体积均是20mL、浓度均为0.1000 mol/L的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法正确的是( )


| A.酸性强弱顺序是HX> HY> HZ |
| B.加入10 mL NaOH溶液时,HY溶液中c(Na+)>c(Y -) |
| C.pH=2的HZ溶液加水稀释10倍,pH为3 |
| D.加入20 mL NaOH溶液时,只有HY溶液达到滴定终点 |
您最近一年使用:0次
解题方法
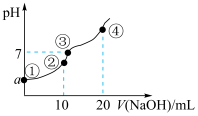
4 . 常温下,向10.00 mL 0.1mol/L某二元酸H2X溶液中逐滴加入0.1 mol/L NaOH溶液,其pH变化如图所示(忽略温度变化),已知:常温下,H2X的电离常数Ka1=1.1×10-5,Ka2=1.3×10-8。下列叙述正确的是
| A.a近似等于3 |
| B.点②处c(Na+)+2c(H+)+c(H2X)=2c(X2-)+c(HX-)+2c(OH-) |
| C.点③处为H2X和NaOH中和反应的滴定终点 |
| D.点④处c(Na+)=2c(X2-)>c(OH-)>c(HX-)>c(H+) |
您最近一年使用:0次
2019-11-03更新
|
937次组卷
|
5卷引用:广西名校高三2019-2020学年第一学期第一次大联考-化学
解题方法
5 . 甲胺(CH3NH2)是一种应用广泛的一元弱碱。常温下,向200mL0.10mol/L的甲胺溶液中滴加V mL.0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是


| A.b点对应加入盐酸的体积V< 20.00mL |
B.甲胺在水中的电离方程式为:CH3NH2+H2O CH3NH3++OH- CH3NH3++OH- |
| C.常温下,甲胺的电离常数为Kb,则pKb=-1gKb=4.3 |
| D.c点可能存在关系: 2c(H+)+ c(CH3NH3+)=c(CH3NH2) +2c(OH- )+ c(Cl-) |
您最近一年使用:0次
2018-03-10更新
|
442次组卷
|
2卷引用:广西桂林、贺州、崇左三市2018届高三第二次联合调研考试理综化学试题
6 . 25℃时,分别取浓度均为0.1mol·L-1的醋酸溶液和氨水溶液各20mL于两个锥形瓶中,分别用0.1mol·L-1NaOH溶液、0.1mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如右图所示。下列说法正确的是( )


| A.25℃时,0.1mol·L-1的醋酸溶液中CH3COOH约有10%电离 |
| B.绘制曲线Ⅱ的实验中通过控制滴定管玻璃活塞控制滴定速度 |
| C.曲线Ⅰ上a点溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D.曲线Ⅱ上b点溶液中:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
您最近一年使用:0次



