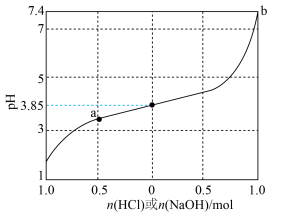
1 . 缓冲溶液是指加少量水稀释或外加少量酸、碱,自身pH不发生显著变化的溶液。1L含1mol乳酸(HLac)和1mol乳酸钠(NaLac)的溶液就是一种缓冲溶液,该溶液的pH为3.85。下图是此缓冲溶液的pH随通入HCl(g)或加入NaOH(s)的物质的量变化的示意图(溶液体积保持1L),已知lg3=0.48。下列说法错误的是
A.此缓冲溶液中(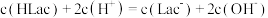 |
| B.通过计算可得出,a点溶液的pH约为3.37 |
| C.根据图像可以判断,b点溶液已失去缓冲能力 |
D.当加入NaOH,且横坐标为0.5时,对应溶液中(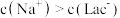 |
您最近半年使用:0次
名校
2 . 配合物的中心离子M与配体L之间存在平衡关系:
 ,
,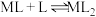
 ,
,
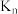 。向
。向 溶液中滴加氨水,含铜微粒的分布系数
溶液中滴加氨水,含铜微粒的分布系数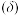 与溶液中
与溶液中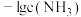 关系如图。下列说法错误的是
关系如图。下列说法错误的是

 ,
,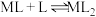
 ,
,
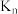 。向
。向 溶液中滴加氨水,含铜微粒的分布系数
溶液中滴加氨水,含铜微粒的分布系数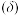 与溶液中
与溶液中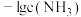 关系如图。下列说法错误的是
关系如图。下列说法错误的是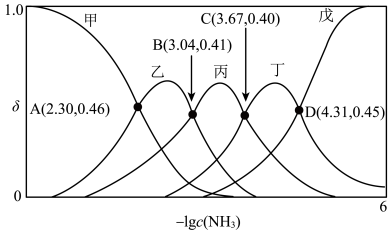
A.曲线甲表示的含铜微粒是 |
B.当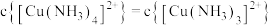 时, 时,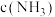 的数量级为 的数量级为 |
C.溶液中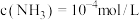 时, 时,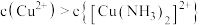 |
D.反应 的平衡常数为 的平衡常数为 , , |
您最近半年使用:0次
解题方法
3 . 常温下,将 溶液滴入三元酸
溶液滴入三元酸 溶液中,混合溶液中
溶液中,混合溶液中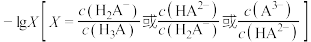 随
随 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是
 溶液滴入三元酸
溶液滴入三元酸 溶液中,混合溶液中
溶液中,混合溶液中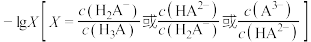 随
随 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是
A.曲线 表示 表示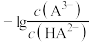 随 随 的变化关系 的变化关系 |
B.当 时,混合溶液中 时,混合溶液中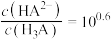 |
C.常温下,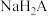 溶液中: 溶液中: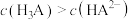 |
D.当 时, 时, |
您最近半年使用:0次
4 . 常温下,下列有关氨水的说法正确的是
| A.等物质的量浓度的氨水与NaOH溶液,导电能力相同 |
B.往氨水中加水稀释, 逐渐减小 逐渐减小 |
C.pH均为10的氨水与 溶液中, 溶液中, 相等 相等 |
| D.pH=11的氨水与pH=3的盐酸等体积混合后溶液显酸性 |
您最近半年使用:0次
5 . 下列叙述正确的是
A.将 溶液从 溶液从 升温至 升温至 ,溶液中 ,溶液中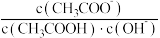 增大 增大 |
B.向盐酸中加入氨水至中性,溶液中 |
C. 时, 时, 的 的 溶液比等浓度的 溶液比等浓度的 溶液的导电能力弱 溶液的导电能力弱 |
D. 时, 时, 一元酸 一元酸 与 与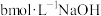 溶液等体积混合后所得溶液的 溶液等体积混合后所得溶液的 为 为 ,则 ,则 |
您最近半年使用:0次
6 . 已知  时
时 ,下列叙述中不正确的是
,下列叙述中不正确的是
 时
时 ,下列叙述中不正确的是
,下列叙述中不正确的是A. 时,向等浓度的 时,向等浓度的 和 和 混合溶液中逐滴加入氨水,先出现红褐色沉淀 混合溶液中逐滴加入氨水,先出现红褐色沉淀 |
B. 时, 时, 溶液中有少量 溶液中有少量 时,可以加入 时,可以加入 进行除杂 进行除杂 |
C. 时, 时,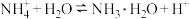 的平衡常数为 的平衡常数为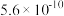 |
D. 时,加大量水稀释氨水,溶液中粒子的浓度均减小 时,加大量水稀释氨水,溶液中粒子的浓度均减小 |
您最近半年使用:0次
7 . 现有常温下 的醋酸溶液,下列有关叙述正确的是
的醋酸溶液,下列有关叙述正确的是
 的醋酸溶液,下列有关叙述正确的是
的醋酸溶液,下列有关叙述正确的是A.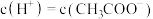 |
B.加入醋酸钠固体可抑制醋酸的电离,但电离常数 不变 不变 |
C.与 的 的 溶液等体积混合后,溶液呈碱性 溶液等体积混合后,溶液呈碱性 |
D.醋酸的物质的量浓度为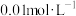 |
您最近半年使用:0次
8 . 常温下,一种解释乙酰水杨酸(用HA表示, )药物在人体吸收模式如下:
)药物在人体吸收模式如下:
 )药物在人体吸收模式如下:
)药物在人体吸收模式如下:
A.血浆中 大于胃中 大于胃中 | B.取胃中液体,加水稀释100倍后,pH=3.0 |
C.在血浆中,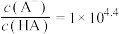 | D.在血浆和胃中,HA电离程度相同 |
您最近半年使用:0次
名校
9 . 向硫酸铜溶液中通入氨气,溶液中含Cu微粒存在如下平衡: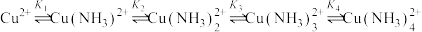 ,各含铜组分分布系数与
,各含铜组分分布系数与 关系如图所示。下列说法错误的是
关系如图所示。下列说法错误的是
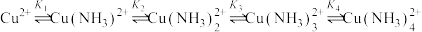 ,各含铜组分分布系数与
,各含铜组分分布系数与 关系如图所示。下列说法错误的是
关系如图所示。下列说法错误的是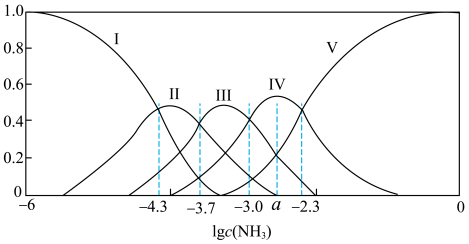
A.曲线Ⅰ代表 |
B.反应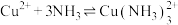 的平衡常数的值为 的平衡常数的值为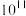 |
C.当溶液中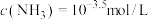 时,溶液中离子浓度最大的是 时,溶液中离子浓度最大的是 |
| D.a=-2.65 |
您最近半年使用:0次
10 . 室温下,向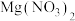 溶液、
溶液、 溶液、
溶液、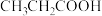 溶液中分别滴加
溶液中分别滴加 溶液,测得溶液
溶液,测得溶液 [
[ ,X代表
,X代表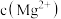 、
、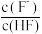 、
、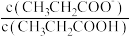 ]随溶液
]随溶液 的变化曲线如图所示。
的变化曲线如图所示。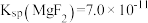 ,
, 的酸性比
的酸性比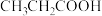 强。下列叙述正确的是
强。下列叙述正确的是
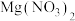 溶液、
溶液、 溶液、
溶液、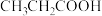 溶液中分别滴加
溶液中分别滴加 溶液,测得溶液
溶液,测得溶液 [
[ ,X代表
,X代表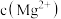 、
、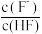 、
、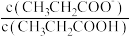 ]随溶液
]随溶液 的变化曲线如图所示。
的变化曲线如图所示。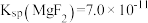 ,
, 的酸性比
的酸性比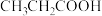 强。下列叙述正确的是
强。下列叙述正确的是
A. 代表 代表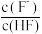 , ,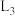 代表 代表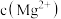 |
B.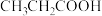 的 的 数量级为 数量级为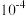 |
C.相同浓度的 、 、 混合溶液的 混合溶液的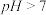 |
D.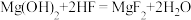 的 的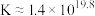 |
您最近半年使用:0次



