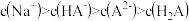配合物的中心离子M与配体L之间存在平衡关系:
 ,
,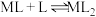
 ,
,
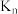 。向
。向 溶液中滴加氨水,含铜微粒的分布系数
溶液中滴加氨水,含铜微粒的分布系数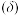 与溶液中
与溶液中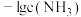 关系如图。下列说法错误的是
关系如图。下列说法错误的是

 ,
,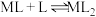
 ,
,
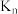 。向
。向 溶液中滴加氨水,含铜微粒的分布系数
溶液中滴加氨水,含铜微粒的分布系数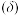 与溶液中
与溶液中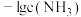 关系如图。下列说法错误的是
关系如图。下列说法错误的是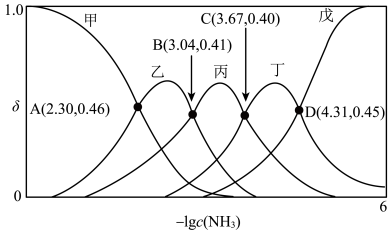
A.曲线甲表示的含铜微粒是 |
B.当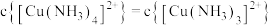 时, 时,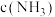 的数量级为 的数量级为 |
C.溶液中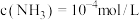 时, 时,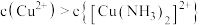 |
D.反应 的平衡常数为 的平衡常数为 , , |
更新时间:2024-05-11 13:57:33
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】在某温度时,将n mol/L醋酸滴入10mL 1.0mo/L氢氧化钠溶液中,溶液pH和温度随加入醋酸体积变化曲线如图所示。下列有关说法正确的是


| A.n=1.0 |
| B.水的电离程度:c>b>a |
| C.25℃时,CH3COONa的水解常数为(n-1)×10-7 |
| D.b点:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知:pKa=-lgKa。25℃时,几种弱酸的pKa值如下表所示。下列说法正确的是
| 弱酸的化学式 | CH3COOH | HCOOH | H2SO3 |
| pKa | 4.74 | 3.74 | 1.90 7.20 |
| A.向Na2SO3溶液中加入过量乙酸,反应生成SO2 |
| B.25℃时,pH=8的甲酸钠溶液中,c( HCOOH)=9.9×10-7mol·L-1 |
| C.25℃时,某乙酸溶液pH=a,则等浓度的甲酸pH=a-1 |
| D.相同温度下,等浓度的 HCOONa溶液比Na2SO3溶液的pH大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】已知:25℃时某些弱酸的电离平衡常数(如下表)。下面图象表示常温下稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化。下列说法正确的是()
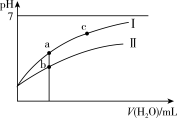
| CH3COOH | HClO | H2CO3 |
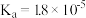 | 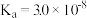 | 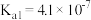 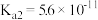 |

| A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) |
B.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO |
C.图象中a、c两点处的溶液中 相等(HR代表CH3COOH或HClO) 相等(HR代表CH3COOH或HClO) |
| D.图象中a点酸的浓度大于b点酸的浓度 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】甘氨酸铜是一种优质的有机铜源,其化学结构稳定,对环境污染也比无机铜低。甘氨酸铜有顺式和反式两种同分异构体,结构如下图。下列说法正确的是
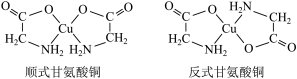
A.铜原子的杂化类型为 杂化 杂化 |
| B.O→Cu的配位键键能小于N→Cu的配位键键能 |
| C.顺式甘氨酸铜溶解度小于反式甘氨酸铜 |
| D.甘氨酸铜晶体中相邻微粒通过范德华力相连,堆积成超分子 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】许多过渡金属离子能形成种类繁多的配合物。下列说法正确的是


A.二乙二胺合铜配离子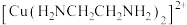 的结构如图所示,可知 的结构如图所示,可知 的配位数为4,配体数也为4 的配位数为4,配体数也为4 |
B.由反应 ,可知配位能力: ,可知配位能力: |
C. 配合物中含有5mol配位键 配合物中含有5mol配位键 |
D.配合物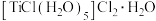 中心离子为 中心离子为 ,1mol该配合物与 ,1mol该配合物与 溶液作用,生成3molAgCl 溶液作用,生成3molAgCl |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】已知联氨(N2H4)为二元弱碱,常温下将盐酸滴加到联氨(N2H4)的水溶液中,混合溶液中微粒的物质的量分数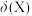 随
随 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是

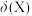 随
随 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是
A.反应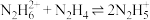 的 的 (已知 (已知 ) ) |
B.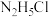 溶液中存在: 溶液中存在: |
C.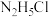 溶液中: 溶液中: |
D. |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】已知25℃时,Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5,Ka(HF)=3.5×10-4,进行如下实验:
①测定0.1000mol•L-1Na2C2O4溶液pH=8.4;
②向5mL0.1000mol•L-1NaF溶液中,滴加5滴0.1000mol•L-1H2C2O4溶液;
③向0.1000mol•L-1H2C2O4溶液中滴加NaOH溶液至溶液pH=3;
④向0.1000mol•L-1Na2C2O4溶液中滴加同浓度同体积的稀盐酸。
下列说法不正确 的是
①测定0.1000mol•L-1Na2C2O4溶液pH=8.4;
②向5mL0.1000mol•L-1NaF溶液中,滴加5滴0.1000mol•L-1H2C2O4溶液;
③向0.1000mol•L-1H2C2O4溶液中滴加NaOH溶液至溶液pH=3;
④向0.1000mol•L-1Na2C2O4溶液中滴加同浓度同体积的稀盐酸。
下列说法
A.实验①溶液中存在:c(C2O )>c(HC2O )>c(HC2O )>c(H2C2O4) )>c(H2C2O4) |
| B.实验②反应的化学方程式为:NaF+H2C2O4=HF+NaHC2O4 |
C.实验③所得溶液中:c(C2O )<c(H2C2O4) )<c(H2C2O4) |
D.实验④所得溶液中:c(H+)+c(H2C2O4)=c(C2O )+c(OH-) )+c(OH-) |
您最近一年使用:0次




 溶液用
溶液用 溶液调节pH,溶液中
溶液调节pH,溶液中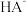 及
及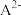 的物质的量浓度变化如图所示。下列说法错误的是
的物质的量浓度变化如图所示。下列说法错误的是


 的
的
 溶液中:
溶液中: