解题方法
1 . 下列离子方程式正确的是
A.氨气溶于醋酸溶液:NH3+H+=NH |
B.碳酸钙与稀盐酸反应:CO +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
C.硫酸铜溶液与氢氧化钡溶液反应:SO +Ba2+=BaSO4↓ +Ba2+=BaSO4↓ |
| D.向氯化铜溶液中通入硫化氢气体:Cu2++H2S=CuS↓+2H+ |
您最近一年使用:0次
解题方法
2 . 中国政府承诺:力争 的排放在2030年前实现“碳达峰”,2060年前实现“碳中和”。
的排放在2030年前实现“碳达峰”,2060年前实现“碳中和”。 的捕集与利用成为当前研究的热点。
的捕集与利用成为当前研究的热点。
Ⅰ.“氨法”捕集二氧化碳是实现“碳中和”的重要途径之一
反应的化学方程式为: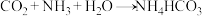 。
。
完成下列填空:
(1)写出氮原子的核外电子排布式_______ ,写出 分子的电子式
分子的电子式_______ 。
(2)用方程式表示二氧化碳溶于水溶液呈现酸性的原因_______ 。
(3)组成 的四种元素中,由其中任意两种元素组成且含非极性键的分子可以是
的四种元素中,由其中任意两种元素组成且含非极性键的分子可以是_______ (写出一种,下同);由其中任意三种元素组成的离子化合物可以是_______ 。
(4)上述氨法吸收废气中 时,一般温度控制在30℃,用化学方程式表示温度不宜太高的原因。
时,一般温度控制在30℃,用化学方程式表示温度不宜太高的原因。_______
Ⅱ.我国化学家研究在铜基催化剂作用下将 高效转化为甲酸,合成铜基催化剂时有一步反应为:
高效转化为甲酸,合成铜基催化剂时有一步反应为: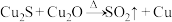 (未配平)。
(未配平)。
(5)配平上述化学方程式_______ 。若反应中转移 电子,则生成气体在标准状态下的体积为
电子,则生成气体在标准状态下的体积为_______ L。
 的排放在2030年前实现“碳达峰”,2060年前实现“碳中和”。
的排放在2030年前实现“碳达峰”,2060年前实现“碳中和”。 的捕集与利用成为当前研究的热点。
的捕集与利用成为当前研究的热点。Ⅰ.“氨法”捕集二氧化碳是实现“碳中和”的重要途径之一
反应的化学方程式为:
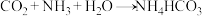 。
。完成下列填空:
(1)写出氮原子的核外电子排布式
 分子的电子式
分子的电子式(2)用方程式表示二氧化碳溶于水溶液呈现酸性的原因
(3)组成
 的四种元素中,由其中任意两种元素组成且含非极性键的分子可以是
的四种元素中,由其中任意两种元素组成且含非极性键的分子可以是(4)上述氨法吸收废气中
 时,一般温度控制在30℃,用化学方程式表示温度不宜太高的原因。
时,一般温度控制在30℃,用化学方程式表示温度不宜太高的原因。Ⅱ.我国化学家研究在铜基催化剂作用下将
 高效转化为甲酸,合成铜基催化剂时有一步反应为:
高效转化为甲酸,合成铜基催化剂时有一步反应为: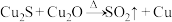 (未配平)。
(未配平)。(5)配平上述化学方程式
 电子,则生成气体在标准状态下的体积为
电子,则生成气体在标准状态下的体积为
您最近一年使用:0次
名校
解题方法
3 . 下列化学用语对事实的表述不正确 的是
A.硬脂酸与乙醇的酯化反应: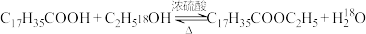 |
B.常温时, 氨水的 氨水的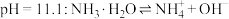 |
C.由Na和Cl形成离子键的过程: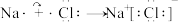 |
D.电解精炼铜的阴极反应: |
您最近一年使用:0次
名校
解题方法
4 . 酸的强弱除与本身性质有关外,还与溶剂有关。HA和HB在水中皆为弱酸,且酸性HA<HB,在液氨中两者皆为强酸。则下列表述正确的是
| A.液氨中:NaA+HCl→NaCl+HA | B.水溶液中:NaB+HA→NaA+HB |
| C.液氨中:HB→H++B- | D.水溶液中的pH:NaA<NaB |
您最近一年使用:0次
解题方法
5 . Li-SOCl2电池采用LiAlCl4的SOCl2溶液为电解质溶液,是目前比能量最高的化学电源,具有电压高.储存寿命长.工作温度范围宽.成本低等优点。
(1)该电池的工作原理为:4Li+2SOCl2=4LiCl↓+SO2↑+S↓,该反应的还原产物为__________ ,若生成标准状况下气体11.2L,则转移电子的数目为_____________ ;
(2)SOCl2可用于AlCl3·6H2O制备无水AlCl3,请结合离子方程式解释不采用直接加热晶体的方法除去结晶水的原因_____________________________________________________________ ;
(3)解释Li-SOCl2电池组装必须在无水条件下的原因_______________________________ ;
(4)工业制硫酸中,SO2的催化氧化采用常压而不是高压的原因______________________ ;
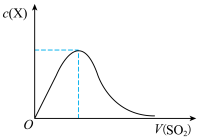
(5)向NaOH溶液中缓慢通入SO2至过量,反应过程中某微粒X的物质的量浓度随着通入SO2体积的变化如图所示,该微粒X为_____________ ,SO2过量时溶液仍然存在微粒X的原因____________________________ 。
(1)该电池的工作原理为:4Li+2SOCl2=4LiCl↓+SO2↑+S↓,该反应的还原产物为
(2)SOCl2可用于AlCl3·6H2O制备无水AlCl3,请结合离子方程式解释不采用直接加热晶体的方法除去结晶水的原因
(3)解释Li-SOCl2电池组装必须在无水条件下的原因
(4)工业制硫酸中,SO2的催化氧化采用常压而不是高压的原因
(5)向NaOH溶液中缓慢通入SO2至过量,反应过程中某微粒X的物质的量浓度随着通入SO2体积的变化如图所示,该微粒X为

您最近一年使用:0次
解题方法
6 . 用碳化铝制取甲烷的化学方程式为:Al4C3+12H2O=4Al(OH)3↓+3CH4↑。下列有关化学用语表示正确的是( )
| A.铝离子的电子排布式:1s22s22p63s23p1 |
| B.水分子的结构式:H—O—H |
C.甲烷的比例模型: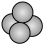 |
| D.氢氧化铝的电离方程式:H++AlO2-+H2O=Al(OH)3=Al3++3OH- |
您最近一年使用:0次
13-14高三上·上海·阶段练习
解题方法
7 . 双氧水是二元弱酸,则下列有关化学用语使用正确的是
A.H2O2的电子式: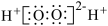 |
| B.双氧水的电离方程式为H2O2⇌H+ + HO2- |
| C.16O22-离子中,质量数之和是电子数之和的两倍 |
| D.将双氧水溶液加热升温后,溶液pH一定减小 |
您最近一年使用:0次
解题方法
8 . 磷有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产中的还原剂。完成下列填空:
(1)H3PO2是一元中 强酸,写出其电离方程式:_______ ;请将NaH2PO2溶液中的各离子按浓度由大到小的顺序排列:__________ 。
(2)室温下0.1mol/L的NaH2PO2溶液和0.1mol/L的Na2CO3溶液,pH更大的是_______ ,其原因是__________ 。
(3)化学镀银,可利用H3PO2把溶液中的Ag+还原为银的反应,已知该反应中还原剂与氧化剂的物质的量之比为1:4,则氧化产物是_______ (填化学式)。
(4)工业上可用白磷(P4)与Ba(OH)2溶液反应生成PH3和Ba(H2PO2)2。写出并配平该反应的化学方程式________ ,若反应中转移电子6NA,用去还原剂_____ mol。再向Ba(H2PO2)2溶液中加入盐酸制备H3PO2,有人说应该用硫酸代替盐酸,请说明用硫酸代替盐酸的优点:_______ 。
(5)下图是利用电解原理制备H3PO2的示意图(阳离子交换膜和阴离子交换膜分别只允许阳、阴离子通过;已知电极反应为:

阳极 4OH--4e→O2↑+ H2O
阴极 2H+ + 2e→H2↑):
分析在阳极室得到H3PO2原因:_______ 。
(1)H3PO2是
(2)室温下0.1mol/L的NaH2PO2溶液和0.1mol/L的Na2CO3溶液,pH更大的是
(3)化学镀银,可利用H3PO2把溶液中的Ag+还原为银的反应,已知该反应中还原剂与氧化剂的物质的量之比为1:4,则氧化产物是
(4)工业上可用白磷(P4)与Ba(OH)2溶液反应生成PH3和Ba(H2PO2)2。写出并配平该反应的化学方程式
(5)下图是利用电解原理制备H3PO2的示意图(阳离子交换膜和阴离子交换膜分别只允许阳、阴离子通过;已知电极反应为:

阳极 4OH--4e→O2↑+ H2O
阴极 2H+ + 2e→H2↑):
分析在阳极室得到H3PO2原因:
您最近一年使用:0次
解题方法
9 . 室温下,0.2mol/L的一元碱BOH与等浓度的盐酸等体积混合后,所得溶液中部分微粒的组分及浓度如图所示,下列对混合溶液的分析正确的是
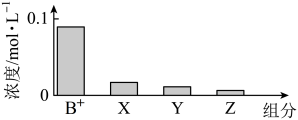

| A.溶液显酸性 |
| B.升温,c(X)增大,c(Y)减小 |
| C.c(B+) + c(Y) = c(Cl-) |
| D.稀释溶液,c(X)增大,c(Z)增大 |
您最近一年使用:0次
10 . 下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)( )
A.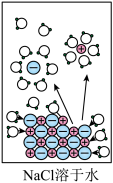 NaCl→Na++Cl- NaCl→Na++Cl- |
B. CuCl→Cu2++2Cl- CuCl→Cu2++2Cl- |
C.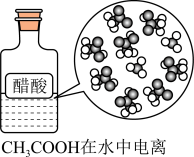 CH3COOH⇌CH3COO-+H+ CH3COOH⇌CH3COO-+H+ |
D.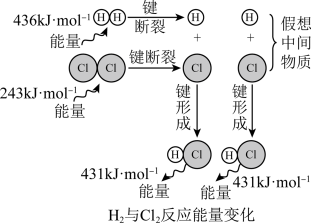 H2 (g)+Cl2(g)→2HCl(g)+183kJ H2 (g)+Cl2(g)→2HCl(g)+183kJ |
您最近一年使用:0次



