解题方法
1 . 久置的硝酸银溶液,试剂瓶底部有黑色固体A,瓶口和瓶壁上有黑色固体B。
已知:①硝酸银见光或受热会分解,分解产物相同。
②氧化银为棕黑色粉末,难溶于水,可溶于氨水和稀硝酸,见光或200℃左右分解生成氧气。
③AgOH不稳定,极易分解生成 和
和 。
。
某兴趣小组开展以下探究活动。
Ⅰ.探究硝酸银固体受热分解的产物
利用下列装置(夹持仪器略去)进行实验。
(1)仪器e名称为___________ ,试管b的主要作用是___________ 。
(2)试管a中反应的化学方程式为___________ 。
Ⅱ.探究A、B的成分
【提出猜想】甲、乙同学猜想固体中含有Ag、 中的一种或两种。
中的一种或两种。
(3)从化学变化角度,甲、乙同学猜想固体中可能含有 的依据是
的依据是___________ 。
【进行实验】甲、乙分别对固体A、B按以下步骤进行实验。
i.取少量固体于试管中;
ii.加入过量氨水,振荡;
iii.……
【形成结论】甲得出固体A为Ag和 的混合物,乙得出固体B为Ag。
的混合物,乙得出固体B为Ag。
(4)①甲同学步骤ⅱ观察到的现象为___________ ,相应的化学方程式为___________ 。
②乙同学步骤ⅲ加入的试剂为___________ (填名称)。
【反思与应用】
(5)固体A与固体B成分不同的可能原因是___________ 。
(6)实验室保存硝酸银溶液采取的措施为___________ (写出两条)。
已知:①硝酸银见光或受热会分解,分解产物相同。
②氧化银为棕黑色粉末,难溶于水,可溶于氨水和稀硝酸,见光或200℃左右分解生成氧气。
③AgOH不稳定,极易分解生成
 和
和 。
。某兴趣小组开展以下探究活动。
Ⅰ.探究硝酸银固体受热分解的产物
利用下列装置(夹持仪器略去)进行实验。

(1)仪器e名称为
(2)试管a中反应的化学方程式为
Ⅱ.探究A、B的成分
【提出猜想】甲、乙同学猜想固体中含有Ag、
 中的一种或两种。
中的一种或两种。(3)从化学变化角度,甲、乙同学猜想固体中可能含有
 的依据是
的依据是【进行实验】甲、乙分别对固体A、B按以下步骤进行实验。
i.取少量固体于试管中;
ii.加入过量氨水,振荡;
iii.……
【形成结论】甲得出固体A为Ag和
 的混合物,乙得出固体B为Ag。
的混合物,乙得出固体B为Ag。(4)①甲同学步骤ⅱ观察到的现象为
②乙同学步骤ⅲ加入的试剂为
【反思与应用】
(5)固体A与固体B成分不同的可能原因是
(6)实验室保存硝酸银溶液采取的措施为
您最近一年使用:0次
2024-04-01更新
|
629次组卷
|
5卷引用:福建省莆田市2024届高三下学期毕业班二模考试化学试题
福建省莆田市2024届高三下学期毕业班二模考试化学试题(已下线)题型9 实验综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届陕西省渭南市临渭区高三下学期三模理综试题-高中化学2024届陕西省渭南市富平县高三下学期二模理综试题-高中化学(已下线)压轴题12?化学实验综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
解题方法
2 . 贵金属银有广泛用途。工业上用银锰精矿(主要含 、MnS、
、MnS、 等)制备银,同时获得二氧化锰的流程如下。
等)制备银,同时获得二氧化锰的流程如下。
(1)“浸锰”步骤中产生的浸锰液主要含有 ,生成气体的主要成分为
,生成气体的主要成分为_______ ;用惰性电极电解浸锰液制 ,写出电解总反应的化学方程式
,写出电解总反应的化学方程式_______ 。
(2)已知“浸铁”步骤中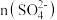 保持不变,反应中n(氧化剂):n(还原剂)=
保持不变,反应中n(氧化剂):n(还原剂)=_______ ;浸铁滤饼的主要成分为S和_______ 。
(3)“浸银”时发生反应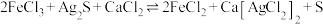 ,其中
,其中 在溶液中是一种稳定配合物。加入
在溶液中是一种稳定配合物。加入 的作用是
的作用是_______ ;结合离子方程式,从平衡角度分析选用氯化物浓溶液的原因是_______ 。
(4)“沉银”步骤中,生成单质银的离子反应方程式为_______ ,沉银液经处理可再利用,方法是向沉银液中通入_______ (写化学式),通过一步转化后循环再用。
 、MnS、
、MnS、 等)制备银,同时获得二氧化锰的流程如下。
等)制备银,同时获得二氧化锰的流程如下。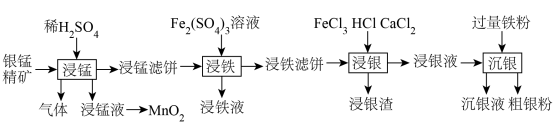
(1)“浸锰”步骤中产生的浸锰液主要含有
 ,生成气体的主要成分为
,生成气体的主要成分为 ,写出电解总反应的化学方程式
,写出电解总反应的化学方程式(2)已知“浸铁”步骤中
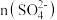 保持不变,反应中n(氧化剂):n(还原剂)=
保持不变,反应中n(氧化剂):n(还原剂)=(3)“浸银”时发生反应
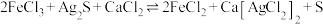 ,其中
,其中 在溶液中是一种稳定配合物。加入
在溶液中是一种稳定配合物。加入 的作用是
的作用是(4)“沉银”步骤中,生成单质银的离子反应方程式为
您最近一年使用:0次
名校
解题方法
3 . 《清波杂志》卷十二记载:信州铅山胆水自山下注,势若瀑布,用以浸铜,……。古传一人至水滨,遗匙钥,翌日得之,已成铜矣。下列说法正确的是
| A.胆水为强电解质 |
| B.胆水呈碱性 |
| C.向胆水中加入过量氨水,有蓝色沉淀生成 |
| D.浸铜时发生置换反应 |
您最近一年使用:0次
名校
4 . 利用下列装置和试剂进行实验,能达到实验目的的是


| A.用装置甲测定盐酸的浓度 | B.用装置乙验证苯和溴发生取代反应 |
C.用装置丙制备无水 | D.用装置丁在铁片上镀铜 |
您最近一年使用:0次
名校
5 . 下列说法错误的是
| A.除去MgCl2酸性溶液中的Fe3+,可加入MgO调节pH使Fe3+转化为Fe(OH)3沉淀 |
| B.将AlCl3溶液蒸干灼烧,可得到AlCl3 |
| C.实验室盛放Na2CO3、Na2SiO3溶液的试剂瓶应用橡皮塞,而不能用玻璃塞 |
D.泡沫灭火器原理:Al3++3 =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
您最近一年使用:0次
名校
6 . 下列有关说法正确的是


| A.BeF2和BeCl2均为离子化合物 |
| B.BeO的晶胞如图所示,晶胞中O2-的配位数为4 |
| C.ⅡA族元素形成的氧化物均能与冷水直接化合成强碱 |
| D.在空气中加热蒸发BeCl2和MgCl2溶液都能得到BeCl2和MgCl2固体 |
您最近一年使用:0次
解题方法
7 . 用含铁废铜制备胆矾的流程如图所示,下列说法正确的是


A.“溶解”中加 仅发生反应 仅发生反应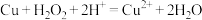 |
B.流程中 可用 可用 代替 代替 |
C.系列操作中加硫酸的作用是抑制 水解 水解 |
| D.“系列操作”是指蒸发结晶,趁热过滤,洗涤,干燥 |
您最近一年使用:0次
解题方法
8 . 三草酸合铁(Ⅲ)酸钾晶体{ ,
,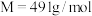 },为翠绿色单斜晶体,溶于水,难溶于乙醇,是一些有机反应的催化剂。实验室制备该晶体具体步骤如下:
},为翠绿色单斜晶体,溶于水,难溶于乙醇,是一些有机反应的催化剂。实验室制备该晶体具体步骤如下:
Ⅰ.制备
ⅰ.称 摩尔盐[
摩尔盐[ ,
, ]放入
]放入 水中。再加入
水中。再加入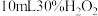 溶液,搅拌,微热。
溶液,搅拌,微热。
ⅱ.继续加入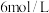 氨水(过量),加热,不断搅拌,煮沸后静置,倾去上层清液,抽滤得
氨水(过量),加热,不断搅拌,煮沸后静置,倾去上层清液,抽滤得 沉淀。
沉淀。
Ⅱ.制备
ⅲ.称取 和
和 加入盛有
加入盛有 水的烧杯中,加热使其完全溶解后,搅拌,将步骤ⅱ制取的
水的烧杯中,加热使其完全溶解后,搅拌,将步骤ⅱ制取的 加入此溶液中。加热,使
加入此溶液中。加热,使 溶解,溶液呈翠绿色。
溶解,溶液呈翠绿色。
ⅳ.过滤,将滤液浓缩。浓缩液转移至 烧杯中,后进行操作a。将得到的晶体分别用少量水和
烧杯中,后进行操作a。将得到的晶体分别用少量水和 乙醇洗涤,干燥,称量晶体质量为
乙醇洗涤,干燥,称量晶体质量为 。
。
回答下列问题:
(1)步骤ⅰ中使用部分仪器如下:

仪器A的名称是___________ ,微热时,温度不能过高的原因是___________ 。
(2)已知:二价铁在碱性介质中比酸性介质中更易氧化。摩尔盐相比硫酸亚铁不易变质的原因是___________ 。
(3)步骤ⅱ中,制备 加热煮沸的目的是
加热煮沸的目的是___________ 。
(4)步骤ⅲ中,写出将氢氧化铁加入溶液的离子方程式___________ 。
(5)已知三草酸合铁(Ⅲ)酸钾与氢氧化钾溶解性曲线如下图所示,步骤ⅰ中操作 为
为___________ 。

(6)用95%乙醇洗涤晶体的目的为___________ 。
(7)该实验的产率为___________  (保留1位小数)。
(保留1位小数)。
 ,
,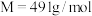 },为翠绿色单斜晶体,溶于水,难溶于乙醇,是一些有机反应的催化剂。实验室制备该晶体具体步骤如下:
},为翠绿色单斜晶体,溶于水,难溶于乙醇,是一些有机反应的催化剂。实验室制备该晶体具体步骤如下:Ⅰ.制备

ⅰ.称
 摩尔盐[
摩尔盐[ ,
, ]放入
]放入 水中。再加入
水中。再加入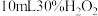 溶液,搅拌,微热。
溶液,搅拌,微热。ⅱ.继续加入
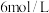 氨水(过量),加热,不断搅拌,煮沸后静置,倾去上层清液,抽滤得
氨水(过量),加热,不断搅拌,煮沸后静置,倾去上层清液,抽滤得 沉淀。
沉淀。Ⅱ.制备

ⅲ.称取
 和
和 加入盛有
加入盛有 水的烧杯中,加热使其完全溶解后,搅拌,将步骤ⅱ制取的
水的烧杯中,加热使其完全溶解后,搅拌,将步骤ⅱ制取的 加入此溶液中。加热,使
加入此溶液中。加热,使 溶解,溶液呈翠绿色。
溶解,溶液呈翠绿色。ⅳ.过滤,将滤液浓缩。浓缩液转移至
 烧杯中,后进行操作a。将得到的晶体分别用少量水和
烧杯中,后进行操作a。将得到的晶体分别用少量水和 乙醇洗涤,干燥,称量晶体质量为
乙醇洗涤,干燥,称量晶体质量为 。
。回答下列问题:
(1)步骤ⅰ中使用部分仪器如下:

仪器A的名称是
(2)已知:二价铁在碱性介质中比酸性介质中更易氧化。摩尔盐相比硫酸亚铁不易变质的原因是
(3)步骤ⅱ中,制备
 加热煮沸的目的是
加热煮沸的目的是(4)步骤ⅲ中,写出将氢氧化铁加入溶液的离子方程式
(5)已知三草酸合铁(Ⅲ)酸钾与氢氧化钾溶解性曲线如下图所示,步骤ⅰ中操作
 为
为
(6)用95%乙醇洗涤晶体的目的为
(7)该实验的产率为
 (保留1位小数)。
(保留1位小数)。
您最近一年使用:0次
名校
解题方法
9 . 常温下,下列各组离子在指定溶液中能大量共存的是
A.无色透明的溶液中:Cu2+、Na+、 、 、 |
B.AlCl3溶液中:Ba2+、Mn2+、 、 、 |
C.酸性溶液中:Fe2+、 、 、 、 、 |
D.使酚酞试液呈红色的溶液中:Na+、K+、 、 、 |
您最近一年使用:0次
名校
解题方法
10 . 已知液氨的电离类似水的电离,碳酸钠在液氨中完全电离并发生类似水解的氨解。肼( )为二元弱碱,在水中的电离方程式与氨相似。下列说法错误的是
)为二元弱碱,在水中的电离方程式与氨相似。下列说法错误的是
 )为二元弱碱,在水中的电离方程式与氨相似。下列说法错误的是
)为二元弱碱,在水中的电离方程式与氨相似。下列说法错误的是A.元素的电负性: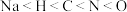 |
B.肼在水中第一步电离的方程式为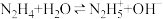 |
C.肼与硫酸反应生成的酸式盐中阳离子的电子式为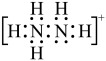 |
D.碳酸钠在液氨中第一步氨解的离子方程式为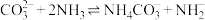 |
您最近一年使用:0次



