名校
解题方法
1 . 下列实验设计不能 达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 向NaAlO2溶液中加入NaHCO3溶液,观察到有白色沉淀生成 | 证明AlO 得质子的能力强于CO 得质子的能力强于CO |
| B | 工业酒精制备无水乙醇 | 工业酒精中加生石灰,蒸馏 |
| C | 检验NH3 | 用湿润的红色石蕊试纸检验 |
| D | 向NaCl、NaI的混合溶液中滴加少量AgNO3溶液,生成淡黄色沉淀 | 证明Ksp(AgCl) > Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下表中根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向某溶液中滴加少量酚酞 | 溶液变红 | 该溶液一定是碱溶液 |
| B | 向某溶液中滴加少量盐酸 | 产生白色沉淀 | 原溶液中一定含有Ag+ |
| C | 将某气体通入品红溶液中 | 溶液褪色 | 该气体一定是SO2 |
| D | 向饱和AgCl溶液中加入NaCl固体 | 产生白色沉淀 | AgCl溶液中存在沉淀溶解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
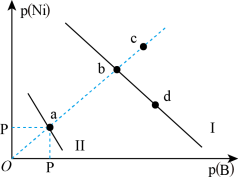
3 . 已知298K时,Ksp(NiS)=1.0×10-21,Ksp(NiCO3)=1.0×10-7;p(Ni)=-lgc(Ni2+),p(B)=-lgc(S2-)或-lgc(CO )。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
 )。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
| A.常温下NiCO3的溶解度大于NiS的溶解度 |
| B.向d点对应的溶液中加入对应阴离子的钠盐,d点向b点移动 |
| C.对于曲线Ⅰ,在b点加热,b点向c点移动 |
D.P为3.5且对应的阴离子是CO |
您最近一年使用:0次
2021-09-05更新
|
3105次组卷
|
42卷引用:专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题
(已下线)专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)小题22 难溶电解质的溶解平衡——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)2021年高考全国乙卷化学试题变式题陕西省宝鸡市陈仓区2022届高三上学期第一次教学质量检测化学试题湖北省宜昌英杰学校2021-2022学年高三上学期10月月考化学试题四川省资阳市高中2018届高三第二次诊断性考试理科综合化学试题西北师大附中2018届下学期高三年级第二次模拟理综化学试卷西藏自治区拉萨中学2018届高三第七次月考理综化学试题【全国市级联考】河北省保定市2018届高三第二次模拟考试理科综合化学试题【全国市级联考】江西省南昌市2018届高三第三次模拟考试理综化学试题【全国百强校】广东省阳春市第一中学2018届高三第九次月考理综化学试题【市级联考】湖北省十堰市2019届高三下学期模拟化学试题四川省泸县第四中学2019届高三下学期三诊模拟理科综合化学试题辽宁省六校协作体2020届高三上学期期中考试化学试题福建省厦门外国语学校2020届高三12月月考化学试题2020届高三化学化学二轮复习——常考题型:沉淀溶解平衡的曲线分析【精编25题】吉林省梅河口市第五中学2020届高三下学期模拟考试化学试题(已下线)考点13 沉淀溶解平衡-2020年高考化学命题预测与模拟试题分类精编(已下线)易错17 难溶电解质的溶解平衡及应用-备战2021年高考化学一轮复习易错题选择性必修1(SJ)专题3专题培优专练选择性必修1 化学反应原理综合训练(已下线)3.4.2 沉淀溶解平衡原理的应用-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)江西省九江市第一中学2021-2022学年高二上学期第二次月考化学试题(已下线)【直击双一流】06-备战2022年高考化学名校进阶模拟卷(通用版)湖南省株洲市第一中学2021-2022学年高三下学期期中考试化学试题(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型27 沉淀溶解平衡常数及其应用图象(已下线)T13-溶液中的离子平衡浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题步步为赢 高二化学寒假作业:综合检测(一)鲁科版(2019)选择性必修1化学反应原理 综合训练高中必刷题高二选择性必修1化学反应原理综合训练(已下线)3.4+难溶电解质的溶解平衡-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)第三章 水溶液中的离子平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过素养 学科素养拓展训练人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 过素养 学科素养拓展训练山东省临朐县实验中学2020-2021学年高二上学期12月月结学情检测化学试题陕西省汉中中学2021-2022学年高二上学期第四次月考化学试题吉林省长春市第五中学2022-2023学年高二上学期期中考试化学试题
2021高三·全国·专题练习
名校
4 . 在25℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16.下列叙述正确的是
| A.饱和AgCl、AgI溶液中所含Ag+的浓度相同 |
| B.向饱和AgCl溶液中加入盐酸,Ksp大 |
| C.向AgCl的悬浊液中加入KI溶液,白色沉淀转化为黄色 |
| D.向含相同物质的量浓度的Cl-和I-的溶液中逐滴加入AgNO3溶液,Cl-先沉淀 |
您最近一年使用:0次
2021-09-05更新
|
433次组卷
|
4卷引用:课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)
(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)辽宁省铁岭市清河高级中学2021-2022学年高二上学期第一次阶段考试化学试题(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)辽宁省葫芦岛市2022~2023 学年高二上学期学业质量监测化学试题
2021高三·全国·专题练习
名校
5 . 已知如下物质的溶度积常数:Ksp(FeS)=6.3×10-18,Ksp(CuS)=6.3×10-36.下列说法正确的是
| A.同温度下,CuS的溶解度大于FeS的溶解度 |
| B.同温度下,向饱和FeS溶液中加入少量Na2S固体后,Ksp(FeS)变小 |
| C.向含有等物质的量的FeCl2和CuCl2的混合溶液中逐滴加入Na2S溶液,最先出现的沉淀是FeS |
| D.除去工业废水中的Cu2+和Hg2+,可以选用FeS作沉淀剂 |
您最近一年使用:0次
2021-09-05更新
|
1120次组卷
|
10卷引用:课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)
(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题27 难溶电解质的溶解平衡(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)第三章第四节 难溶电解的溶解平衡(备作业)-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)黑龙江省哈尔滨师范大学青冈实验中学2021-2022学年高二10月月考化学试题(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)期末综合测试卷02-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)(已下线)3.4.2 沉淀溶解平衡原理的应用-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)第三章 水溶液中的离子平衡-2021-2022学年高二化学课后培优练(人教版选修4)江西省南昌市知行中学2021-2022学年高二上学期12月月考化学试题新疆乌鲁木齐市第四中学2021-2022学年高二上学期期末考试化学试题
解题方法
6 . 含钙物质在生产生活中发挥着重要作用,如 、
、 等。
等。
(1)菠菜成分测定中常用 为沉淀剂。菠菜中含有的草酸以
为沉淀剂。菠菜中含有的草酸以 、
、 、
、 存在,三种微粒之和称为总草酸。某研究小组测定菠菜中总草酸含量,进行如下实验。
存在,三种微粒之和称为总草酸。某研究小组测定菠菜中总草酸含量,进行如下实验。
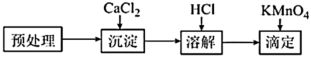
①在“预处理”步骤,将菠菜碾碎后预处理,得含总草酸的溶液( ),该步骤
),该步骤依次 需要的装置有_______ 。
②在“沉淀”步骤,调节 至溶液弱碱性,再滴加足量
至溶液弱碱性,再滴加足量 溶液,产生白色沉淀,过滤得到
溶液,产生白色沉淀,过滤得到 固体。“调节溶液至弱碱性”的目的是
固体。“调节溶液至弱碱性”的目的是_______ 。
草酸溶液中微粒的物质的量分数随溶液 变化如图所示:
变化如图所示:
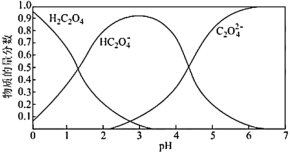
③在“溶解”步骤,稀 溶解
溶解 ,所得溶液
,所得溶液 ,该步骤主要反应的离子方程式是:
,该步骤主要反应的离子方程式是:_______ 。
④在“滴定”步骤,用 标准溶液滴定
标准溶液滴定 次,判断达到滴定终点的现象是
次,判断达到滴定终点的现象是_______ 。
(2) 的饱和石灰水,加热至
的饱和石灰水,加热至 ,发现溶液变浑浊,且加热过程中并未见水分蒸发,现探究溶液变浑浊的原因。
,发现溶液变浑浊,且加热过程中并未见水分蒸发,现探究溶液变浑浊的原因。
提出猜想。
猜想a: 的溶解度随温度升高而减小,升温的过程中析出
的溶解度随温度升高而减小,升温的过程中析出 。
。
猜想b:温度变化的过程中, 变质,使溶液变浑浊。
变质,使溶液变浑浊。
设计实验,验证猜想。
提供 下的
下的 饱和溶液Ⅰ、
饱和溶液Ⅰ、 下的
下的 饱和溶液Ⅱ。
饱和溶液Ⅱ。
①查阅资料: 时,
时,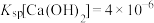 ,
,
_______  。
。
②上述实验结果是 ,是否可以证明猜想a成立,
,是否可以证明猜想a成立,_______ (填“是”或“否”)。
③进一步验证猜想b,补充实验3,填写在答题卡上_______ 。
(3)实验总结。
根据实验 的结果,可以判断猜想b成立。猜想b成立的判断依据是
的结果,可以判断猜想b成立。猜想b成立的判断依据是_______ 。
 、
、 等。
等。(1)菠菜成分测定中常用
 为沉淀剂。菠菜中含有的草酸以
为沉淀剂。菠菜中含有的草酸以 、
、 、
、 存在,三种微粒之和称为总草酸。某研究小组测定菠菜中总草酸含量,进行如下实验。
存在,三种微粒之和称为总草酸。某研究小组测定菠菜中总草酸含量,进行如下实验。
①在“预处理”步骤,将菠菜碾碎后预处理,得含总草酸的溶液(
 ),该步骤
),该步骤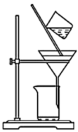 | 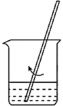 | 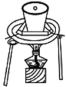 | 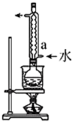 |
| A | B | C | D |
 至溶液弱碱性,再滴加足量
至溶液弱碱性,再滴加足量 溶液,产生白色沉淀,过滤得到
溶液,产生白色沉淀,过滤得到 固体。“调节溶液至弱碱性”的目的是
固体。“调节溶液至弱碱性”的目的是草酸溶液中微粒的物质的量分数随溶液
 变化如图所示:
变化如图所示:
③在“溶解”步骤,稀
 溶解
溶解 ,所得溶液
,所得溶液 ,该步骤主要反应的离子方程式是:
,该步骤主要反应的离子方程式是:④在“滴定”步骤,用
 标准溶液滴定
标准溶液滴定 次,判断达到滴定终点的现象是
次,判断达到滴定终点的现象是(2)
 的饱和石灰水,加热至
的饱和石灰水,加热至 ,发现溶液变浑浊,且加热过程中并未见水分蒸发,现探究溶液变浑浊的原因。
,发现溶液变浑浊,且加热过程中并未见水分蒸发,现探究溶液变浑浊的原因。提出猜想。
猜想a:
 的溶解度随温度升高而减小,升温的过程中析出
的溶解度随温度升高而减小,升温的过程中析出 。
。猜想b:温度变化的过程中,
 变质,使溶液变浑浊。
变质,使溶液变浑浊。设计实验,验证猜想。
提供
 下的
下的 饱和溶液Ⅰ、
饱和溶液Ⅰ、 下的
下的 饱和溶液Ⅱ。
饱和溶液Ⅱ。| 实验序号 | 试样 | 测试温度/℃ | 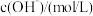 |
 | Ⅰ: 的 的 饱和溶液 饱和溶液 | 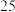 |  |
 | Ⅱ: 的 的 饱和溶液 饱和溶液 | 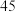 |  |
 | _______ | _______ | 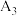 |
 时,
时,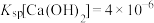 ,
,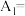
 。
。②上述实验结果是
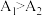 ,是否可以证明猜想a成立,
,是否可以证明猜想a成立,③进一步验证猜想b,补充实验3,填写在答题卡上
(3)实验总结。
根据实验
 的结果,可以判断猜想b成立。猜想b成立的判断依据是
的结果,可以判断猜想b成立。猜想b成立的判断依据是
您最近一年使用:0次
名校
7 . 甲、乙两物质的溶解度曲线如图所示,下列说法不正确的是
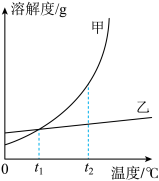

| A.甲溶于水,一定明显放热 |
B. ℃时,甲、乙的溶解度相同 ℃时,甲、乙的溶解度相同 |
C.分别将等质量的甲、乙饱和溶液从 ℃降至 ℃降至 ℃,析出固体(不含结晶水)的质量甲一定多于乙 ℃,析出固体(不含结晶水)的质量甲一定多于乙 |
| D.从甲的溶液中(含少量杂质)将甲固体结晶的操作为:加热浓缩、冷却结晶 |
您最近一年使用:0次
解题方法
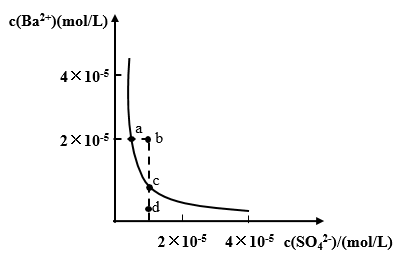
8 . 一定条件下,BaSO4在溶液中达到溶解平衡时存在溶度积常数Ksp=c(Ba2+)·c( )某温度时,溶液中c(Ba2+)与c(
)某温度时,溶液中c(Ba2+)与c( )的关系曲线如下图所示。下列说法正确的是
)的关系曲线如下图所示。下列说法正确的是
 )某温度时,溶液中c(Ba2+)与c(
)某温度时,溶液中c(Ba2+)与c( )的关系曲线如下图所示。下列说法正确的是
)的关系曲线如下图所示。下列说法正确的是
| A.加入Na2SO4可以使溶液由a点交到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.d点无BaSO4沉淀生成 |
| D.a点对应的Ksp大于c点对应的Ksp |
您最近一年使用:0次
2021高三·全国·专题练习
名校
解题方法
9 . 已知:298 K时,物质的溶度积如表所示。
下列说法正确的是
| 化学式 | CH3COOAg | AgCl | Ag2CrO4 | Ag2S |
| Ksp | 2.3×10-3 | 1.56×10-10 | 1.12×10-12 | 6.7×10-15 |
| A.将0.001 mol·L-1的AgNO3溶液逐滴滴入0.001 mol·L-1的KCl和0.001 mol·L-1的K2CrO4的混合液中,则先产生Ag2CrO4沉淀 |
| B.向2.0×10-4 mol·L-1的K2CrO4溶液中加入等体积的2.0×10-4 mol·L-1的AgNO3溶液,则有Ag2CrO4沉淀生成(忽略混合时溶液体积的变化) |
| C.向CH3COOAg悬浊液中加入盐酸,发生反应的离子方程式为CH3COOAg+H++Cl-=CH3COOH+AgCl |
| D.向AgCl悬浊液中加入Ag2S固体,AgCl的溶解度增大 |
您最近一年使用:0次
2021高三·全国·专题练习
名校
10 . 某兴趣小组进行下列实验:
①将0.1 mol·L-1 MgCl2溶液和0.5 mol·L-1 NaOH溶液等体积混合得到浊液
②取少量①中浊液,滴加0.1 mol·L-1 FeCl3溶液,出现红褐色沉淀
③将①中浊液过滤,取少量白色沉淀,滴加0.1 mol·L-1 FeCl3溶液,白色沉淀变为红褐色沉淀
④另取少量白色沉淀,滴加饱和NH4Cl溶液,沉淀溶解
下列说法中不正确的是
①将0.1 mol·L-1 MgCl2溶液和0.5 mol·L-1 NaOH溶液等体积混合得到浊液
②取少量①中浊液,滴加0.1 mol·L-1 FeCl3溶液,出现红褐色沉淀
③将①中浊液过滤,取少量白色沉淀,滴加0.1 mol·L-1 FeCl3溶液,白色沉淀变为红褐色沉淀
④另取少量白色沉淀,滴加饱和NH4Cl溶液,沉淀溶解
下列说法中不正确的是
| A.将①中所得浊液过滤,所得滤液中含少量Mg2+ |
| B.①中浊液中存在沉淀溶解平衡: Mg(OH)2(s)⇌ Mg2+(aq)+2OH-(aq) |
| C.实验②和③均能说明Fe(OH)3比Mg(OH)2难溶 |
D.NH4Cl溶液中的NH 可能是④中沉淀溶解的原因 可能是④中沉淀溶解的原因 |
您最近一年使用:0次
2021-08-10更新
|
982次组卷
|
11卷引用:考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题27 难溶电解质的溶解平衡(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)3.4.1 沉淀溶解平衡原理-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)江苏省扬州中学2021-2022学年上学期高二12月月考化学试题(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第八章 水溶液中的离子反应与平衡 第52练 难溶电解质的溶解平衡河北省石家庄市正中实验中学东校区2022-2023学年高二上学期10月月考化学试题黑龙江省双鸭山市第一中学2022-2023学年高二下学期开学考试化学试题作业(二十一) 沉淀溶解平衡的应用



