1 . 将CaCO3悬浊液静置后,向上层清液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是
A.c(CO ) ) | B.c(Ca2+) | C.c(H+) | D.Ksp(CaCO3) |
您最近一年使用:0次
名校
2 . 某小组研究沉淀之间的转化,实验设计如下:(已知:AgCl为白色固体,AgI为黄色固体)
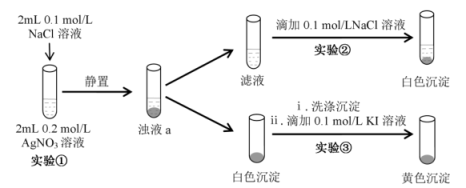
下列分析不正确的是

下列分析不正确的是
| A.浊液a中存在沉淀溶解平衡:AgCl(s)⇌Ag+(aq)+Cl−(aq) |
| B.实验①和②说明Ag+(aq)与Cl−(aq)的反应是有限度的 |
| C.实验③中颜色变化说明AgCl转化为AgI |
| D.实验①和③可以证明AgI比AgCl更难溶 |
您最近一年使用:0次
2021-01-22更新
|
385次组卷
|
6卷引用:北京市丰台区2020-2021学年高二上学期期末考试化学试题
3 . 沈括《梦溪笔谈》记载“石穴中水,所滴者皆为钟乳”,下列条件不利于碳酸钙析出的是
| A.c(Ca2+)减小 | B.水分蒸发 | C.CO2压强减小 | D.温度升高 |
您最近一年使用:0次
名校
解题方法
4 . 某温度时,CaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法中,不正确 的是


A.CaSO4在水中存在沉淀溶解平衡:CaSO4 Ca2+(aq)+SO Ca2+(aq)+SO (aq) (aq) |
| B.a点表示CaSO4在水中达到沉淀溶解平衡 |
| C.b点有CaSO4沉淀生成 |
D.由图可知,含大量SO 的溶液中不存在Ca2+ 的溶液中不存在Ca2+ |
您最近一年使用:0次
2021-01-22更新
|
276次组卷
|
4卷引用:北京市大兴区2020-2021学年高二上学期期末考试化学试题
5 . 废旧磷酸铁锂电池中电极片主要由LiFePO4、铝箔、少量铜及炭黑组成,回收Fe、Li的具体流程如下:
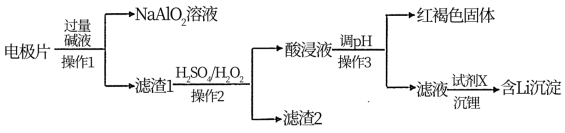
已知:LiFePO4溶于酸,不溶于碱;Li2SO4、Li2CO3在常温下的溶解度分别为34.2 g、1.3 g。
上述流程中各步反应的离子方程式正确的是

已知:LiFePO4溶于酸,不溶于碱;Li2SO4、Li2CO3在常温下的溶解度分别为34.2 g、1.3 g。
上述流程中各步反应的离子方程式正确的是
A.铝箔溶于过量碱液: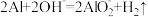 |
B.酸浸液中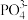 水解: 水解: |
C.滤渣1中加入H2SO4和H2O2可发生反应: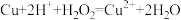 |
D.滤液中加入试剂X时发生的主要反应: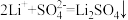 |
您最近一年使用:0次
2021-01-22更新
|
346次组卷
|
5卷引用:江苏省泰州市2021届高三上学期期末调研测试化学试题
名校
解题方法
6 . 氮肥厂的废水中氮元素以NH3•H2O、NH3和NH 的形式存在,对氨氮废水无害化处理已成为全球科学研究热点,下面是两种电化学除氨氮的方法。
的形式存在,对氨氮废水无害化处理已成为全球科学研究热点,下面是两种电化学除氨氮的方法。
方法一:电化学氧化法
(1)有研究表明,当以碳材料为阴极,O2可在阴极生成H2O2,并进一步生成氧化性更强的·OH,·OH可以将水中氨氮氧化为N2。
①写出·OH的电子式_______ 。
②写出·OH去除氨气的化学反应方程式_______ 。
③阴极区加入Fe2+可进一步提高氨氮的去除率,结合下图解释Fe2+的作用_______ 。
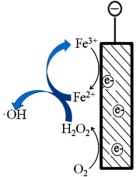
方法二:电化学沉淀法
已知:常温下MgNH4PO4•6H2O、Mg3(PO4)2和Mg(OH)2的溶度积如下
(2)用0.01 mol/L NH4H2PO4溶液模拟氨氮废水,电解沉淀原理如图甲,调节溶液初始pH=7,氨氮的去除率和溶液pH随时间的变化情况如图乙所示。
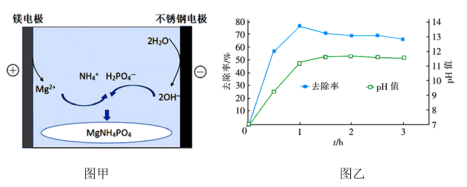
①用化学用语表示磷酸铵镁沉淀的原理:Mg – 2e−=Mg2+,_______ (补全反应)。
②反应1 h以后,氨氮的去除率随时间的延长反而下降的原因_______ 。
 的形式存在,对氨氮废水无害化处理已成为全球科学研究热点,下面是两种电化学除氨氮的方法。
的形式存在,对氨氮废水无害化处理已成为全球科学研究热点,下面是两种电化学除氨氮的方法。方法一:电化学氧化法
(1)有研究表明,当以碳材料为阴极,O2可在阴极生成H2O2,并进一步生成氧化性更强的·OH,·OH可以将水中氨氮氧化为N2。
①写出·OH的电子式
②写出·OH去除氨气的化学反应方程式
③阴极区加入Fe2+可进一步提高氨氮的去除率,结合下图解释Fe2+的作用

方法二:电化学沉淀法
已知:常温下MgNH4PO4•6H2O、Mg3(PO4)2和Mg(OH)2的溶度积如下
| 物质 | MgNH4PO4•6H2O | Mg3(PO4)2 | Mg(OH)2 |
| 溶度积 | 2.5×10−13 | 1.04×10−24 | 1.8×10−11 |
(2)用0.01 mol/L NH4H2PO4溶液模拟氨氮废水,电解沉淀原理如图甲,调节溶液初始pH=7,氨氮的去除率和溶液pH随时间的变化情况如图乙所示。

①用化学用语表示磷酸铵镁沉淀的原理:Mg – 2e−=Mg2+,
②反应1 h以后,氨氮的去除率随时间的延长反而下降的原因
您最近一年使用:0次
2021-01-21更新
|
392次组卷
|
3卷引用:北京市石景山区2021届高三上学期期末考试化学试题
北京市石景山区2021届高三上学期期末考试化学试题(已下线)大题06 化学反应原理综合题(一)-【考前抓大题】备战2021年高考化学(全国通用)北京市清华大学附属中学2022-2023学年高三上学期12月统练六化学试题
7 . 在25℃时,碳酸钙在水中的沉淀溶解平衡曲线如图所示。已知25℃时硫酸钙的Ksp=9.1×10-6,下列说法正确的是
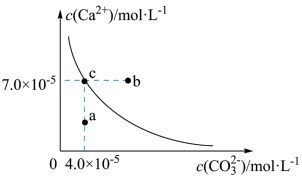

| A.图中b点碳酸钙的结晶速率小于其溶解速率 |
| B.通过蒸发,可使溶液由a点变化到c点 |
| C.除去锅炉水垢中硫酸钙的办法是将其转化为碳酸钙,然后用酸去除 |
| D.在25℃时,从CaCO3(s)转化为CaSO4(s)更容易实现 |
您最近一年使用:0次
解题方法
8 . 已知:pCu=-lgc(Cu+),pX=-1gc(X-)(其中X代表Cl、Br、I)。298K时,Ksp(CuCl)=10-6,Ksp(CuBr)=10-9,Ksp(CuI)=10-12。在CuCl、CuBr、CuI的饱和溶液中阳离子和阴离子浓度关系如图所示。下列说法正确的是


| A.298K时,在CuCl的饱和溶液中加入少量NaCl固体,c(Cu+)和c(Cl-)都减小 |
| B.图中x代表CuI曲线,且P点c(Cu+)=c(I-) |
| C.升高溶液温度,M点可能移动到N点 |
D.298K时,CuBr(s)+I-(aq) CuI(s)+Br-(aq)的平衡常数K=103 CuI(s)+Br-(aq)的平衡常数K=103 |
您最近一年使用:0次
2021-01-20更新
|
185次组卷
|
2卷引用:辽宁省锦州市2020-2021学年高二上学期期末考试化学试题
名校
解题方法
9 . 下列关于沉淀溶解平衡的判断正确的是
| A.某离子被沉淀完全是指该离子在溶液中的浓度为0 |
B.向饱和 水溶液中加入 水溶液中加入 固体, 固体,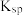 值变大 值变大 |
C.向 悬浊液中滴加 悬浊液中滴加 溶液,生成红褐色沉淀 溶液,生成红褐色沉淀 |
D.含有 和 和 固体的悬浊液: 固体的悬浊液: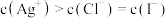 |
您最近一年使用:0次
2014·陕西·二模
名校
10 . 已知25℃时,AgCl的Ksp=1.56×10-10,AgBr的Ksp=5.0×10-13,将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓硝酸银溶液,发生的反应为
| A.只有AgBr沉淀生成 | B.AgCl和AgBr沉淀等量生成 |
| C.AgCl沉淀少于AgBr沉淀 | D.AgCl沉淀多于AgBr沉淀 |
您最近一年使用:0次
2021-01-19更新
|
196次组卷
|
18卷引用:河南省新蔡县2020-2021学年高二上学期期末调研考试化学试题
河南省新蔡县2020-2021学年高二上学期期末调研考试化学试题辽宁省本溪市第一中学2018-2019学年高二上学期期末考试化学试题山西省运城市芮城县2018-2019学年高二上学期期末考试化学试题北京市昌平区新学道临川学校2019-2020学年高二上学期期末考试化学试题四川省成都外国语学校2020-2021学年高二下学期开学考试化学试题内蒙古呼和浩特市2021-2022学年高二上学期期末考试化学试题陕西省渭南市白水县2021-2022学年高二上学期期末考试化学试题(已下线)2014陕西省西工大附中高三上学期第二次适应性训练化学试卷(已下线)2015届湖北省恩施高中高三上学期起点考试化学试卷2015届湖南省长浏宁三县一中高三5月模拟考试化学试卷2015届湖南省长沙、浏阳、宁乡三市高三下学期模拟考试化学试卷2015-2016学年湖南省常德一中高二下第一次月考化学试卷河南省洛阳市2018-2019学年高二第一学期期中考试化学试题吉林省长春市实验中学2019-2020学年高二上学期期中考试化学试题(已下线)【南昌新东方】莲塘一中2020届高二11月质量检测(已下线)【南昌新东方】2019 南大附中 高二上 期中江西省临川一中暨临川一中实验学校2020-2021学年高二上学期期中考试化学试题安徽省池州市第一中学2020-2021学年高二12月月考化学试题



