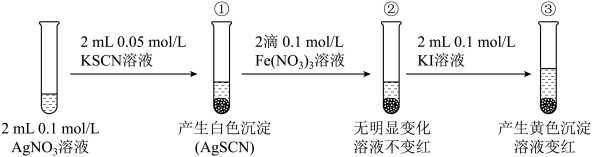
1 . 下列有关说法中,正确的是
| A.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 |
| B.在Ca(OH)2(Ksp=5.5×10-6)、Mg(OH)2(Ksp=1.2×10-11)、AgCl(Ksp=1.56×10-10)三种物质中,AgCl的溶解度最小 |
C.已知BaSO4的Ksp=c(Ba2+)·c(SO ),所以在BaSO4溶液中有c(Ba2+)= c(SO ),所以在BaSO4溶液中有c(Ba2+)= c(SO )= )= |
| D.Ksp小的难溶物可以转变为Ksp更小的难溶物,不可以转变为Ksp更大的难溶物 |
您最近一年使用:0次
名校
解题方法
2 . 利用含钴废料(主要成分为 ,还含有少量的铝箔、
,还含有少量的铝箔、 等杂质)制备碳酸钴的工艺流程如图:
等杂质)制备碳酸钴的工艺流程如图: 的反应原理:
的反应原理: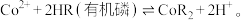 下列说法错误的是
下列说法错误的是
 ,还含有少量的铝箔、
,还含有少量的铝箔、 等杂质)制备碳酸钴的工艺流程如图:
等杂质)制备碳酸钴的工艺流程如图: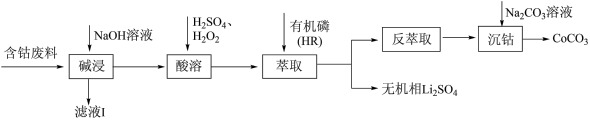
 的反应原理:
的反应原理: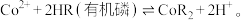 下列说法错误的是
下列说法错误的是A.“滤液Ⅰ”中溶质的主要成分是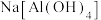 |
B.“反萃取”中可加入 分离出 分离出 |
C.“酸溶”反应中 可以换成 可以换成 |
D.为提高产品的纯度,“沉钴”时 溶液滴加速率不宜过快 溶液滴加速率不宜过快 |
您最近一年使用:0次
2024-01-08更新
|
438次组卷
|
3卷引用:江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷
江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷 福建省泉州市第七中学2023-2024学年高三上学期期中考试化学试题 (已下线)通关练02 重要无机化合物的性质及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
3 . 为研究沉淀的生成及转化,进行如下实验。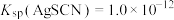
下列关于该实验的分析不正确 的是
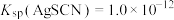
下列关于该实验的分析
A.①中产生白色沉淀的原因是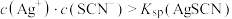 |
B.充分反应后①中 浓度为 浓度为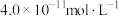 |
C.③中产生黄色沉淀可证明 向 向 沉淀转化 沉淀转化 |
D.②中加入KI溶液后一定发生了反应 |
您最近一年使用:0次
2024-01-01更新
|
303次组卷
|
8卷引用:江西省宜春市宜丰中学2023-2024学年高三上学期1月月考化学试题
江西省宜春市宜丰中学2023-2024学年高三上学期1月月考化学试题江西省宜春市丰城市东煌学校2023-2024学年高二上学期1月期末化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题四川省成都市第七中学2023-2024学年高一上学期12月月考化学试题北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)辽宁省大连市第十二中学2023-2024学年高二上学期12月学情反馈化学试题(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
名校
解题方法
4 . 室温下,下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将1mL0.1mol/L 溶液滴入5mL 0.1mol/L NaOH溶液有沉淀产生,再滴加0.1mol/L 溶液滴入5mL 0.1mol/L NaOH溶液有沉淀产生,再滴加0.1mol/L 溶液 溶液 | 先有白色沉淀生成,后变为浅蓝色沉淀 | 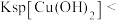 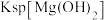 |
| B | 向浓度均为0.1mol/L的 和 和 混合溶液中滴加0.1mol/L 混合溶液中滴加0.1mol/L 溶液 溶液 | 先出现黄色沉淀 |  还原性强于 还原性强于 |
| C | 室温时,在pH试纸上滴2~3滴 溶液 溶液 | 测得, |  溶液中 溶液中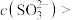  |
| D | 用pH计测量相同浓度NaClO溶液和 溶液的pH值 溶液的pH值 | NaClO溶液的pH值大于 溶液 溶液 |  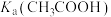 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-29更新
|
441次组卷
|
2卷引用:江西省上饶市第一中学2023-2024学年高二下学期开学考试化学试题
名校
5 . 下列实验装置(部分夹持装置已略去)能达到对应实验目的的是


| A.用图甲测定中和热 |
| B.用装置乙作为分馏的接收装置 |
C.图丙比较 和 和 溶解度大小 溶解度大小 |
| D.图丁探究铁的吸氧腐蚀 |
您最近一年使用:0次
名校
6 . 某化学兴趣小组以含钴废渣(主要成分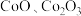 ,还含有
,还含有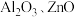 等杂质)为原料制备
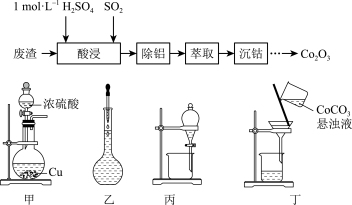
等杂质)为原料制备 的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
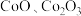 ,还含有
,还含有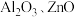 等杂质)为原料制备
等杂质)为原料制备 的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
的一种实验流程如下。下列与流程相关的原理、装置和操作能达到实验目的的是
A.将 固体放入蒸发血中灼烧制 固体放入蒸发血中灼烧制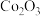 |
B.“酸浸”所需的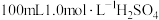 溶液用装置乙配制 溶液用装置乙配制 |
C.“萃取”的目的是除去 ,用装置丙,振荡时分液漏斗下口应倾斜向上 ,用装置丙,振荡时分液漏斗下口应倾斜向上 |
D.用装置甲制备“酸浸”所需的 ,“酸浸”时 ,“酸浸”时 为还原剂 为还原剂 |
您最近一年使用:0次
2023-12-18更新
|
303次组卷
|
3卷引用:江西省宜春市宜丰中学2023-2024学年高一上学期1月期末化学试题
名校
7 . 下列实验操作、现象、解释或结论都正确的是
| 选项 | 操作 | 现象 | 解释或结论 |
| A | 在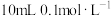 的 的 溶液中依次滴入几滴 溶液中依次滴入几滴 溶液和KI溶液 溶液和KI溶液 | 溶液先产生白色沉淀,后又产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 将 通入 通入 溶液 溶液 | 有白色沉淀生成 | 生成了 沉淀 沉淀 |
| C | 向某钠盐粉末上滴加浓盐酸,将产生的气体通入品红溶液 | 品红溶液褪色 | 该钠盐为 、 、 或 或 |
| D | 在 溶液中通入 溶液中通入 气体 气体 | 有沉淀生成 | 沉淀为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-16更新
|
360次组卷
|
3卷引用:江西省上饶市清源学校2023-2024学年高二上学期12月考试化学试题
名校
解题方法
8 . MnO2是重要化工原料,由软锰矿制备MnO2的一种工艺流程如下:

资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH:
③该工艺条件下,MnO2与H2SO4不反应。
(1)溶出
①溶出前,软锰矿需研磨,目的是___________ 。
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:
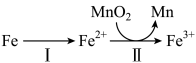
i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是___________ 。
ii.若I中Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2,而实际比值(0.9)小于2,原因是___________ 。
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2后加入NH3·H2O,调溶液pH,说明试剂加入顺序及调节pH的原因:___________ 。
(3)电解
Mn2+纯化液经电解得MnO2,生成1molMnO2电子转移的数目为___________ 。
(4)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,如热至充分反应,生成CO2,再滴加cmol/L KMnO4溶液至剩余Na2C2O4恰好完全反应,消耗KMnO4溶液的体积为dL,产品纯度为___________ (用质量分数表示)。[已知:MnO2及 均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]

资料:
①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2。
②金属离子沉淀的pH:
| Fe3+ | A13+ | Mn2+ | Fe2+ | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
(1)溶出
①溶出前,软锰矿需研磨,目的是
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:

i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是
ii.若I中Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2,而实际比值(0.9)小于2,原因是
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2后加入NH3·H2O,调溶液pH,说明试剂加入顺序及调节pH的原因:
(3)电解
Mn2+纯化液经电解得MnO2,生成1molMnO2电子转移的数目为
(4)产品纯度测定
向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,如热至充分反应,生成CO2,再滴加cmol/L KMnO4溶液至剩余Na2C2O4恰好完全反应,消耗KMnO4溶液的体积为dL,产品纯度为
 均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
均被还原为Mn2+,M(MnO2)=86.94g/mol、M(Na2C2O4)=134.0g/mo]
您最近一年使用:0次
2023-12-15更新
|
183次组卷
|
3卷引用:江西省上饶市广丰一中2023-2024学年高二上学期12月考试化学试卷
9 . 常温下,向10.0mL浓度均为0.1mol/L的 和
和 混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3.
混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3.

已知:①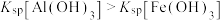 ;
;
②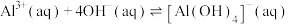 ,298K,
,298K, 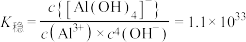 。
。
下列叙述正确的是
 和
和 混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3.
混合溶液中加入NaOH固体,溶液中金属元素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b两点溶液的pH分别为3.0,4.3.
已知:①
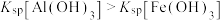 ;
;②
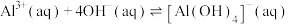 ,298K,
,298K, 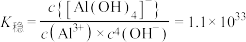 。
。下列叙述正确的是
A.曲线Ⅱ代表 |
B.常温下,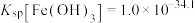 |
C.c点铁铝元素主要存在形式为 和 和 |
D.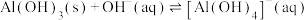 的平衡常数K为 的平衡常数K为 数量级 数量级 |
您最近一年使用:0次
名校
10 . 已知CuS是一种不溶于非氧化性酸的沉淀。下列说法正确并能用勒 夏特列原理解释的是
夏特列原理解释的是
 夏特列原理解释的是
夏特列原理解释的是| A.工业合成SO3采用高压条件以增大平衡转化率 |
B.向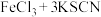  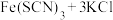 的平衡体系中加入少量KCl固体,溶液颜色变浅 的平衡体系中加入少量KCl固体,溶液颜色变浅 |
C.向氯水中加碳酸钠,可提高溶液中 的浓度 的浓度 |
| D.向饱和H2S溶液中加入少量硫酸铜溶液,溶液酸性增强 |
您最近一年使用:0次



