1 . 某溶液中含有 ,
, ,
, ,现用NaOH溶液、盐酸和
,现用NaOH溶液、盐酸和 溶液将这三种离子逐一沉淀分离,其流程如图所示。下列说法正确的是
溶液将这三种离子逐一沉淀分离,其流程如图所示。下列说法正确的是

 ,
, ,
, ,现用NaOH溶液、盐酸和
,现用NaOH溶液、盐酸和 溶液将这三种离子逐一沉淀分离,其流程如图所示。下列说法正确的是
溶液将这三种离子逐一沉淀分离,其流程如图所示。下列说法正确的是
A.试剂A为 溶液 溶液 |
B.沉淀3的化学式可能是 |
C.生成沉淀1的离子方程式为: |
D.向氯化银悬浊液中加入少量水。氯化银溶解平衡正向移动, 和 和 浓度均减小 浓度均减小 |
您最近一年使用:0次
2022-12-04更新
|
158次组卷
|
3卷引用:山东省枣庄滕州市2022-2023学年高三上学期期中考试化学试题
山东省枣庄滕州市2022-2023学年高三上学期期中考试化学试题山东省滕州市第二中学2022-2023学年高三上学期11月定时检测化学试题(已下线)广东省东莞市2022-2023学年高三上学期期末教学质量检查变式汇编(11-16)
解题方法
2 . 完成下列方程式的书写
(1)工业上以黄铜矿(主要含CuFeS2,还含FeS等)为原料可以制备Cu,流程如下:

①写出“浸取”时CuFeS2和FeCl3溶液反应的离子方程式:_________ 。
②写出第二次“溶解”时反应的化学方程式为_________ 。
③用(NH4)2SO3还原CuCl2溶液也能获得CuCl,pH约为4时,CuCl的产率最大。写出该条件下反应的离子方程式:_________ 。
(2)我国科研人员研究出在Cu-ZnO-ZrO2催化剂上CO2氢化合成甲醇的反应历程如图所示。

反应③的化学方程式为_________ 。
(1)工业上以黄铜矿(主要含CuFeS2,还含FeS等)为原料可以制备Cu,流程如下:

①写出“浸取”时CuFeS2和FeCl3溶液反应的离子方程式:
②写出第二次“溶解”时反应的化学方程式为
③用(NH4)2SO3还原CuCl2溶液也能获得CuCl,pH约为4时,CuCl的产率最大。写出该条件下反应的离子方程式:
(2)我国科研人员研究出在Cu-ZnO-ZrO2催化剂上CO2氢化合成甲醇的反应历程如图所示。

反应③的化学方程式为
您最近一年使用:0次
3 . 工业上以黑钨矿为原料利用纯碱烧结水浸法冶炼金属钨的流程如图(已知:黑钨矿的主要成分为 、
、 ,同时还含有少量
,同时还含有少量 )。则下列说法正确的是
)。则下列说法正确的是

已知:①
②
 、
、 ,同时还含有少量
,同时还含有少量 )。则下列说法正确的是
)。则下列说法正确的是
已知:①

②

| A.以上步骤中都涉及氧化还原反应 |
| B.由题目信息可知,同浓度的硅酸根离子比钨酸根离子结合质子能力强 |
C.滤渣2成分为 |
D.必须用电解法将 还原成单质 还原成单质 |
您最近一年使用:0次
名校
解题方法
4 . 某工厂生产硼砂产生的固体废料中,主要含有MgCO3、CaCO3、SiO2、Al2O3和Fe2O3等,其中MgCO3质量分数为63%。用该固体废料回收镁的工艺流程如下:

(1)操作I的名称是_________ ,所需要的玻璃仪器为_________ 。
(2)“酸浸”时,试剂A的化学式是_________ ,为加快酸浸速率,可采取的措施是_________ 。(写一条即可)。
(3)滤液a中的金属阳离子是_________ 。对滤液a调pH时合理的pH范围是_________ 。
(4)“沉镁”时发生反应的化学方程式是_________ 。
(5)若滤液b中c(SO )=2.1mol/L,c(Mg2+)=1.0 mol/L,已知氢离子、氢氧根离子浓度忽略不计,则c(NH
)=2.1mol/L,c(Mg2+)=1.0 mol/L,已知氢离子、氢氧根离子浓度忽略不计,则c(NH )为
)为_________ mol/L。
(6)若流程中镁的总损耗为10%,则100t的固体废料可回收镁的质量是_________ 。

| 金属离子 | Al3+ | Fe3+ | Mg2+ |
| 开始沉淀时(c=1 mol/L)的pH | 1.7 | 1.2 | 8.8 |
| 完全沉淀时(c=1.0×10-5 mol/L)的pH | 4.7 | 2.9 | 11.3 |
(2)“酸浸”时,试剂A的化学式是
(3)滤液a中的金属阳离子是
(4)“沉镁”时发生反应的化学方程式是
(5)若滤液b中c(SO
 )=2.1mol/L,c(Mg2+)=1.0 mol/L,已知氢离子、氢氧根离子浓度忽略不计,则c(NH
)=2.1mol/L,c(Mg2+)=1.0 mol/L,已知氢离子、氢氧根离子浓度忽略不计,则c(NH )为
)为(6)若流程中镁的总损耗为10%,则100t的固体废料可回收镁的质量是
您最近一年使用:0次
名校
解题方法
5 . 劳动成就梦想。下列劳动项目与化学知识相符的是
| 选项 | 劳动项目 | 化学知识 |
| A | 废水处理:加入 处理含重金属离子 处理含重金属离子 的废水 的废水 |  具有还原性,将 具有还原性,将 转化为 转化为 单质沉淀 单质沉淀 |
| B | 家务劳动:用洁厕灵(主要含浓盐酸)清洗马桶 | 含氯化合物具有杀菌消毒功能 |
| C | 职业劳动:葡萄酒中加入适量 |  可防止氧化,起到保质作用 可防止氧化,起到保质作用 |
| D | 工厂参观:燃煤时,加入生石灰 | 生石灰可以和 反应,从而降低温室效应 反应,从而降低温室效应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 化学之美不仅美在其外,更深藏于内。下列化学之美与所涉及的化学知识不相符的是
| 选项 | 化学之美 | 化学知识 |
| A | 天然的水晶、玛瑙饰品光彩夺目 | 水晶、玛瑙主要成分为硅酸盐 |
| B | 干冰可用在舞台上制造“云雾” | 干冰升华,吸收大量的热 |
| C | 清晨的阳光射入密林形成光柱 | 水雾属于气溶胶,能产生丁达尔现象 |
| D | 桂林的地下溶洞千姿百态 | 溶洞的形成涉及CaCO3的沉淀溶解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-26更新
|
248次组卷
|
2卷引用:广东省广州市2022-2023学年高三上学期11月调研测试化学试题
7 . 常温下,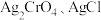 的
的 值分别为
值分别为 ,下列说法正确的是
,下列说法正确的是
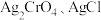 的
的 值分别为
值分别为 ,下列说法正确的是
,下列说法正确的是A.反应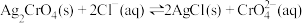 的平衡常数 的平衡常数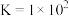 |
B.在食盐水中, 的溶解度及 的溶解度及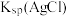 均比在蒸馏水中小 均比在蒸馏水中小 |
C.常温下, 饱和溶液中 饱和溶液中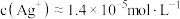 |
D.向饱和 中加入 中加入 溶液有沉淀生成, 溶液有沉淀生成, 减小 减小 |
您最近一年使用:0次
名校
8 . 下列反应的发生与“盐类水解平衡”或“难溶电解质的溶解平衡”无关 的是
| A.镁条与NH4Cl溶液反应生成H2 |
| B.NaHSO4溶液与NaOH溶液反应生成Na2SO4 |
| C.盐酸与CaCO3反应生成CO2 |
| D.Fe2(SO4)3溶液和Na2CO3溶液反应生成CO2 |
您最近一年使用:0次
2022-11-20更新
|
400次组卷
|
5卷引用:北京市首都师范大学附属中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
9 . 铜镍电镀废水处理后得到电镀污泥,利用以下T艺可制备硫酸镍晶体( ):
):

已知:①电镀污泥含有 、
、 、
、 、
、 和
和 等。
等。
②该工艺条件下,几种金属离子开始沉淀和完全沉淀的pH如表所示:
|
|
|
| |
开始沉淀的pH | 6.3 | 2.2 | 4.3 | 7.2 |
完全沉淀的pH | 9.6 | 3.2 | 5.6 | 8.4 |
③ 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。
请回答下列问题:
(1)“酸浸”步骤中,为了提高浸出速率,可采取的措施有
(2)滤渣2的主要成分为
(3)若上述流程省去“氧化”步骤,造成的后果是
(4)写出“沉镍”步骤中得到碱式碳酸镍[
 ]的离子方程式:
]的离子方程式:(5)一系列操作的实验步骤如下,请补充相关实验内容:
ⅰ.
ⅱ.将沉淀转移至烧杯中,滴加稀硫酸直至沉淀恰好完全溶解;
ⅲ.蒸发浓缩、冷却结晶,过滤得 晶体;
晶体;
ⅳ.用少量 晶体并晾干。
晶体并晾干。
(6)在空气中煅烧26.3g
 ,剩余固体的质量随时间变化的曲线如图所示,该曲线中D点所表示的氧化物中Ni、O的原子个数比为
,剩余固体的质量随时间变化的曲线如图所示,该曲线中D点所表示的氧化物中Ni、O的原子个数比为
您最近一年使用:0次
2022-11-15更新
|
254次组卷
|
5卷引用:河南省安阳市2022-2023学年高三上学期期中考试化学试题
解题方法
10 . 下列实验对应的离子方程式正确的是
A.向饱和食盐水中加浓盐酸析出固体:Na++Cl− NaCl↓ NaCl↓ |
| B.在铜片表面滴几滴稀硝酸产生无色气体:Cu+2H+=Cu2++H2↑ |
C.向Na2CO3溶液中滴加少量氯水:CO +2Cl2+H2O=CO2↑+2Cl−+2HClO +2Cl2+H2O=CO2↑+2Cl−+2HClO |
| D.向血红色Fe(SCN)3溶液中加入过量铁粉至溶液褪色:2Fe3++Fe=3Fe2+ |
您最近一年使用:0次



