名校
1 . 某同学进行如下实验:
已知:i.H2O2 H++HO
H++HO HO
HO
 H++O
H++O
ii.BaO2是一种白色难溶于水的固体
下列说法不合理的是
| 序号 | 实验① | 实验② | 实验③ | 实验④ | 实验⑤ |
| 方案 | 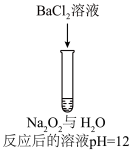 | 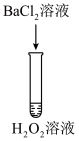 | 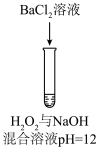 | 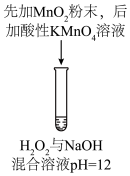 | 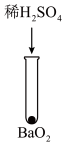 |
| 现象 | 出现白色沉淀 | 无明显现象 | 出现白色沉淀 | 产生大量气泡,高锰酸钾溶液不褪色 | 出现白色沉淀 |
 H++HO
H++HO HO
HO
 H++O
H++O
ii.BaO2是一种白色难溶于水的固体
下列说法不合理的是
| A.实验①和③生成白色沉淀的反应属于复分解反应 |
| B.实验③可证明H2O2溶液中存在电离平衡 |
| C.实验⑤的白色沉淀经检验为BaSO4,但不能证明溶解度BaO2>BaSO4 |
| D.可用BaCl2、MnO2、H2O检验长期放置的Na2O2中是否含有Na2CO3 |
您最近一年使用:0次
名校
解题方法
2 . 某同学进行如下实验:
已知:ⅰ. 、HO
、HO
 H++O2—
H++O2—
ⅱ.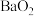 是一种白色难溶于水的固体
是一种白色难溶于水的固体
下列说法合理的是
| 序号 | 实验① | 实验② | 实验③ | 实验④ | 实验⑤ |
| 方案 |  溶液 溶液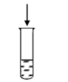  与 与 反应后的溶液 反应后的溶液 |  溶液 溶液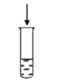  溶液 溶液 |  溶液 溶液  与NaOH混合溶液 与NaOH混合溶液 | 先加 粉末,后加酸性 粉末,后加酸性 溶液 溶液  与NaOH混合溶液 与NaOH混合溶液 | 稀  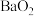 |
| 现象 | 出现白色沉淀 | 无明显现象 | 出现白色沉淀 | 产生大量气泡,高锰酸钾溶液不褪色 | 出现白色沉淀 |
 、HO
、HO
 H++O2—
H++O2—ⅱ.
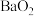 是一种白色难溶于水的固体
是一种白色难溶于水的固体下列说法合理的是
A.实验③可证明 溶液中存在电离平衡 溶液中存在电离平衡 |
| B.实验①和③生成白色沉淀的反应属于氧化还原反应 |
C.实验⑤的白色沉淀经检验为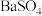 ,说明溶解度BaO2>BaSO4 ,说明溶解度BaO2>BaSO4 |
D.可用 、 、 、 、 检验长期放置的 检验长期放置的 中是否含有 中是否含有 |
您最近一年使用:0次
名校
3 .  与NaOH溶液反应会生成
与NaOH溶液反应会生成 、
、 、
、 等物质。室温下,通过下列实验探究这些含磷化合物的性质。
等物质。室温下,通过下列实验探究这些含磷化合物的性质。
下列有关说法正确的是
 与NaOH溶液反应会生成
与NaOH溶液反应会生成 、
、 、
、 等物质。室温下,通过下列实验探究这些含磷化合物的性质。
等物质。室温下,通过下列实验探究这些含磷化合物的性质。| 实验 | 实验操作和现象 |
| 1 | 蘸取0.1  溶液点在pH试纸上, 溶液点在pH试纸上, ;蘸取0.1 ;蘸取0.1  溶液点在pH试纸上, 溶液点在pH试纸上, |
| 2 | 向0.1  溶液中加入足量0.2 溶液中加入足量0.2  溶液,生成白色沉淀,蘸取上层清液点在pH试纸上, 溶液,生成白色沉淀,蘸取上层清液点在pH试纸上, |
| 3 | 向 中加入足量一定浓度的硫酸,生成 中加入足量一定浓度的硫酸,生成 和 和 |
| 4 | 向含有酚酞的0.1  溶液中滴加0.1 溶液中滴加0.1 NaOH溶液,至溶液由无色变为浅红色 NaOH溶液,至溶液由无色变为浅红色 |
A.0.1  溶液中存在: 溶液中存在: |
B.实验2中发生反应的离子方程式为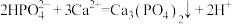 |
C.可用实验3证明 |
D.实验4的过程中可能存在 |
您最近一年使用:0次
名校
4 . 下列关于实验内容和实验目的说法正确的是
| 编号 | 实验内容 | 实验目的 |
| A | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体,溶液红色变浅 固体,溶液红色变浅 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| B | 室温下,用 试纸测定浓度为 试纸测定浓度为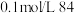 消毒液和 消毒液和 溶液的 溶液的 | 比较 和 和 的酸性强弱 的酸性强弱 |
| C | 用 注射器吸入 注射器吸入 和 和 的混合气体,将细管端用橡胶塞封闭,然后把注射器的活塞往外拉,可观察到混合气体的颜色先变浅后变深 的混合气体,将细管端用橡胶塞封闭,然后把注射器的活塞往外拉,可观察到混合气体的颜色先变浅后变深 | 证明对有气体参加的可逆反应,改变压强一定会使平衡发生移动 |
| D | 向 溶液中滴2滴 溶液中滴2滴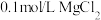 溶液,产生白色沉淀后,再滴加2滴 溶液,产生白色沉淀后,再滴加2滴 溶液,又生成红褐色沉淀 溶液,又生成红褐色沉淀 | 证明在相同温度下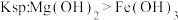 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-04更新
|
219次组卷
|
3卷引用:浙江省北斗联盟2021-2022学年高二下学期期中联考化学试题
名校
5 . 下列关于实验内容和实验目的说法正确的是
| 编号 | 实验内容 | 实验目的 |
| A | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体,溶液红色变浅 固体,溶液红色变浅 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| B | 室温下,用pH试纸测定浓度为0.1mol/LNaClO溶液和0.1mol/L 溶液的pH 溶液的pH | 比较HClO和 的酸性强弱 的酸性强弱 |
| C | 用50mL注射器吸入20mL 和 和 的混合气体,将细管端用橡胶塞封闭,然后把注射器的活塞往外拉,可观察到混合气体的颜色先变深后变浅 的混合气体,将细管端用橡胶塞封闭,然后把注射器的活塞往外拉,可观察到混合气体的颜色先变深后变浅 | 证明对有气体参加的可逆反应,改变压强可能会使平衡发生移动 |
| D | 向10mL0.2mol/LNaOH溶液中滴2滴0.1mol/L 溶液,产生白色沉淀后,再滴加2滴0.1mol/L 溶液,产生白色沉淀后,再滴加2滴0.1mol/L 溶液,又生成红褐色沉淀 溶液,又生成红褐色沉淀 | 证明在相同温度下Ksp: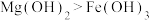 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 向 溶液中通入过量
溶液中通入过量 ,过程和现象如图。
,过程和现象如图。
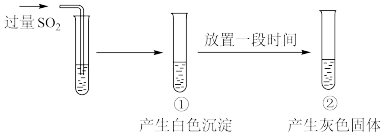
经检验,白色沉淀为 ;灰色固体中含有
;灰色固体中含有 。
。
下列说法错误的是
 溶液中通入过量
溶液中通入过量 ,过程和现象如图。
,过程和现象如图。
经检验,白色沉淀为
 ;灰色固体中含有
;灰色固体中含有 。
。下列说法错误的是
A.①中生成白色沉淀的离子方程式为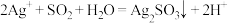 |
B.①中未生成 ,证明溶度积: ,证明溶度积: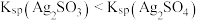 |
C.放置一段时间②中产生灰色固体是因为过量的 将部分 将部分 还原。 还原。 |
D.该实验条件下, 与 与 反应生成 反应生成 的速率大于生成 的速率大于生成 的速率 的速率 |
您最近一年使用:0次
2022-11-19更新
|
172次组卷
|
2卷引用:湖北省荆荆宜三校2022-2023学年高三上学期11月联考化学试题
名校
7 . 室温下,下列说法中不正确的是
| A.已知酸性:CH3COOH>H2CO3>HClO,则pH相同的①CH3COONa ②NaHCO3 ③NaClO三种溶液的c(Na+):③>②>① |
B.0.01mol/L NH4HCO3溶液中离子浓度:c(NH )>c(HCO )>c(HCO )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
| C.向NaHS溶液中加入等物质的量的KOH固体后:c(Na+)=c(H2S)+c(HS-)+2c(S2-) (忽略溶液温度的变化) |
| D.向含白色ZnS的悬浊液中滴入几滴CuSO4溶液,产生黑色沉淀可证明Ksp(ZnS)>Ksp(CuS) |
您最近一年使用:0次
8 . 常温下,将0.025molBaSO4粉末置于盛有蒸馏水的烧杯中形成1L悬浊液,然后向烧杯中加入Na2CO3固体(忽略溶液体积的变化)并充分搅拌。加入Na2CO3固体的过程中溶液中几种离子的浓度变化曲线如图所示,下列说法中错误的是
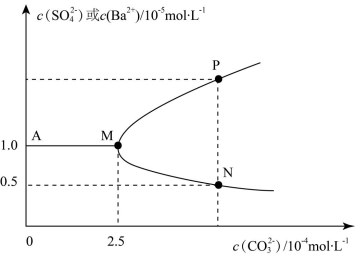

| A.常温下,Ksp(BaCO3)=2.5×10-9 |
| B.P点对应纵坐标的数据为2.5 |
| C.若要使BaSO4全部转化为BaCO3至少要加入0.65molNa2CO3 |
| D.该实验证明,溶解度较小的沉淀在一定条件下,也可能转化为溶解度较大的沉淀 |
您最近一年使用:0次
9 . 某学习小组进行如下实验来证明Ksp(BaCO3)> Ksp(BaSO4)。下 列相关说法错误的是


| A.试管I中产生白色沉淀,试管II中白色沉淀质量增加 |
B.试管II中反应的离子方程式为: BaCO3(s) +SO (aq) (aq)  BaSO4(s) + CO BaSO4(s) + CO (ag) (ag) |
| C.取试管I中上层清液,加入3 mol·L-1 BaCl2溶液会产生浑浊现象 |
| D.在实验结束后的试管II中加入足量稀盐酸,无明显现象 |
您最近一年使用:0次
名校
10 . 已知: (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
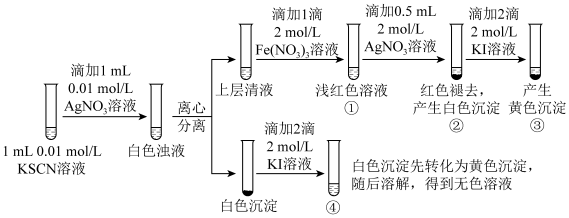
下列说法中,不正确 的是
 (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
下列说法中,
A.①中现象能说明 与 与 生成的白色浊液中存在沉淀溶解平衡 生成的白色浊液中存在沉淀溶解平衡 |
B.②中现象产生的原因是发生了反应: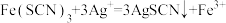 |
| C.③中产生黄色沉淀的现象能证明AgI的溶解度比AgSCN的溶解度小 |
D.④中黄色沉淀溶解的原因可能是AgI与KI溶液中的 进一步发生了反应 进一步发生了反应 |
您最近一年使用:0次
2021-11-15更新
|
697次组卷
|
3卷引用:北京市北师大附属实验中学2021-2022学年高二上学期期中考试化学试题
北京市北师大附属实验中学2021-2022学年高二上学期期中考试化学试题(已下线)第21讲 难溶电解质的沉淀溶解平衡(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)辽宁省大连市第八中学2021-2022学年高三上学期12月月考化学试题



