1 . 25℃时,向2.5L蒸馏水中加入0.05molBaSO4固体粉末,再逐渐加入一定量的Na2CO3固体粉末,边加边搅拌(忽略溶液体积变化)。溶液中部分离子的浓度变化如图所示。下列说法正确的是
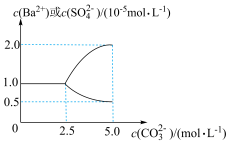

| A.25℃时,Ksp(BaCO3)<Ksp(BaSO4) |
| B.BaSO4在水中的Ksp大于其在BaCl2溶液中的Ksp |
| C.加入1.3molNa2CO3,即可使BaSO4全部转化为BaCO3 |
D.当BaSO4恰好全部转化为BaCO3时,c( )>c(Ba2+)>c( )>c(Ba2+)>c( )>c(OH-) )>c(OH-) |
您最近一年使用:0次
2023-12-16更新
|
346次组卷
|
4卷引用:山东省淄博市2021届高三三模考试化学试题
2 . 下列关于沉淀的叙述不正确的是
| A.生产、科研中常利用生成沉淀来达到分离或除杂的目的 |
| B.沉淀的溶解只能通过酸碱中和反应来实现 |
| C.沉淀转化的实质就是沉淀溶解平衡的移动 |
| D.一般来说,溶解度小的沉淀转化成溶解度更小的沉淀容易实现 |
您最近一年使用:0次
2022-12-20更新
|
67次组卷
|
3卷引用:山东省威海市文登新一中2021-2022学年高二上学期期中考试化学试题
3 . 运用化学反应原理,研究硫、磷化合物的反应具有重要意义。
(1)已知H3PO2(次磷酸)的水溶液中存在 H3PO2分子。H3PO2与足量 NaOH溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为___________ ,该盐属于___________ (填"正盐"或"酸式盐")。H3PO2易被氧化为 H3PO4,已知常温下H3PO4的电离常数为 ,请利用以上数据计算推测 Na2HPO4溶液的酸碱性
,请利用以上数据计算推测 Na2HPO4溶液的酸碱性___________ 。(填“酸性”、“碱性”或“中性”)
(2)常温下,用NaOH溶液吸收 SO2得到 pH=9的Na2SO3溶液,吸收过程中水的电离衡___________ (填"向左"、"向右"或"不")移动。试计算该溶液中
___________ 。(常温下 H2SO3的电离平衡常数 )
)
(3)NaHSO3溶液的pH<7,NaHCO3溶液的pH>7,则NaHSO3溶液中c(H2SO3)___________ (填“>”“<”或“=”,下同)c( ),NaHCO3溶液中c(H2CO3)
),NaHCO3溶液中c(H2CO3)___________ c( )。
)。
(4)化工生产中常用 FeS作沉淀剂除去工业废水中的Cu2+,其反应原理为Cu2+(aq)+FeS(s)⇌CuS(s)+Fe2+(aq)。下列有关叙述正确的是___________ 。
a.
b.达到平衡时c(Fe2+)=c(Cu2+)
c.溶液中加入少量 Na2S固体后,溶液中c(Fe2+)、c(Cu2+)都减小
d. 该反应平衡常数
(1)已知H3PO2(次磷酸)的水溶液中存在 H3PO2分子。H3PO2与足量 NaOH溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为
 ,请利用以上数据计算推测 Na2HPO4溶液的酸碱性
,请利用以上数据计算推测 Na2HPO4溶液的酸碱性(2)常温下,用NaOH溶液吸收 SO2得到 pH=9的Na2SO3溶液,吸收过程中水的电离衡

 )
)(3)NaHSO3溶液的pH<7,NaHCO3溶液的pH>7,则NaHSO3溶液中c(H2SO3)
 ),NaHCO3溶液中c(H2CO3)
),NaHCO3溶液中c(H2CO3) )。
)。(4)化工生产中常用 FeS作沉淀剂除去工业废水中的Cu2+,其反应原理为Cu2+(aq)+FeS(s)⇌CuS(s)+Fe2+(aq)。下列有关叙述正确的是
a.

b.达到平衡时c(Fe2+)=c(Cu2+)
c.溶液中加入少量 Na2S固体后,溶液中c(Fe2+)、c(Cu2+)都减小
d. 该反应平衡常数

您最近一年使用:0次
2022-09-22更新
|
97次组卷
|
2卷引用:山东省临沂市第二中学2021-2022学年高二上学期12月月考化学试题
名校
解题方法
4 . 下列说法中正确的是
A.用标准盐酸滴定未知浓度的 溶液,滴定前酸式滴定管尖嘴有气泡未排出,滴定后气泡消失,会造成测定结果偏低 溶液,滴定前酸式滴定管尖嘴有气泡未排出,滴定后气泡消失,会造成测定结果偏低 |
B.等体积的 的酸 的酸 和 和 的溶液分别与足量的铁粉反应, 的溶液分别与足量的铁粉反应, 放出的 放出的 多,则 多,则 酸性弱 酸性弱 |
C.由水电离出的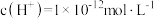 的溶液中一定能大量存在如下离子: 的溶液中一定能大量存在如下离子: 、 、 、 、 、 、 |
D.工业废水中的 、 、 等重金属阳离子不可以通过加入 等重金属阳离子不可以通过加入 除去 除去 |
您最近一年使用:0次
2022-09-11更新
|
130次组卷
|
3卷引用:山东省济宁市兖州区2021-2022学年高二上学期期中考试化学试题
名校
5 . 下列用于解释事实的方程式书写不正确 的是
A.将纯水加热至较高温度,水的pH变小:H2O H+ + OH− ΔH>0 H+ + OH− ΔH>0 |
B.NH4Cl溶液可以用作除铁锈的工作原理:NH + H2O + H2O  NH3·H2O + H+ NH3·H2O + H+ |
C.向氢氧化镁悬浊液中滴入酚酞溶液,溶液变红: Mg(OH)2(s)  Mg2+(aq) + 2OH−(aq) Mg2+(aq) + 2OH−(aq) |
D.用饱和Na2CO3溶液处理锅炉水垢中的CaSO4:Ca2+ + CO = CaCO3 = CaCO3 |
您最近一年使用:0次
10-11高二下·浙江杭州·期中
名校
解题方法
6 . 下列化学原理的应用,可以用沉淀溶解平衡原理来解释的是
①热纯碱溶液洗涤油污的能力比冷纯碱溶液强
②误将钡盐[ 、
、 ]当作食盐食用后,常用0.5%的
]当作食盐食用后,常用0.5%的 溶液解毒
溶液解毒
③石灰岩(喀斯特地貌)溶洞的形成
④ 不能作“钡餐”,而
不能作“钡餐”,而 可以
可以
⑤泡沫灭火器灭火原理
①热纯碱溶液洗涤油污的能力比冷纯碱溶液强
②误将钡盐[
 、
、 ]当作食盐食用后,常用0.5%的
]当作食盐食用后,常用0.5%的 溶液解毒
溶液解毒 ③石灰岩(喀斯特地貌)溶洞的形成
④
 不能作“钡餐”,而
不能作“钡餐”,而 可以
可以 ⑤泡沫灭火器灭火原理
| A.②③④ | B.①②③ | C.③④⑤ | D.①②③④⑤ |
您最近一年使用:0次
2022-04-06更新
|
1235次组卷
|
55卷引用:山东省淄博市桓台第二中学2021-2022学年高一9月月考化学试题
山东省淄博市桓台第二中学2021-2022学年高一9月月考化学试题(已下线)小题22 难溶电解质的溶解平衡——备战2021年高考化学经典小题考前必刷(全国通用)云南省永胜县第一中学2020-2021学年高二下学期6月份考试化学试题(已下线)第26讲 难溶电解质的溶解平衡(精讲)-2022年一轮复习讲练测选择性必修1(SJ)专题3第四单元 沉淀溶解平衡课时1 沉淀溶解平衡及其应用(已下线)专题3.4.2 沉淀溶解平衡的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)北京市首都师范大学附属中学2021-2022学年高二上学期期中考试化学试题(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡原理的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)江西省遂川中学2021-2022学年高二上学期第二次月考化学(A卷)试题陕西省黄陵中学2021-2022学年高二上学期期中考试化学试题(已下线)2010—2011学年浙江省杭州师范大学附属中学高二下学期期中考试化学试卷(已下线)2011-2012年山西省平遥中学高二上学期期中考试化学(理)试卷河北省衡水中学2016-2017学年高一下学期三调考试化学试题吉林省延边第二中学2017-2018学年高二上学期第二次月考化学试题2017-2018学年四川省乐山四校高二第二学期半期联考化学试题【全国百强校】河北省辛集中学2018-2019学年高二上学期期中考试化学试题(已下线)2019年1月7日 《每日一题》人教选修4-沉淀的生成与溶解【全国百强校】河北省冀州市中学2018-2019学年高二上学期第五次月考化学试题2019年10月20日《每日一题》2020年高考化学一轮复习—— 每周一测黑龙江省哈尔滨市第六中学2019-2020学年高二上学期期中考试化学试题北京市2019—2020学年高二上学期期中考试化学试题(选修4人教版)苏教版选修四化学反应原理专题3第四单元 难溶电解质的沉淀溶解平衡 同步检测试卷山西省太原市太原师范学院附属中学2019-2020学年高二上学期12月月考理科化学试题高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 课时1 溶解平衡及其应用(已下线)第3章 章末检测-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)河北省石家庄市辛集市第一中学2019-2020学年高二第二次考试(二)化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡湖南省常德市淮阳中学2019-2020学年高二下学期期中考试化学试题(已下线)3.4 难溶电解质的溶解平衡(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)3.4.2 沉淀溶解平衡原理的应用(重点练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)湖北省武汉市钢城四中2020-2021学年高二上学期期中考试化学试题陕西省宝鸡市宝鸡中学2020-2021学年高二上学期阶段考试(一)化学试题山西省怀仁市第一中学云东校区2020-2021学年高二上学期第三次月考化学试题黑龙江省哈尔滨市第一六二中学2021-2022学年高二上学期期末考试化学试题(已下线)第10练 沉淀溶解平衡-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)黑龙江省大庆中学2021-2022学年高二下学期开学考试化学试题江苏省天一中学2021-2022学年高二上学期期末考试化学试题黑龙江省双鸭山市第一中学2021-2022学年高二下学期开学考试化学试题(已下线)第26讲 难溶电解质的溶解平衡(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第24讲 沉淀溶解平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第三章 水溶液中的离子反应与平衡(B卷·能力提升练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)山西省太原师范学院附属中学2022-2023学年高二上学期12月月考化学试题新疆阿克苏市实验中学2022-2023学年高二上学期期末考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第52练 难溶电解质的溶解平衡3.4.1沉淀溶解平衡原理 课后(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)作业(二十一) 沉淀溶解平衡的应用
名校
解题方法
7 . 下列实验操作、现象、结论正确的是
| 操作及现象 | 结论 | |
| A | 向Al2(SO4)3溶液中滴加Na2S溶液,产生白色沉淀 | 白色沉淀成分是Al2S3 |
| B | 将粗铜和精铜分别连接电源的正、负极,两电极减少和增加的质量不相等 | 质量变化大的电极一定与电源的负极相连 |
| C | 向盛有2mL 0.1mol/LZnSO4溶液的试管中加入2mL 1mol/LNa2S溶液,再加入0.1mol/LCuSO4溶液,最终得到黑色沉淀 | CuS的溶解度比ZnS小 |
| D | 向盛有0.01mol/L CH3COONa溶液的试管中滴加几滴酚酞试液,溶液变红,加热,颜色变深 | 溶液中存在水解平衡CH3COO-+H2O CH3COOH+OH—,且为吸热反应 CH3COOH+OH—,且为吸热反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-07更新
|
393次组卷
|
4卷引用:山东省青岛市黄岛区2020-2021学年高二上学期期末考试化学试题
名校
解题方法
8 . 磷酸铁锂是一种锂离子电池材料,该电池正极片主要含有石墨、Al、LiFePO4等物质,还有少量不溶性杂质。采用下列工艺流程回收制备有关物质。

已知:不同温度下,碳酸锂在水中的溶解度如下表所示:
请回答下列问题:
(1)为提高电极片的碱浸率,可以采用的方法有_______ (任写一条即可,题干中的除外)。
(2)得到滤渣2的离子方程式是_______ 。
(3)“沉淀池”中先加试剂X,试剂X不可选用_______ (填下列选项字母),Na2CO3溶液的作用是_______ 。
a.碘水 b.双氧水 c.氨水
(4)写出“滤渣”中加入NaOH溶液时发生反应的离子方程式_______ 。
(5)20℃时,“沉锂”后的溶液中Li2CO3的浓度为_______ mol·L-1(假设溶液密度为1.0148g·mL-1)。
(6)“沉锂”后所得固体需要进行洗涤,洗涤时最好选用_______ (填“冷水”或“热水”)。

已知:不同温度下,碳酸锂在水中的溶解度如下表所示:
| T/℃ | 0 | 10 | 20 | 30 | 50 | 60 | 80 | 100 |
| 溶解度/g | 1.64 | 1.53 | 1.48 | 1.17 | 1.05 | 1.01 | 0.85 | 0.72 |
(1)为提高电极片的碱浸率,可以采用的方法有
(2)得到滤渣2的离子方程式是
(3)“沉淀池”中先加试剂X,试剂X不可选用
a.碘水 b.双氧水 c.氨水
(4)写出“滤渣”中加入NaOH溶液时发生反应的离子方程式
(5)20℃时,“沉锂”后的溶液中Li2CO3的浓度为
(6)“沉锂”后所得固体需要进行洗涤,洗涤时最好选用
您最近一年使用:0次
2021-12-30更新
|
537次组卷
|
2卷引用:山东省实验中学2021-2022学年高三上学期第三次诊断考试化学试题
名校
9 . 由下列实验和现象所得到的结论或解释正确的是
| 实验 | 现象 | 结论 |
| A.向含有ZnS和Na2S的悬浊液中滴加CuSO4溶液 | 生成黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| B.取Al和Fe2O3反应所得的固体,溶于足量稀盐酸,滴加KSCN溶液 | 溶液不变红 | Al和Fe2O3反应后固体中不含Fe2O3 |
| C.将SO2通入溴水中 | 溴水褪色 | SO2有还原性 |
| D.①某溶液中加入Ba(NO3)2溶液 ②再加足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中有SO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . MnCO3是制造电信器材软磁铁氧体的原料。工业上利用软锰矿(主要成分为MnO2,还含有CaCO3、Fe2O3、Al2O3等杂质)制取碳酸锰的流程如图。

已知:还原焙烧主反应为2MnO2+C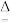 2MnO+CO2↑;Na2S2O8能将Mn2+氧化为MnO
2MnO+CO2↑;Na2S2O8能将Mn2+氧化为MnO
(1)步骤C中得到的滤渣的成分是___________ ,步骤D中还原剂与氧化剂的物质的量之比为___________ ,步骤E中调节pH至4.5的作用是___________ 。
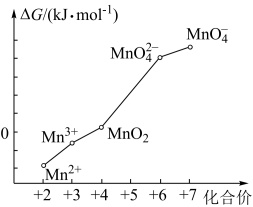
(2)pH=0的溶液中,不同价态含锰微粒的能量(∆G)如图。若某种含锰微粒的能量处于相邻价态两种微粒能量连线左上方,则该微粒不稳定并发生歧化反应,转化为相邻价态的微粒。图中五种含锰微粒中,不能稳定存在于pH=0的溶液中的离子有___________ 。
(3)步骤G的离子方程式为___________ 。
(4)设计实验证明步骤H中Mn2+是否已完全反应___________ 。
(5)实验室中利用固体KMnO4进行如图实验:

若标准状况下收集到气体H的体积为4.48L,则气体G的物质的量为____ 。

已知:还原焙烧主反应为2MnO2+C
 2MnO+CO2↑;Na2S2O8能将Mn2+氧化为MnO
2MnO+CO2↑;Na2S2O8能将Mn2+氧化为MnO
(1)步骤C中得到的滤渣的成分是
(2)pH=0的溶液中,不同价态含锰微粒的能量(∆G)如图。若某种含锰微粒的能量处于相邻价态两种微粒能量连线左上方,则该微粒不稳定并发生歧化反应,转化为相邻价态的微粒。图中五种含锰微粒中,不能稳定存在于pH=0的溶液中的离子有

(3)步骤G的离子方程式为
(4)设计实验证明步骤H中Mn2+是否已完全反应
(5)实验室中利用固体KMnO4进行如图实验:

若标准状况下收集到气体H的体积为4.48L,则气体G的物质的量为
您最近一年使用:0次



