1 . 在直流电源作用下,双极膜(膜a、膜b)中间层中的 解离为
解离为 和
和 。脂肪族二胺是一类重要的大宗化学品,我国科学家提出了化学电池法高效制备二胺,工作机理如图所示:
。脂肪族二胺是一类重要的大宗化学品,我国科学家提出了化学电池法高效制备二胺,工作机理如图所示:

下列说法错误的是
 解离为
解离为 和
和 。脂肪族二胺是一类重要的大宗化学品,我国科学家提出了化学电池法高效制备二胺,工作机理如图所示:
。脂肪族二胺是一类重要的大宗化学品,我国科学家提出了化学电池法高效制备二胺,工作机理如图所示:
下列说法错误的是
| A.电势:M电极<N电极 |
B.M极电极反应式为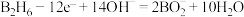 |
C.工作一段时间后,装置中需要定期补充 和 和 |
D.当N极制取 己二胺时,理论上有 己二胺时,理论上有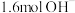 透过膜a 透过膜a |
您最近一年使用:0次
名校
2 . 电化学原理在电池制造、能量转换、物质合成等方面应用广泛。
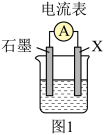
(1)若用如图1装置,依据反应Cu+2Fe3+=2Fe2++Cu2+设计原电池,则电极X应为_____ (填化学式),石墨电极的电极反应式为_____ 。将石墨换成铁电极后,电池总反应变为_____ 。
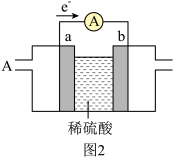
(2)燃料电池必须从电池外部源源不断地向电池提供天然气、甲烷、煤气等含氢化合物作为燃料。基于甲烷(CH4)-空气燃料电池,其工作原理如图2,a、b均为惰性电极。a为_____ 极,正极的电极反应式为_____ 。当通入4.48L(标准状况下)甲烷气体时,测得电路中转移1.1mol电子,则甲烷的利用率为_____ 。(保留小数点后1位)。
(3)在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图3所示:

已知H2O在电极附近发生电极反应H2O+2e-=H2+O2-,则CO2发生的电极反应为_____ 。当H2和CO共生成2mol时,生成标准状况下O2的体积为_____ 。
(1)若用如图1装置,依据反应Cu+2Fe3+=2Fe2++Cu2+设计原电池,则电极X应为

(2)燃料电池必须从电池外部源源不断地向电池提供天然气、甲烷、煤气等含氢化合物作为燃料。基于甲烷(CH4)-空气燃料电池,其工作原理如图2,a、b均为惰性电极。a为

(3)在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图3所示:

已知H2O在电极附近发生电极反应H2O+2e-=H2+O2-,则CO2发生的电极反应为
您最近一年使用:0次
2023-04-29更新
|
237次组卷
|
2卷引用:山东省菏泽市2022-2023学年高一下学期期中考试化学(A)试题
名校
3 . 由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
(1)装置甲中作正极的是__________________ (填“A”或“B”) ;
(2)装置乙溶液中C电极反应:__________________________________ ;装置乙中反应一段时间后,测得C电极 的质量增加12.8克,则该电池反应转移电子的物质的量为___________ mol
(3)装置丙中金属A上电极反应属于______________ (填“氧化反应”或“还原反应”);
(4)四种金属活动性由强到弱的顺序是_______________________ 。
| 装置 | 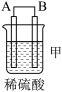 | 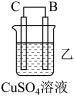 | 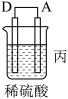 |
| 现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中作正极的是
(2)装置乙溶液中C电极反应:
(3)装置丙中金属A上电极反应属于
(4)四种金属活动性由强到弱的顺序是
您最近一年使用:0次
2019-03-28更新
|
531次组卷
|
3卷引用:【全国百强校】山东省邹平市第一中学2018-2019学年高一下学期第一次阶段性考试化学试题
4 . 化学性质类似 的盐酸羟胺(
的盐酸羟胺( )是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有
)是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有 、
、 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是

 的盐酸羟胺(
的盐酸羟胺( )是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有
)是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有 、
、 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是
| A.图1电池工作时,Pt电极是正极 |
B.图2中,A为 和 和 ,B为 ,B为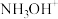 |
C.电极b接电源负极,处理 ,酸性废水中 ,酸性废水中 减少 减少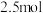 |
D.电池工作时,每消耗 (标准状况下),左室溶液质量增加 (标准状况下),左室溶液质量增加 |
您最近一年使用:0次
名校
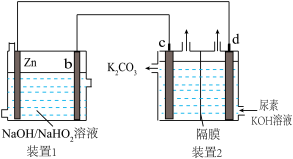
5 . 目前研究较多的Zn-H2O2电池,其电池总反应为Zn+OH-+HO =ZnO
=ZnO +H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
+H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
 =ZnO
=ZnO +H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
+H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
| A.装置1中OH-移向Zn电极 |
| B.反应过程中,d极附近的pH增大 |
C.电极c的主要反应式为CO(NH2)2-6e-+8OH-=CO +N2+6H2O +N2+6H2O |
| D.通电一段时间后,若Zn电极的质量减轻19.5g,则c电极产生N22.24L(标准状况) |
您最近一年使用:0次
名校
解题方法
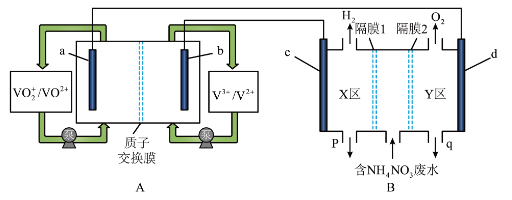
6 . 全钒液流电池是化学储能领域的一个研究热点,储能容量大、使用寿命长,利用该电池电解处理含 的废水制备硝酸和氨水的原理如图所示,
的废水制备硝酸和氨水的原理如图所示, 电极均为惰性电极。
电极均为惰性电极。
回答下列问题:
(1) 电极为
电极为___________ (填“正极”或“负极”), 电极反应式为
电极反应式为___________ 。
(2)隔膜1为___________ 交换膜(填“阴离子”或“阳离子”),q口流出液含有的溶质为___________ (填化学式),d电极的电极反应式为___________ 。
(3)B装置中产生的气体总量为 (标准状况下)时,通过质子交换膜的
(标准状况下)时,通过质子交换膜的  的物质的量为
的物质的量为___________  。
。
 的废水制备硝酸和氨水的原理如图所示,
的废水制备硝酸和氨水的原理如图所示,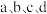 电极均为惰性电极。
电极均为惰性电极。
回答下列问题:
(1)
 电极为
电极为 电极反应式为
电极反应式为(2)隔膜1为
(3)B装置中产生的气体总量为
 (标准状况下)时,通过质子交换膜的
(标准状况下)时,通过质子交换膜的  的物质的量为
的物质的量为 。
。
您最近一年使用:0次
名校
解题方法
7 . 盐酸羟胺(NH3OHCl)是一种常见的还原剂和显像剂,其化学性质与NH4Cl类似。工业上主要采用电化学法制备,装置如图1所示,含Fe的催化电极反应机理如图2所示,不考虑溶液体积的变化。
下列说法正确的是

下列说法正确的是

| A.电池工作时,Pt电极为正极 |
| B.图2中,M为H+,N为NH3OH+ |
| C.电池工作时,每消耗2.24LNO左室溶液质量增加3.3g |
| D.电池工作一段时间后,正极区溶液的pH减小 |
您最近一年使用:0次
2024-02-11更新
|
146次组卷
|
2卷引用:山东省淄博市部分学校2023-2024学年高三上学期联考化学试卷
名校
解题方法
8 . 我国科学家设计可同时实现, 制备和海水淡化的新型电池,装置意图如图,下列说法
制备和海水淡化的新型电池,装置意图如图,下列说法不正确 的是
 制备和海水淡化的新型电池,装置意图如图,下列说法
制备和海水淡化的新型电池,装置意图如图,下列说法
| A.电极a是正极 |
B.电极b的反应式: |
C.每生成 ,有 ,有 发生迁移 发生迁移 |
| D.离子交换膜c、d分别是阴离子交换膜和阳离子交换膜 |
您最近一年使用:0次
2023-12-11更新
|
344次组卷
|
2卷引用:山东省临沂市平邑县第一中学西校区2023-2024学年高二上学期元旦竞赛考试化学试题
名校
解题方法
9 . 目前,我国光伏发电并网装机容量稳居全球首位。以四甲基氯化铵[(CH3)4NCl]为原料,采用光伏并网发电装置,通过电渗析法合成(CH3)4NOH,工作原理如图。下列说法正确的是
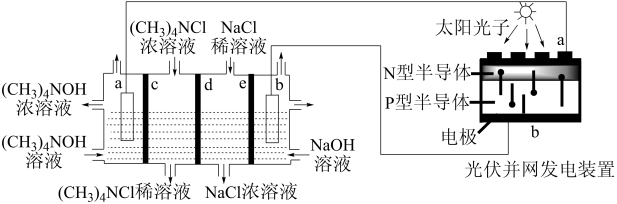

| A.光伏并网发电装置中N型半导体为负极 |
B.c 阳离子交换膜,d、e均为阴离子交换膜 阳离子交换膜,d、e均为阴离子交换膜 |
| C.保持电流恒定,升高温度可加快合成四甲基氢氧化铵的速率 |
| D.制备182g四甲基氢氧化铵,两极共产生33.6L气体(标准状况) |
您最近一年使用:0次
名校
10 . 电化学的应用十分广泛,在分析检测、有机合成等领域应用很广,请分析下列几种电化学装置并回答问题:
Ⅰ.微生物燃料电池是废水处理中实现碳氮联合转化产生CO2和N2的装置,如图所示,1、2为厌氧微生物电极,3为阳离子交换膜,4为好氧微生物反应器。请回答:
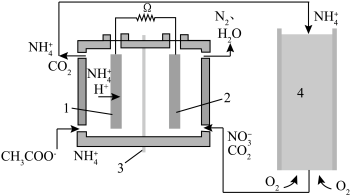
(1)电极2名称:___________ 极,电池工作一段时间后,电极2附近的pH___________ (填“增大”“减小”或“不变”)。
(2)在好氧微生物反应器中发生的反应方程式___________ 。
(3)若反应消耗O2(标准状况)4.48L,理论上生成N2物质的量为___________ mol。
II.次磷酸钴(II)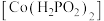 广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图。
广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图。
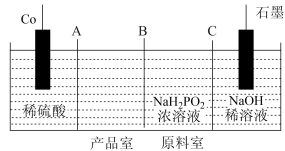
(4)A、B、C均为离子交换膜,其中为阳离子交换膜的是___________ 。
(5)石墨电极每生成1molH2时,___________ 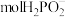 向
向___________ 迁移(填“阴极室”“阳极室”或“产品室”)。
(6)若以铅蓄电池为直流电源,则铅蓄电池中正极的电极反应式为___________ 。
(7)用 溶液化学镀钴是在强碱性条件下通过发生自身氧化还原反应,反应的同时会生成
溶液化学镀钴是在强碱性条件下通过发生自身氧化还原反应,反应的同时会生成 ,其离子方程式为
,其离子方程式为___________ 。
Ⅰ.微生物燃料电池是废水处理中实现碳氮联合转化产生CO2和N2的装置,如图所示,1、2为厌氧微生物电极,3为阳离子交换膜,4为好氧微生物反应器。请回答:

(1)电极2名称:
(2)在好氧微生物反应器中发生的反应方程式
(3)若反应消耗O2(标准状况)4.48L,理论上生成N2物质的量为
II.次磷酸钴(II)
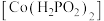 广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图。
广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图。
(4)A、B、C均为离子交换膜,其中为阳离子交换膜的是
(5)石墨电极每生成1molH2时,
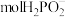 向
向(6)若以铅蓄电池为直流电源,则铅蓄电池中正极的电极反应式为
(7)用
 溶液化学镀钴是在强碱性条件下通过发生自身氧化还原反应,反应的同时会生成
溶液化学镀钴是在强碱性条件下通过发生自身氧化还原反应,反应的同时会生成 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次



