1 . 利用下列装置和试剂进行实验,能达到实验目的的是
A.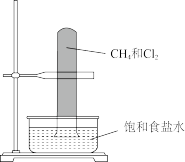 甲烷与氯气暗处发生取代反应 甲烷与氯气暗处发生取代反应 |
B. 比较Zn与Cu的金属性 比较Zn与Cu的金属性 |
C. 蒸干FeCl3溶液,制备无水FeCl3固体 蒸干FeCl3溶液,制备无水FeCl3固体 |
D.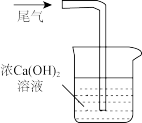 实验室处理尾气SO2 实验室处理尾气SO2 |
您最近一年使用:0次
2022-08-16更新
|
204次组卷
|
2卷引用:重庆市巴蜀中学2023届高三第一次高考适应性月考化学试题
名校
解题方法
2 . 请回答下列问题:
(1)铅酸蓄电池是一种可充电电池,其总反应式为Pb+PbO2+2H2SO4 2PbSO4+2H2O,原电池负极的电极反应式为
2PbSO4+2H2O,原电池负极的电极反应式为_______ ,正极附近溶液的pH_______ (填“增大”、“不变”或“减小”)。
(2)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是_______ ,写出正极的电极反应式_______ 。若开始时两极质量相等,当导线中通过0.2mol电子时,两个电极的质量差为_______ 。
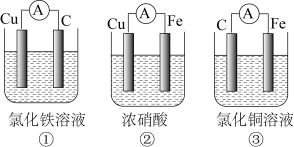
(3)乙醇燃料电池技术方面获得新突破,乙醇(CH3CH2OH)燃料电池的工作原理如图所示。
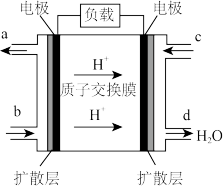
①该电池工作时,c入口处对应的电极为_______ (填“正”或“负”)极,b处入口的物质为_______
②工作一段时间后,当2.3 g乙醇完全反应生成CO2时,外电路中通过的电子数目为_______ 。
(1)铅酸蓄电池是一种可充电电池,其总反应式为Pb+PbO2+2H2SO4
 2PbSO4+2H2O,原电池负极的电极反应式为
2PbSO4+2H2O,原电池负极的电极反应式为(2)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是
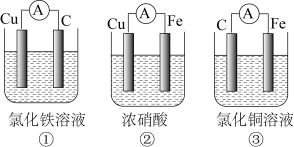
(3)乙醇燃料电池技术方面获得新突破,乙醇(CH3CH2OH)燃料电池的工作原理如图所示。

①该电池工作时,c入口处对应的电极为
②工作一段时间后,当2.3 g乙醇完全反应生成CO2时,外电路中通过的电子数目为
您最近一年使用:0次
2022-11-02更新
|
537次组卷
|
2卷引用:重庆市璧山来凤中学2022-2023学年高二上学期期中考试化学试题
名校
3 . I.如图所示,某同学设计了一个燃料电池并进行电解实验,请回答下列问题:

(1)甲池中通____ (填“氧气”或“甲烷”)的是负极,其电极反应式为____ 。
(2)标准状况下,若有2.24L氧气参加反应,则乙装置中铁电极上生成气体的物质的量为____ mol。
(3)丙池中铜片上可观察到的现象为____ 。
II.据报道,我国已研制出“可充室温钠-二氧化碳电池”,如图所示,该电池的工作原理为4Na+3CO2 Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。
Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。

(4)放电时,钠箔为该电池的____ 极(填“正”或“负”):电解质溶液中ClO 流向
流向____ (填“钠箔”或“多壁碳纳米管”)电极。
(5)充电时,多糖碳纳米管连接直流电源的____ (填“正”或“负”)极,其电极反应式为____ 。

(1)甲池中通
(2)标准状况下,若有2.24L氧气参加反应,则乙装置中铁电极上生成气体的物质的量为
(3)丙池中铜片上可观察到的现象为
II.据报道,我国已研制出“可充室温钠-二氧化碳电池”,如图所示,该电池的工作原理为4Na+3CO2
 Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。
Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。
(4)放电时,钠箔为该电池的
 流向
流向(5)充电时,多糖碳纳米管连接直流电源的
您最近一年使用:0次
名校
解题方法
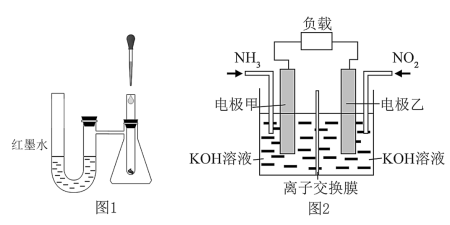
4 . (1)为了探究化学反应的热效应,某兴趣小组采用如图1所示装置进行实验:将稀盐酸滴入装入铁粉的试管中,U形管内的现象为_____ ,发生的反应是_____ (填“放热”或“吸热”)反应,以下选项中与其能量变化相同的是_______ (填字母)。
A.盐酸与碳酸氢钠的反应B.CaCO3的分解反应
C.食物的缓慢氧化D.Ba(OH)2•8H2O和NH4Cl的反应
E.H2和Cl2的反应
(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为_____ 。
A.铝片、铝片B.铜片、铜片C.铝片、铜片D.铜片、铝片
(3)雾霾中含有氮的氧化物,利用反应NO2+NH3→N2+H2O(未配平)制作如图2所示的电池,用以消除氮氧化物的污染。电极甲是_____ 极,电池工作时,OH-定向移向______ 电极(填“甲”或“乙”),写出负极电极反应式:_____ ,若一段时间内测得外电路中有1.2mol电子通过,则负极比正极产生的气体多____ L(标准状况下)。
A.盐酸与碳酸氢钠的反应B.CaCO3的分解反应
C.食物的缓慢氧化D.Ba(OH)2•8H2O和NH4Cl的反应
E.H2和Cl2的反应

(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铝片B.铜片、铜片C.铝片、铜片D.铜片、铝片
(3)雾霾中含有氮的氧化物,利用反应NO2+NH3→N2+H2O(未配平)制作如图2所示的电池,用以消除氮氧化物的污染。电极甲是
您最近一年使用:0次
5 . 工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电板上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是
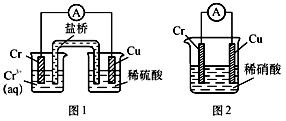

| A.图1为原电池装置,盐桥中的阴离子移向Cu电极的烧杯中 |
| B.由实验现象可知:金属活动性Cu>Cr |
| C.图2装置中Cu电极上发生的电极反应式为:Cu-2e-=Cu2+ |
| D.两个装置中,电子均由Cr电极流向Cu电极 |
您最近一年使用:0次
2018-04-10更新
|
239次组卷
|
2卷引用:重庆市第一中学2017-2018学年高二下学期第一次月考化学试题
名校
解题方法
6 . 电化学原理在能量转化,物质制备及环境保护等领域均有广泛应用,请按要求回答下列问题:
一种以液态肼(N2H4)为燃料的电池装置如图甲所示,该电池用KOH溶液作为电解质溶液。以该燃料电池作为电源电解足量的饱和CuSO4溶液以实现向铁棒上镀铜,装置如图乙所示。
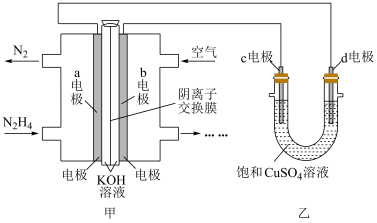
(1)b电极为燃料电池的_______ 极(填“ 正”或“负”)。a电极反应式为_______________ ,c电极应选用的电极材料为_____ (填“铁”或“铜” ) 。若c、d电极均为惰性电极,则c电极反应式应为_____________________________ ,装置乙总反应为___________________
氰化物有剧毒,在含氰工业废水排放前,需要对其进行治理。在碱性条件下利用电解法除去废水中的氯化物(以CN- 代表),装置如图丙,已知石墨电极上依次发生的部分反应有:
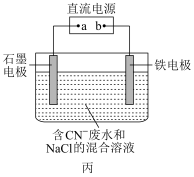
a.CN-+ 2OH--2e -=CNO- + H2O
b.2Cl--2e- = Cl2↑
c.3Cl2+ 2CNO -+ 8OH-=N2↑+6C1-+ 2CO + 4H2O
+ 4H2O
(2)铁电极上发生的电极反应为__________________
(3)忽略铁电极上的其他反应,电解一段时间后,相同条件下在石墨电极处测得产生N2 a mL,同时在铁电极处产生气体b mL,则氰去除率为_______ (氰去除率= 100%)
100%)
一种以液态肼(N2H4)为燃料的电池装置如图甲所示,该电池用KOH溶液作为电解质溶液。以该燃料电池作为电源电解足量的饱和CuSO4溶液以实现向铁棒上镀铜,装置如图乙所示。

(1)b电极为燃料电池的
氰化物有剧毒,在含氰工业废水排放前,需要对其进行治理。在碱性条件下利用电解法除去废水中的氯化物(以CN- 代表),装置如图丙,已知石墨电极上依次发生的部分反应有:

a.CN-+ 2OH--2e -=CNO- + H2O
b.2Cl--2e- = Cl2↑
c.3Cl2+ 2CNO -+ 8OH-=N2↑+6C1-+ 2CO
 + 4H2O
+ 4H2O(2)铁电极上发生的电极反应为
(3)忽略铁电极上的其他反应,电解一段时间后,相同条件下在石墨电极处测得产生N2 a mL,同时在铁电极处产生气体b mL,则氰去除率为
 100%)
100%)
您最近一年使用:0次
名校
解题方法
7 . 盐酸羟胺(NH2OH⋅HCl)在水中完全电离为NH3OH+和Cl−,可利用如下装置来制备盐酸羟胺。以盐酸为离子导体,向两电极分别通入NO和H2。下列说法正确的是
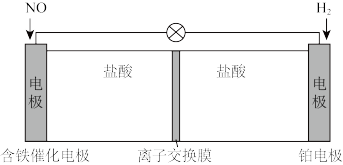

| A.铂电极为正极 |
| B.离子交换膜为阴离子交换膜,Cl−从左室移向右室 |
| C.含铁催化电极上的反应为:NO+3e−+4H+=NH3OH+ |
| D.每生成1mol盐酸羟胺电路中转移4mol e− |
您最近一年使用:0次
2022-11-28更新
|
211次组卷
|
3卷引用:重庆2023届拔尖强基联合11月定时检测化学试题
8 . 盐酸羟胺 主要用作还原剂和定影剂,是一种易溶于水的盐。以
主要用作还原剂和定影剂,是一种易溶于水的盐。以 、
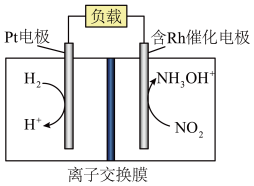
、 、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。下列说法错误的是
、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。下列说法错误的是
 主要用作还原剂和定影剂,是一种易溶于水的盐。以
主要用作还原剂和定影剂,是一种易溶于水的盐。以 、
、 、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。下列说法错误的是
、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。下列说法错误的是
A.盐酸羟胺在水溶液中的电离方程式为: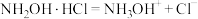 |
B.正极的电极反应为: |
| C.该电化学装置中的离子交换膜最好选择质子交换膜 |
D.电池工作时,每消耗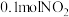 ,右室溶液质量增加 ,右室溶液质量增加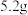 |
您最近一年使用:0次
2023-04-23更新
|
271次组卷
|
2卷引用:重庆市育才中学校2022-2023学年高一下学期期中考试化学试题
名校
解题方法
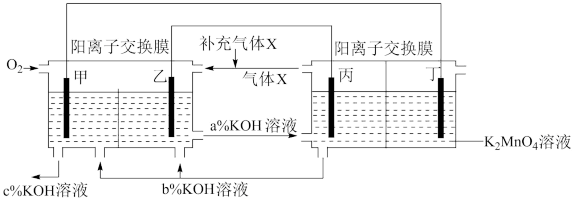
9 . 一种将燃料电池与电解池组合制备 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
| A.甲为正极,丙为阴极 |
B.丁极的电极反应式为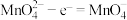 |
C.KOH溶液的质量分数: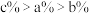 |
D.标准状况下,乙电极上每消耗 气体时,理论上有 气体时,理论上有 移入阴极区 移入阴极区 |
您最近一年使用:0次
2022-05-29更新
|
665次组卷
|
7卷引用:重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题
重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题(已下线)课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省株洲市第一中学2022届高三下学期第三次模拟考试化学试题四川省泸州市泸县第五中学2021-2022学年高三下学期二诊模拟考试理综化学试题河南省南阳市第一中学校2022-2023学年高三上学期12月月考化学试题
解题方法
10 . 请回答下列问题:
(1)把A、B、C、D四种金属按表中装置进行实验。
根据表中信息判断四种金属活动性由大到小的顺序是_______ ;写出装置乙中正极的电极反应式:_______ 。
(2)锂离子电池已经成为新一代实用的蓄电池,它具有能量密度大、电压高的特性。某锂离子电池放电时电极反应如下:
负极Li-e-=Li+,
正极Li1-xMnO2+xLi++xe-=LiMnO2
该锂离子电池放电时电池的反应方程式为_______ 。
(3)H2还原CO电化学法制备甲醇(CO+2H2=CH3OH)的工作原理如下图所示:
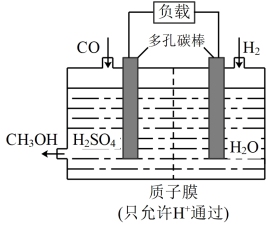
通入H2的一端是电池的_______ 极(填“正”或“负”),电池工作过程中H+通过质子膜向_______ (填“左”或者“右”)移动,通入CO的一端发生的电极反应式为_______ 。
(1)把A、B、C、D四种金属按表中装置进行实验。
| 装置 | 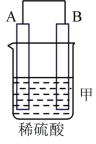 | 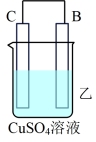 | 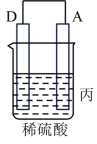 |
| 电子从A到B | C电极的质量增加 | 二价金属D不断溶解 |
(2)锂离子电池已经成为新一代实用的蓄电池,它具有能量密度大、电压高的特性。某锂离子电池放电时电极反应如下:
负极Li-e-=Li+,
正极Li1-xMnO2+xLi++xe-=LiMnO2
该锂离子电池放电时电池的反应方程式为
(3)H2还原CO电化学法制备甲醇(CO+2H2=CH3OH)的工作原理如下图所示:

通入H2的一端是电池的
您最近一年使用:0次



