名校
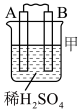
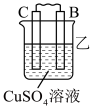
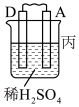
1 . 由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象判断下列说法错误 的是
| 装置 |
|
|
|
| 现象 | A上有气体产生 | B的质量增加 | 二价金属A不断溶解 |
A.装置甲中正极的电极反应式是: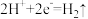 |
| B.装置乙中B为负极 |
| C.四种金属的活泼性强弱顺序为:C>B>A>D |
D.装置丙中负极电极反应式为: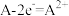 |
您最近一年使用:0次
名校
2 . 完成下列问题。
(1)下列反应中,属于放热反应的是___________ (填字母,下同),属于吸热反应的是___________ 。
a.盐酸与烧碱溶液反应 b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.葡萄糖在人体内氧化分解
(2)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。
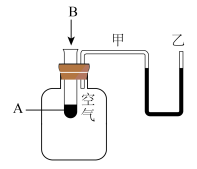
试回答下列问题:
①该反应为___________ 反应(填“放热”或“吸热”)。
②该反应的反应物化学键断裂吸收的能量________ (填“高”或“低”)于生成物化学键形成放出的能量。
(3) A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲溶液中的阴离子移向________ (填“A”或“B”)极。
②装置乙中正极的电极反应式为________ 。
③四种金属活动性由强到弱的顺序是________ 。
(4)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如下图所示:
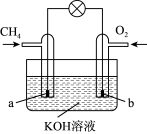
①外电路电子移动方向:___________ (填“a极到b极”或“b极到a极”)。
②a电极的电极方程式为___________ 。
(1)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应 b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.葡萄糖在人体内氧化分解
(2)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。

试回答下列问题:
①该反应为
②该反应的反应物化学键断裂吸收的能量
(3) A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 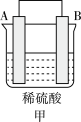 |  |  |
| 现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲溶液中的阴离子移向
②装置乙中正极的电极反应式为
③四种金属活动性由强到弱的顺序是
(4)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如下图所示:

①外电路电子移动方向:
②a电极的电极方程式为
您最近一年使用:0次
3 . 某科学探究小组为探究电化学原理, 设计了如图所示的装置进行探究实验。下列对实验中观察到的现象或相关结论的叙述错误的是
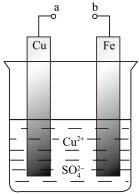

| A.a和b不连接时,铁片上有红色的铜析出 |
| B.a和b用导线连接时, 铜片为负极 |
| C.无论a和b是否连接,反应的本质相同,铁片均会被氧化,溶液中均有Fe2+生成 |
| D.a和b用导线连接时,溶液中的Cu2+应向铜电极移动且能更快地在铜电极上析出铜 |
您最近一年使用:0次
名校
解题方法
4 . 对右图所示的装置中实验现象的描述正确的是
| 选项 | a电极 | b电极 | X溶液 | 实验现象 | 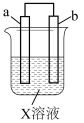 |
| A | 石墨 | 石墨 | CuCl2溶液 | a极质量增加,b极放出无色气体 | |
| B | Cu | Fe | KNO3溶液 | a极质量增加,b极放出无色气体 | |
| C | 石墨 | Fe |  溶液 溶液 | a极质量增加,b极质量减小 | |
| D | 石墨 | Zn | HCl溶液 | a放出无色气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 回答下列问题:
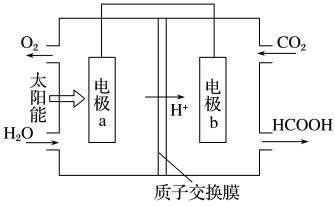
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作____ 极,表面发生的电极反应为____ 。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。
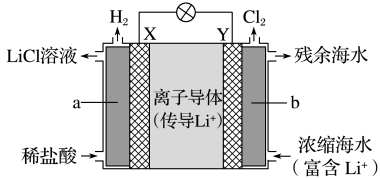
①X为____ 极,Y极反应式为_____ 。
②Y极生成1molCl2时,____ molLi+移向____ (填“X”或“Y”)极。
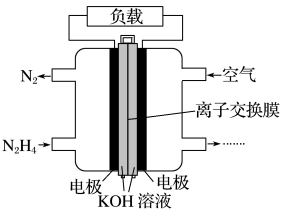
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH作电解质。负极反应式为____ ;正极反应式为____ 。
(4)Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为2AgCl+Mg=Mg2++2Ag+2Cl-。
①负极反应式为_____ ;
②正极反应式为_____ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作

(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

①X为
②Y极生成1molCl2时,
(3)一种以肼(N2H4)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH作电解质。负极反应式为

(4)Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为2AgCl+Mg=Mg2++2Ag+2Cl-。
①负极反应式为
②正极反应式为
您最近一年使用:0次
名校
解题方法
6 . Ⅰ.回答下列问题
(1)利用反应Cu+2FeCl3=CuCl2+2FeCl2,设计成如图所示的原电池,回答下列问题:
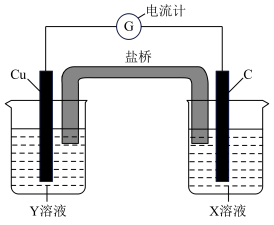
①写出电极反应式。正极:_______ ;负极:_______ 。
②图中X溶液的溶质是_______ (填化学式,下同),Y溶液的溶质是_______ 。
③原电池工作时,盐桥中的_______ (填“阳”或“阴”)离子向X溶液方向移动。
(2)控制合适的条件将反应2Fe3++2I-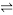 2Fe2++I2设计成如图所示的原电池。请回答下列问题:
2Fe2++I2设计成如图所示的原电池。请回答下列问题:

①反应开始时,乙中石墨电极上发生_______ (填“氧化”或“还原”,下同)反应,电极反应式为_______ 。甲中石墨电极上发生_______ 反应,电极反应式为_______ 。
②电流计读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作_______ (填“正”或“负”)极,该电极的电极反应式为_______ 。
(3)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为_______ 。
Ⅱ.已知:①将 0.1 mol·Lˉ1KI 溶液加入到 0.1 mol·L-1 FeCl3溶液中时,可以看到溶液颜色加深,滴加淀粉后溶液变为蓝色;
②当离子浓度相同时,氧化性:Ag+>Fe3+;
③ 若浓度减小时,离子的氧化性也会随之减弱。
(4)甲同学猜测,0.1 mol·Lˉ1 KI 溶液(加入几滴淀粉溶液)加入0.1mol·Lˉ1AgNO3 溶液中时,溶液应变蓝色。请写出该猜测对应的离子方程式_______ 。实验结果未见到蓝色。
(5)乙同学认为甲同学的实验方案有问题,理由是_______ 。请设计原电池证明Ag+也能氧化 Iˉ,画出装置图,并标明电极材料及电解质溶液。______
(1)利用反应Cu+2FeCl3=CuCl2+2FeCl2,设计成如图所示的原电池,回答下列问题:

①写出电极反应式。正极:
②图中X溶液的溶质是
③原电池工作时,盐桥中的
(2)控制合适的条件将反应2Fe3++2I-
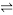 2Fe2++I2设计成如图所示的原电池。请回答下列问题:
2Fe2++I2设计成如图所示的原电池。请回答下列问题:
①反应开始时,乙中石墨电极上发生
②电流计读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作
(3)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为
Ⅱ.已知:①将 0.1 mol·Lˉ1KI 溶液加入到 0.1 mol·L-1 FeCl3溶液中时,可以看到溶液颜色加深,滴加淀粉后溶液变为蓝色;
②当离子浓度相同时,氧化性:Ag+>Fe3+;
③ 若浓度减小时,离子的氧化性也会随之减弱。
(4)甲同学猜测,0.1 mol·Lˉ1 KI 溶液(加入几滴淀粉溶液)加入0.1mol·Lˉ1AgNO3 溶液中时,溶液应变蓝色。请写出该猜测对应的离子方程式
(5)乙同学认为甲同学的实验方案有问题,理由是
您最近一年使用:0次
名校
解题方法
7 . 盐酸羟胺(NH3OHCl)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
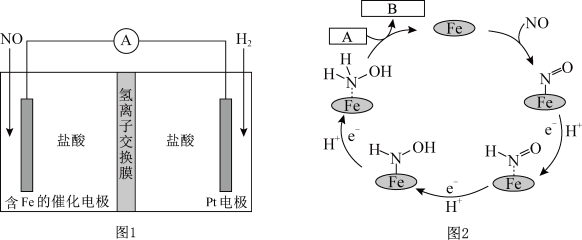

| A.电池工作时,Pt电极是正极 |
| B.图2中,A为H+和e-,B为NH3OH+ |
| C.电池工作时,每消耗2.24LNO(标准状况下),左室溶液质量增加3.3g |
| D.电池工作一段时间后,正、负极区溶液的pH均下降 |
您最近一年使用:0次
2022-04-20更新
|
2085次组卷
|
14卷引用:江苏省南京市第十三中学2022届高三下学期适应性考试化学试题
江苏省南京市第十三中学2022届高三下学期适应性考试化学试题江苏省南京市雨花台中学2022-2023学年高二上学期10月月考化学试题江苏省镇江中学2022-2023学年高一下学期期中考试化学试题江苏省常州市第一中学2022-2023学年高一下学期期末测试化学试题江苏省前黄高级中学2023-2024学年高三上学期期中适应性考试化学试题福建省福州市2022届高中毕业班(3月)第二次质量检测化学试题湖南省大联考雅礼十六校2021-2022学年高三第二次联考化学试题(已下线)秘籍12 原电池原理及应用-备战2022年高考化学抢分秘籍(全国通用)河北省石家庄市第二中学2022届高三下学期5月模拟考试化学试题湖南省郴州市2023届高三下学期第三次教学质量监测化学试题湖南省常德市第一中学2022-2023学年高三下学期5月月考化学试题福建省漳州第一中学2023届高三下学期毕业班质检考化学试题福建省南平第一中学2023-2024学年高三上学期第二次阶段考化学试题福建省厦门第一中学2023-2024学年高二上学期10月月考试化学试题
20-21高二上·江苏镇江·阶段练习
8 . 污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某化学研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已略去)。
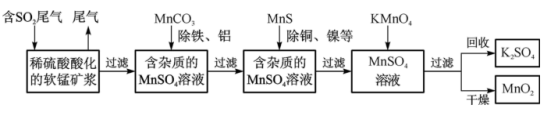
请回答下列问题:
(1)已知:25℃、101 kPa时,
Mn(s)+O2(g)=MnO2(s) ΔH=-520 kJ·mol-1
S(s)+O2(g)=SO2(g) ΔH=-297 kJ·mol-1
Mn(s)+S(s)+2O2(g)=MnSO4(s) ΔH=-1065 kJ·mol-1
SO2与MnO2反应生成无水MnSO4的热化学方程式是___________ 。请画出该反应的能量变化示意图___________ 。

(2)用惰性电极电解硫酸酸化的硫酸锰溶液制备MnO2的装置如下图所示。
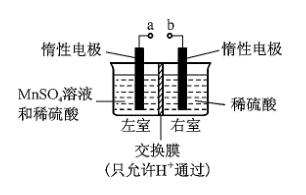
①a应与直流电源的___________ (填“正”或“负”)极相连。
②电解过程中氢离子的作用是___________ ;若转移的电子数为6.02×1023,左室溶液中最终n(H+)的变化量为___________ 。
(3)①MnO2是碱性锌锰电池的正极材料。碱性锌锰电池放电时正极生成MnOOH,正极的电极反应式是___________ 。
②据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星,其工作原理如下图所示。
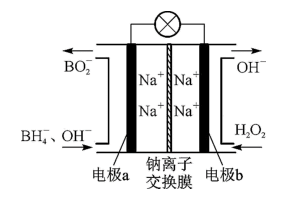
则该电池放电时通入H2O2的一极为___________ 极,电极反应式为___________ ;通入NaBH4的一极电极反应式为___________ 。

请回答下列问题:
(1)已知:25℃、101 kPa时,
Mn(s)+O2(g)=MnO2(s) ΔH=-520 kJ·mol-1
S(s)+O2(g)=SO2(g) ΔH=-297 kJ·mol-1
Mn(s)+S(s)+2O2(g)=MnSO4(s) ΔH=-1065 kJ·mol-1
SO2与MnO2反应生成无水MnSO4的热化学方程式是

(2)用惰性电极电解硫酸酸化的硫酸锰溶液制备MnO2的装置如下图所示。

①a应与直流电源的
②电解过程中氢离子的作用是
(3)①MnO2是碱性锌锰电池的正极材料。碱性锌锰电池放电时正极生成MnOOH,正极的电极反应式是
②据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星,其工作原理如下图所示。

则该电池放电时通入H2O2的一极为
您最近一年使用:0次
9-10高一下·江苏扬州·期末
9 . 按下图装置进行实验,并回答下列问题:
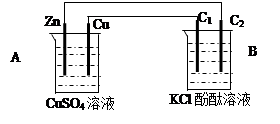
(1)判断装置的名称:A池为___________ ;B池为______________ ;
(2)锌极为________ 极,电极反应式为___________________________________ ;铜极为________ 极,电极反应式为___________________________________ ;石墨棒C1为______ 极,电极反应式为__________________________________ ;石墨棒C2附近发生的实验现象为______________________________________ ;
(3)当C2极析出224mL气体(标准状态)时,锌的质量变化_________ (变大、不变或变小)了________ g,CuSO4溶液的质量_________ (增加、不变或减少)_________ g。
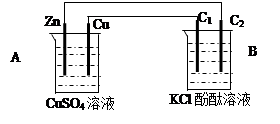
(1)判断装置的名称:A池为
(2)锌极为
(3)当C2极析出224mL气体(标准状态)时,锌的质量变化
您最近一年使用:0次
2014-07-16更新
|
782次组卷
|
11卷引用:2010年江苏省江都中学高一第二学期期末考试化学试题
(已下线)2010年江苏省江都中学高一第二学期期末考试化学试题(已下线)2011-2012学年河北省唐山一中高二上学期期中考试化学(理)试卷(已下线)2011-2012学年福建省厦门一中高二上学期期中考试化学试卷(已下线)2013-2014福建省安溪八中高二下学期期末考试化学试卷2015-2016学年河北省容城中学高二上学期第一次月考化学试卷云南省临沧市凤庆县第二中学2019-2020学年高三第一学期开学考试化学试题(已下线)考点09 原电池及化学电源——《备战2020年高考精选考点专项突破题集》贵州省惠水县第一高级中学2019-2020学年高三上学期期末考试化学试题宁夏回族自治区中卫市中宁县中宁中学2019-2020学年高二下学期阶段测试化学试题鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第3节 电能转化为化学能——电解福建省仙游县郊尾中学2020届高三上学期期中考试化学试题
10 . 现以CO、O2、熔融盐Z(Na2CO3)组成的燃料电池,采用电解法处理CO同时制备N2O5,装置如图所示,其中Y为CO2。下列说法不合理的是
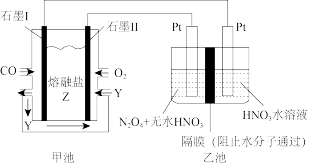

| A.石墨Ⅰ是原电池的负极,发生氧化反应 |
| B.甲池中的CO32-向石墨Ⅱ极移动 |
| C.石墨Ⅰ的电极反应式:CO+CO32--2e-=2CO2 |
| D.若甲池消耗标准状况下的氧气2.24L,则乙池中产生氢气0.2mol |
您最近一年使用:0次