解题方法
1 . 下列实验操作能达到实验目的的是
A.用瓷坩埚高温熔融 固体 固体 |
B.用 气体和NaOH溶液做喷泉实验 气体和NaOH溶液做喷泉实验 |
C.直接加热 固体制备氨气 固体制备氨气 |
| D.用Mg、Al、NaOH溶液设计一个原电池装置,且Mg做电池的负极 |
您最近一年使用:0次
2022-04-21更新
|
151次组卷
|
2卷引用:浙江省A9协作体2021-2022学年高一下学期 期中联考化学试题
名校
解题方法
2 . 下列各实验的方案设计、现象及结论都正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将少量Fe(NO3)2加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成红色 | Fe(NO3)2不一定变质 |
| B | 镁、铝为电极,氢氧化钠为电解质的原电池装置 | 铝表面有气泡 | 金属活动性:Mg>Al |
| C | 向待测液中滴加浓氢氧化钠溶液并加热 | 产生使湿润蓝色石蕊试纸变红的气体 | 待测液中含有 |
| D | 将灼热的木炭加入到浓硝酸中 | 有红棕色气体产生 | 木炭在加热时能与浓硝酸发生反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 某科学探究小组为探究电化学原理, 设计了如图所示的装置进行探究实验。下列对实验中观察到的现象或相关结论的叙述错误的是
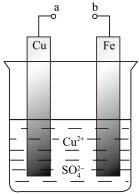

| A.a和b不连接时,铁片上有红色的铜析出 |
| B.a和b用导线连接时, 铜片为负极 |
| C.无论a和b是否连接,反应的本质相同,铁片均会被氧化,溶液中均有Fe2+生成 |
| D.a和b用导线连接时,溶液中的Cu2+应向铜电极移动且能更快地在铜电极上析出铜 |
您最近一年使用:0次
名校
解题方法
4 . 由A、B、C、D四种金属按表中装置进行实验,下列叙述中正确的是
| 实验装置与现象 | |||
| 装置 | 甲 | 乙 | 丙 |
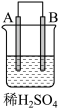 | 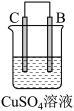 | 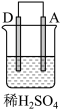 | |
| 现象 | A不断溶解 | C的质量增加 | A上有气体产生 |
| A.装置甲中的B金属是原电池的负极 | B.装置乙中的C金属是原电池的阳极 |
| C.装置丙中的D金属是原电池的正极 | D.四种金属的活泼性顺序是D>A>B>C |
您最近一年使用:0次
2022-09-16更新
|
99次组卷
|
5卷引用:浙江省2018版考前特训(2017年10月):选考仿真测试卷(一)
5 . 由A、B、C、D四种金属按表中装置图进行实验。
根据实验现象回答下列问题:
(1)装置甲中作正极的是_______ (填“A”或“B”)。
(2)装置乙溶液中C电极反应:_______ ;外电路中电子由_______ (填“C极向B极移动”或“B极向C极移动”)。
(3)装置丙中金属A上电极反应属于_______ (填“氧化反应”或“还原反应”)。
(4)四种金属活动性由强到弱的顺序是_______ 。
| 装置 | 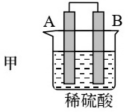 | 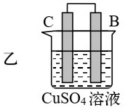 | 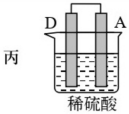 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中作正极的是
(2)装置乙溶液中C电极反应:
(3)装置丙中金属A上电极反应属于
(4)四种金属活动性由强到弱的顺序是
您最近一年使用:0次
名校
解题方法
6 . 把A、B、C、D四种金属按表中装置进行实验。
根据实验现象回答问题:
(1)装置乙中正极的电极反应式是___ 。
(2)装置丙中溶液的酸性___ (填“变大”“变小”或“不变”)。
(3)四种金属活泼性由强到弱的顺序是___ 。
| 装置 | 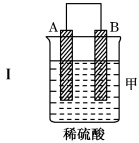 |  | 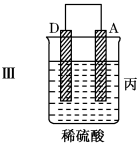 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置乙中正极的电极反应式是
(2)装置丙中溶液的酸性
(3)四种金属活泼性由强到弱的顺序是
您最近一年使用:0次
2021-04-14更新
|
223次组卷
|
3卷引用:浙江省丽水外国语学校高中部2021-2022学年高一下学期第一次阶段性考试(3月)化学试题
解题方法
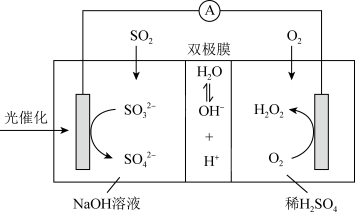
7 . 我国科研人员设计将脱除 的反应与制备
的反应与制备 相结合的协同转化装置如图。在电场作用下,双极膜中间层的
相结合的协同转化装置如图。在电场作用下,双极膜中间层的 解离为
解离为 和
和 ,并向两极迁移。已知:①单独制备
,并向两极迁移。已知:①单独制备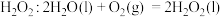 ,不能自发进行;②单独脱除
,不能自发进行;②单独脱除 :
: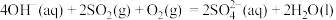 能自发进行。下列说法
能自发进行。下列说法不正确 的是
 的反应与制备
的反应与制备 相结合的协同转化装置如图。在电场作用下,双极膜中间层的
相结合的协同转化装置如图。在电场作用下,双极膜中间层的 解离为
解离为 和
和 ,并向两极迁移。已知:①单独制备
,并向两极迁移。已知:①单独制备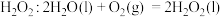 ,不能自发进行;②单独脱除
,不能自发进行;②单独脱除 :
: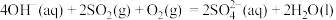 能自发进行。下列说法
能自发进行。下列说法
A.②单独脱除 反应的 反应的 |
B.协同转化工作时, 透过双极膜向左侧移动 透过双极膜向左侧移动 |
C.正极的电极反应式: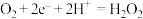 |
D.协同转化总反应: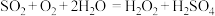 |
您最近一年使用:0次
2013·广东揭阳·三模
解题方法
8 . 某小组利用下列装置进行电化学实验,下列实验操作及预期现象正确的是
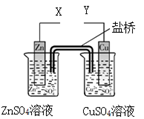

| A.X和Y与电流表连接,电子由Cu极流向Zn极 |
| B.X和Y与电流表连接,将Zn换成Fe测得电流更大 |
| C.X和Y分别与电源“—”、“+”极相连,Cu极质量减轻 |
| D.X和Y分别与电源“—”、“+”极相连,Zn极质量减轻 |
您最近一年使用:0次
9 . 某学习小组设想利用A装置电解制备绿色硝化剂 ,装置如下(c、d为惰性电极)。已知:无水硝酸可在液态
,装置如下(c、d为惰性电极)。已知:无水硝酸可在液态 中发生微弱电离。
中发生微弱电离。
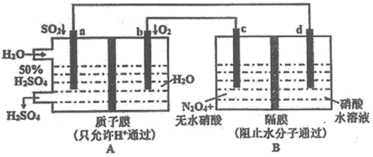
请回答:
(1)a电极名称为_______ 。
(2)写出B装置中生成 的电极反应式
的电极反应式_______ 。
(3) 与水反应生成
与水反应生成 ,
, 作为强氧化剂可氧化大部分金属。3.84g铜粉与100ml一定浓度的硝酸恰好完全反应,收集到2.24L(标准状况下)
作为强氧化剂可氧化大部分金属。3.84g铜粉与100ml一定浓度的硝酸恰好完全反应,收集到2.24L(标准状况下) 与
与 的混合物,则该硝酸物质的量浓度为
的混合物,则该硝酸物质的量浓度为___ 。
 ,装置如下(c、d为惰性电极)。已知:无水硝酸可在液态
,装置如下(c、d为惰性电极)。已知:无水硝酸可在液态 中发生微弱电离。
中发生微弱电离。
请回答:
(1)a电极名称为
(2)写出B装置中生成
 的电极反应式
的电极反应式(3)
 与水反应生成
与水反应生成 ,
, 作为强氧化剂可氧化大部分金属。3.84g铜粉与100ml一定浓度的硝酸恰好完全反应,收集到2.24L(标准状况下)
作为强氧化剂可氧化大部分金属。3.84g铜粉与100ml一定浓度的硝酸恰好完全反应,收集到2.24L(标准状况下) 与
与 的混合物,则该硝酸物质的量浓度为
的混合物,则该硝酸物质的量浓度为
您最近一年使用:0次
解题方法
10 . 某硫酸工厂运用电化学原理设计了如图所示的装置,实现了用SO2发电的同时制备硫酸。图中电极是含催化剂、多孔吸附性的惰性材料。下列说法正确的是
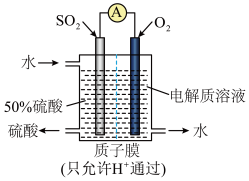

| A.通入SO2气体的一极是负极,发生还原反应 |
| B.正极的电极反应:O2+4e−=2O2− |
| C.该装置工作时的总反应:2SO2+O2+2H2O=2H2SO4 |
| D.氢离子向负极区移动,与负极生成的SO42−结合形成硫酸 |
您最近一年使用:0次



