1 . 利用下列装置和试剂进行实验,能达到实验目的的是
A.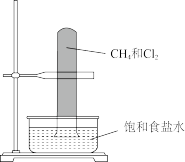 甲烷与氯气暗处发生取代反应 甲烷与氯气暗处发生取代反应 |
B. 比较Zn与Cu的金属性 比较Zn与Cu的金属性 |
C. 蒸干FeCl3溶液,制备无水FeCl3固体 蒸干FeCl3溶液,制备无水FeCl3固体 |
D.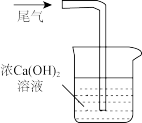 实验室处理尾气SO2 实验室处理尾气SO2 |
您最近一年使用:0次
2022-08-16更新
|
204次组卷
|
2卷引用:四川省广安市邻水县二中2022-2023学年高三上学期10月月考化学试题
名校
解题方法
2 . 请回答下列问题:
(1)铅酸蓄电池是一种可充电电池,其总反应式为Pb+PbO2+2H2SO4 2PbSO4+2H2O,原电池负极的电极反应式为
2PbSO4+2H2O,原电池负极的电极反应式为_______ ,正极附近溶液的pH_______ (填“增大”、“不变”或“减小”)。
(2)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是_______ ,写出正极的电极反应式_______ 。若开始时两极质量相等,当导线中通过0.2mol电子时,两个电极的质量差为_______ 。
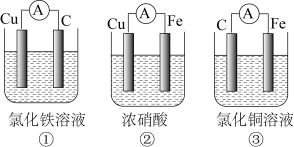
(3)乙醇燃料电池技术方面获得新突破,乙醇(CH3CH2OH)燃料电池的工作原理如图所示。
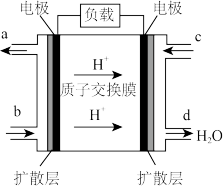
①该电池工作时,c入口处对应的电极为_______ (填“正”或“负”)极,b处入口的物质为_______
②工作一段时间后,当2.3 g乙醇完全反应生成CO2时,外电路中通过的电子数目为_______ 。
(1)铅酸蓄电池是一种可充电电池,其总反应式为Pb+PbO2+2H2SO4
 2PbSO4+2H2O,原电池负极的电极反应式为
2PbSO4+2H2O,原电池负极的电极反应式为(2)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是
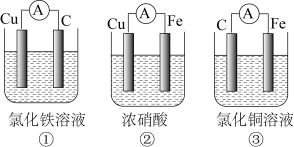
(3)乙醇燃料电池技术方面获得新突破,乙醇(CH3CH2OH)燃料电池的工作原理如图所示。

①该电池工作时,c入口处对应的电极为
②工作一段时间后,当2.3 g乙醇完全反应生成CO2时,外电路中通过的电子数目为
您最近一年使用:0次
2022-11-02更新
|
537次组卷
|
2卷引用:四川省广元中学2022-2023学年高一下学期5月期中考试化学试题
3 . 应用电化学原理,回答下列问题:
(1)上述三个装置中,负极反应的共同特点是_____________________ 。
(2)甲电池工作时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是________________ 。
(3)乙中正极反应式为____________________ ;若将H2换成CH4,则负极反应式为______________________ 。
(4)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池______ 极相连接。
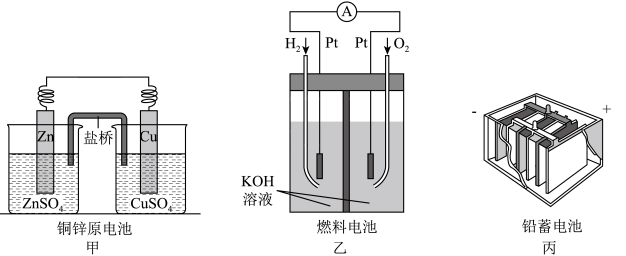
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。按右图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:
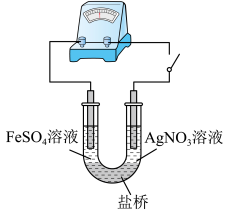
a.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
b.随后向U型管左侧逐渐加入浓Fe2(SO4)3溶液,发现电流计指针的变化依次为:偏移减小→回到零点→逆向偏移。
① 实验a中银作_________ 极。
② 综合实验a和b的现象,得出Ag+和Fe2+反应的离子方程式是_____________________ 。

(1)上述三个装置中,负极反应的共同特点是
(2)甲电池工作时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是
(3)乙中正极反应式为
(4)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。按右图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:

a.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
b.随后向U型管左侧逐渐加入浓Fe2(SO4)3溶液,发现电流计指针的变化依次为:偏移减小→回到零点→逆向偏移。
① 实验a中银作
② 综合实验a和b的现象,得出Ag+和Fe2+反应的离子方程式是
您最近一年使用:0次
名校
解题方法
4 . 有X、Y、Z、M四种金属,按如下装置进行实验,实验现象如表中。
下列说法不正确的是
| 装置 | 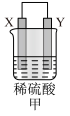 |  | 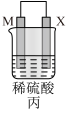 |
| 现象 | 金属X不断溶解 | Z的质量增加 | X上有气体产生 |
| A.装置甲中电子从X极流出,经外电路流入Y极 |
B.装置乙的正极反应式为: |
| C.装置丙溶液中阳离子往M极移动 |
| D.四种金属活动性由强到弱的顺序是:M>X>Y>Z |
您最近一年使用:0次
2023-07-05更新
|
147次组卷
|
2卷引用:四川省眉山市2022-2023学年高一下学期期末考试化学试题
名校
解题方法
5 . 2021年6月24日,《一种硫酸铜废液制备高纯氧化铜》获得第22届中国专利优秀奖,其工艺流程如图:
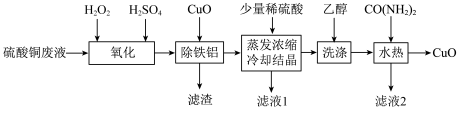
已知:①硫酸铜废液中的杂质离子仅含Na+、Fe2+、Fe3+、Al3+等。
②25℃时的溶度积:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.25×10-33。
回答下列问题:
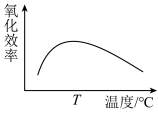
(1)双氧水能把Fe2+氧化为Fe3+,写出反应的离子方程式________ ;如图是双氧水的氧化效率随温度变化的曲线,请解释氧化效率变化的原因________ 。
(2)“除铁铝”时,为使Fe3+和Al3+沉淀完全(溶液中剩余离子的浓度小于1×10-5mol•L-1),需加入CuO调节溶液pH至______ (lg2=0.3)。
(3)“洗涤”目的是为了除去硫酸铜晶体表面沾附的少量杂质,杂质的化学式为______ ,洗涤所需要的玻璃仪器有______ ,判断晶体洗涤干净的实验操作是________ 。
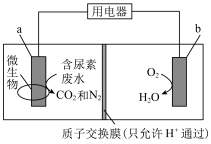
(4)如图装置可在净化含尿素[CO(NH2)2]废水的同时提供电能,以下说法正确的是________ 。

已知:①硫酸铜废液中的杂质离子仅含Na+、Fe2+、Fe3+、Al3+等。
②25℃时的溶度积:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.25×10-33。
回答下列问题:
(1)双氧水能把Fe2+氧化为Fe3+,写出反应的离子方程式

(2)“除铁铝”时,为使Fe3+和Al3+沉淀完全(溶液中剩余离子的浓度小于1×10-5mol•L-1),需加入CuO调节溶液pH至
(3)“洗涤”目的是为了除去硫酸铜晶体表面沾附的少量杂质,杂质的化学式为
(4)如图装置可在净化含尿素[CO(NH2)2]废水的同时提供电能,以下说法正确的是

| A.温度越高,反应速率越快,装置的转化率越高 |
| B.该装置工作时,b为正极,发生还原反应 |
C.装置内溶液电流的方向由 到 到 ,电子的流向与之相反 ,电子的流向与之相反 |
| D.工作一段时间后,正极区域pH会显著升高 |
您最近一年使用:0次
6 . 工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电板上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是
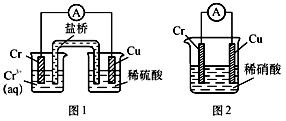

| A.图1为原电池装置,盐桥中的阴离子移向Cu电极的烧杯中 |
| B.由实验现象可知:金属活动性Cu>Cr |
| C.图2装置中Cu电极上发生的电极反应式为:Cu-2e-=Cu2+ |
| D.两个装置中,电子均由Cr电极流向Cu电极 |
您最近一年使用:0次
2018-04-10更新
|
239次组卷
|
2卷引用:四川省宜宾市第四中学校2019-2020学年高二下学期第四学月考试化学试题
名校
7 . 浓差电池是一种利用电解质溶液浓度差产生电势差而形成的电池,理论上当电解质溶液的浓度相等时停止放电。图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电池为电源完成电渗析法制备磷酸二氢钠。下列说法正确的是
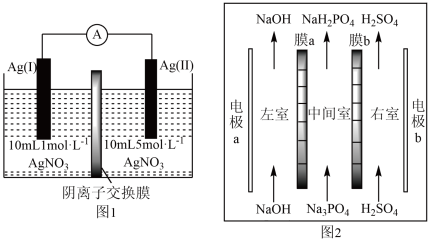
| A.电极Ag(II)的电极反应式为:Ag-e-=Ag+ |
| B.电渗析装置中膜a、b均为阳离子交换膜 |
| C.电渗析过程中左室中NaOH浓度增大,右室H2SO4的浓度减小 |
| D.电池从开始到停止放电,理论上可制备2.4gNaH2PO4 |
您最近一年使用:0次
名校
8 . 浓差电池是一种利用电解质溶液浓度差产生电势差而形成的电池,理论上当电解质溶液的浓度相等时停止放电。图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电池为电源完成电渗析法制备磷酸二氢钠。下列说法错误的是
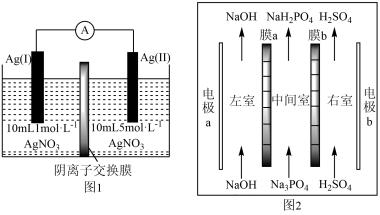

| A.电极a应与Ag(I)相连 |
| B.电渗析装置中膜a为阳离子交换膜 |
C.电渗析过程中左、右室中NaOH和 的浓度均增大 的浓度均增大 |
D.电池从开始到停止放电,理论上可制备2.4g |
您最近一年使用:0次
2024-01-13更新
|
628次组卷
|
4卷引用: 四川省成都市第七中学2023-2024学年高三上学期期末考试理科综合试卷-高中化学
四川省成都市第七中学2023-2024学年高三上学期期末考试理科综合试卷-高中化学陕西省渭南市2023-2024学年高三上学期教学质量检测化学试卷 陕西省渭南市2023-2024学年高三教学质量检测(Ⅰ)化学试题(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
名校
9 . 按要求回答问题:
(1)由SiO2制备高纯度硅的工业流程如图所示:
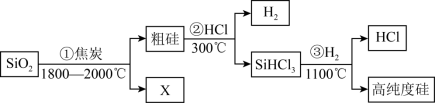
①写出SiO2转化为Si(粗)的化学方程式:____________________________________________ 。
②可以循环使用的物质为_________________________ 。
(2)为了有效实现NO和NO2的相互转化,设计如图实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。
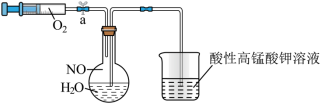
①打开止水夹,推动针筒活塞,使氧气进入烧瓶,首先观察到烧瓶中的现象是____________ ,产生此现象的化学方程式为______________________________________________ 。
②关上止水夹,轻轻摇动烧瓶,写出发生的化学方程式________________________________ 。
(3)以 Fe 和 Cu 为电极,稀 H2SO4 为电解质溶液形成的原电池中:
①H+向________ 极移动(填“正”或“负”)。
②若有 1 mol e- 流过导线,则理论上负极质量减少________ g。
③若将稀硫酸换成浓硝酸,正极电极方程式为:______________________ 。
(1)由SiO2制备高纯度硅的工业流程如图所示:

①写出SiO2转化为Si(粗)的化学方程式:
②可以循环使用的物质为
(2)为了有效实现NO和NO2的相互转化,设计如图实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。

①打开止水夹,推动针筒活塞,使氧气进入烧瓶,首先观察到烧瓶中的现象是
②关上止水夹,轻轻摇动烧瓶,写出发生的化学方程式
(3)以 Fe 和 Cu 为电极,稀 H2SO4 为电解质溶液形成的原电池中:
①H+向
②若有 1 mol e- 流过导线,则理论上负极质量减少
③若将稀硫酸换成浓硝酸,正极电极方程式为:
您最近一年使用:0次
2023-05-18更新
|
318次组卷
|
2卷引用:四川省宜宾市第四中学校2022-2023学年高二下学期6月期末化学试题
名校
解题方法
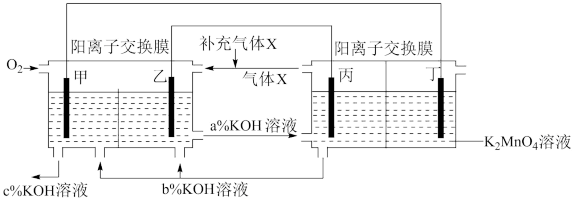
10 . 一种将燃料电池与电解池组合制备 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
| A.甲为正极,丙为阴极 |
B.丁极的电极反应式为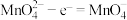 |
C.KOH溶液的质量分数: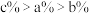 |
D.标准状况下,乙电极上每消耗 气体时,理论上有 气体时,理论上有 移入阴极区 移入阴极区 |
您最近一年使用:0次
2022-05-29更新
|
665次组卷
|
7卷引用:四川省泸州市泸县第五中学2021-2022学年高三下学期二诊模拟考试理综化学试题
四川省泸州市泸县第五中学2021-2022学年高三下学期二诊模拟考试理综化学试题重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题(已下线)课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省株洲市第一中学2022届高三下学期第三次模拟考试化学试题河南省南阳市第一中学校2022-2023学年高三上学期12月月考化学试题



