名校
1 . 填空。
(1)请你写出以强酸溶液为电解质溶液的甲烷燃料电池的负极的电极反应式_______ 。若线路中转移2mol电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L。请你写出铅蓄电池的正极的电极反应式_______ 。
(2)已知2Fe3++Cu=2Fe2++Cu2+,利用这一反应,试设计一个原电池,画出示意图,标明电极材料名称,电解质溶液_______ 。在该电池中,正极是_______ ,电极反应式_______ 。
(1)请你写出以强酸溶液为电解质溶液的甲烷燃料电池的负极的电极反应式
 在标准状况下的体积为
在标准状况下的体积为(2)已知2Fe3++Cu=2Fe2++Cu2+,利用这一反应,试设计一个原电池,画出示意图,标明电极材料名称,电解质溶液
您最近一年使用:0次
名校
解题方法
2 . 近日“宁德时代”宣布2023年实现钠离子电池产业化,钠离子电池以其低成本、高安全性及其优异电化学属性等成为锂离子电池的首选“备胎”,其充放电过程是 在正负极间的镶嵌与脱嵌。下列说法
在正负极间的镶嵌与脱嵌。下列说法不正确 的是
 在正负极间的镶嵌与脱嵌。下列说法
在正负极间的镶嵌与脱嵌。下列说法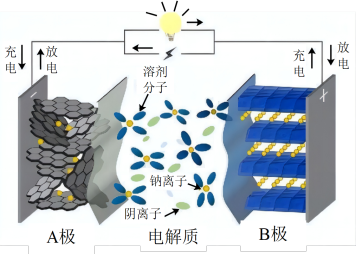
| A.放电时负极区钠单质失去电子 |
B.充电时 由“B极”向“A极”移动 由“B极”向“A极”移动 |
| C.由于未使用稀缺的锂钴元素,量产后该电池生产成本比锂离子电池低 |
D.该电池一种正极材料为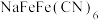 ,充电时的电极反应为: ,充电时的电极反应为: |
您最近一年使用:0次
2022-08-08更新
|
2705次组卷
|
11卷引用:广东省六校2023届高三第一次联考化学试题
广东省六校2023届高三第一次联考化学试题广东省广州市六校2023届高三上学期8月第一次联考化学试题广东省深圳市新安中学2022-2023学年高三上学期周末测试(2022.9.25)化学试题福建省三明第一中学2022-2023学年高三上学期第二次月考化学试题(已下线)热点情景汇编-专题八 化学反应中的电能(已下线)2023年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷B新疆维吾尔自治区阿克苏地区第二中学2022-2023学年高三上学期第一次月考化学试题(已下线)专题16 新型电化学装置分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)T12-电化学原理(已下线)T10-电化学原理江西省南昌市第十九中学2022-2023学年高三上学期(10月)第三次月考化学试卷
解题方法
3 . 运用原电池原理可研究物质的性质或进行工业生产。
(1)某兴趣小组设计图装置用锌、铜作电极材料,硫酸铜溶液为电解质溶液的进行原电池实验。负极材料是____ (填“锌”或“铜”);当正极质量增加12.8g时,转移了____ mol电子。

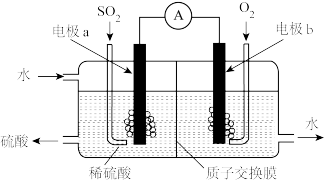
(2)如图所示,运用原电池原理可将SO2转化成硫酸。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。a是____ 极(填“正”或“负”),b电极反应式为____ ,生产过程中H+向____ (填“a”或“b”)电极区域运动。
(1)某兴趣小组设计图装置用锌、铜作电极材料,硫酸铜溶液为电解质溶液的进行原电池实验。负极材料是

(2)如图所示,运用原电池原理可将SO2转化成硫酸。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。a是

您最近一年使用:0次
解题方法
4 . 无论是在环境保护领域还是在工农业生产领域,氮及其化合物一直是我国科研重点。回答下列问题:
(1)下列过程属于氮的固定过程的是_______(填选项字母)。
(2)消除汽车尾气中的氮氧化合物的原理之一为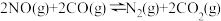 。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
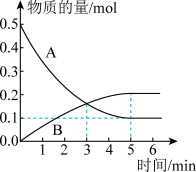
①其中B表示_______ (填“ ”或“
”或“ ”)物质的量的变化曲线。
”)物质的量的变化曲线。
②该温度下,反应开始至5min时该反应的平均反应速率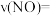
_______ 。
③3min时,反应_______ (填“达到”或“未达到”)化学平衡,6min时,正反应速率_______ (填“>”“<”或“=”)逆反应速率。
④下列情况能说明该反应达到平衡状态的是_______ (填选项字母)。
A.化学反应速率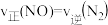
B.CO与 的物质的量之和不再发生变化
的物质的量之和不再发生变化
C.容器内气体压强不再发生变化
D.容器内混合气体密度不再发生变化
(3)实验室用NaOH溶液对氮氧化合物进行尾气吸收,例如NaOH溶液可将 转化为
转化为 和
和 。该吸收过程中发生反应的离子方程式为
。该吸收过程中发生反应的离子方程式为_______ 。
(4)某固体氧化物为电解质的新型燃料电池是以液态肼(N2H4)为燃料,氧气为氧化剂构成,其原理示意图如图所示。
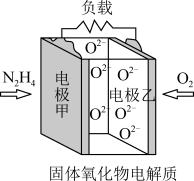
该电池的正极为_______ (填“电极甲”或“电极乙”,下同);电池工作时, 向
向_______ 移动。
(1)下列过程属于氮的固定过程的是_______(填选项字母)。
| A.工业合成氨 |
| B.工业利用氨气合成硝酸 |
| C.雷雨天中氮气与氧气生成氮氧化合物 |
| D.通过碱性试剂将气态的氮氧化合物转化为固态含氮化合物 |
 。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
。一定温度下,向体积为5L的刚性密闭容器中充入0.5molNO和0.5molCO,发生上述反应,测得部分气体的物质的量随时间变化关系如图所示:
①其中B表示
 ”或“
”或“ ”)物质的量的变化曲线。
”)物质的量的变化曲线。②该温度下,反应开始至5min时该反应的平均反应速率
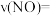
③3min时,反应
④下列情况能说明该反应达到平衡状态的是
A.化学反应速率
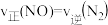
B.CO与
 的物质的量之和不再发生变化
的物质的量之和不再发生变化C.容器内气体压强不再发生变化
D.容器内混合气体密度不再发生变化
(3)实验室用NaOH溶液对氮氧化合物进行尾气吸收,例如NaOH溶液可将
 转化为
转化为 和
和 。该吸收过程中发生反应的离子方程式为
。该吸收过程中发生反应的离子方程式为(4)某固体氧化物为电解质的新型燃料电池是以液态肼(N2H4)为燃料,氧气为氧化剂构成,其原理示意图如图所示。

该电池的正极为
 向
向
您最近一年使用:0次
名校
解题方法
5 . 锌锰干电池的内部构造示意图如图。下列有关描述中正确的是
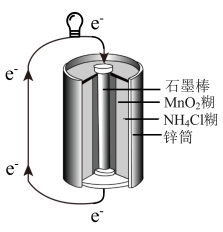

| A.该电池属于二次电池 |
B.电池工作时,电子从正极经 糊流向负极 糊流向负极 |
C.石墨棒作正极, 在正极发生还原反应 在正极发生还原反应 |
D.锌筒作负极,电极反应式为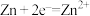 |
您最近一年使用:0次
2022-07-10更新
|
304次组卷
|
3卷引用:广东省深圳市观澜中学2022-2023学年高一下学期3月月考化学试题
6 . 某研究小组设计一种“人体电池”实验装置(如图),进行如下实验。

实验1:一位同学的左手触摸锌片,右手分别触摸铝片、铁片、锡片、铜片;
实验2:两位同学手牵手,一位同学的左手触摸锌片,另一位同学的右手分别触摸铝片、铁片、锡片、铜片。
记录灵敏电流表的读数及指针偏转方向,数据见下表。下列说法正确的是

实验1:一位同学的左手触摸锌片,右手分别触摸铝片、铁片、锡片、铜片;
实验2:两位同学手牵手,一位同学的左手触摸锌片,另一位同学的右手分别触摸铝片、铁片、锡片、铜片。
记录灵敏电流表的读数及指针偏转方向,数据见下表。下列说法正确的是
| 实验时灵敏电流表的读数(微安) | ||||
| 锌-铝 | 锌-铁 | 锌-锡 | 锌-铜 | |
| 实验1 |  | 11 | 17 | a |
| 实验2 |  | 7 | 9 | b |
| A.该人体电池中,锌片作负极,其他金属片均作正极 |
| B.当两手分别触碰锌和铁时,铁片上发生氧化反应 |
| C.实验2的电流均比实验1对应的小,是因为电路中的电阻较大 |
| D.由表格中数据可推测:a<17 |
您最近一年使用:0次
2022-07-06更新
|
322次组卷
|
2卷引用:广东省佛山市普通高中2021-2022学年高一下学期教学质量检测化学试题
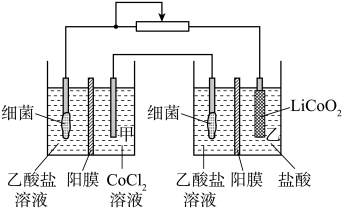
7 . 设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成 ,将废旧锂离子电池的正极材料
,将废旧锂离子电池的正极材料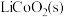 转化为
转化为 ,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
 ,将废旧锂离子电池的正极材料
,将废旧锂离子电池的正极材料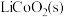 转化为
转化为 ,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
| A.装置工作时,甲室溶液pH逐渐增大 |
| B.装置工作一段时间后,乙室应补充盐酸 |
C.乙室电极反应式为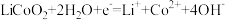 |
D.若甲室 减少 减少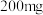 ,乙室 ,乙室 增加 增加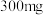 ,则此时已进行过溶液转移 ,则此时已进行过溶液转移 |
您最近一年使用:0次
2022-06-23更新
|
11052次组卷
|
24卷引用:广东省汕头市金山中学2022-2023学年高三上学期第二次月考化学试题
广东省汕头市金山中学2022-2023学年高三上学期第二次月考化学试题2022年新高考山东化学高考真题(已下线)专题08 电化学及其应用-2022年高考真题模拟题分项汇编(已下线)2022年山东省高考真题变式题(不定项选择题)(已下线)考点18 原电池 化学电源-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第34练 原电池-2023年高考化学一轮复习小题多维练(全国通用)(已下线)专题讲座(六) 电解质介质和隔膜在电化学的作用(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第17讲 电解池 金属的腐蚀与防护 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题05 化学能与电能的转化(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题16 新型电化学装置分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题五 锂电池和锂离子电池(练习)(已下线)专题八 电化学的相关计算(练习)(已下线)专题卷15 电解原理在工农业生产中的应用-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点07 重温“两池”原理-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)查补易混易错04 化学反应原理部分-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)专题九 电化学装置图(练)(已下线)专题07 电化学及其应用-2023年高考化学真题题源解密(新高考专用)(已下线)专题10 电化学及其应用-2023年高考化学真题题源解密(全国通用)(已下线)考点18 原电池 化学电源(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)第四章 化学反应与电能 第二节 电解池 第1课时 电解原理山东省枣庄市第八中学2023-2024学年高二上学期10月月考化学试题(已下线)考点3 电解池 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)江苏省苏州实验中学科技城校2023-2024学年高二上学期10月月考化学试题(已下线)题型11 新型电化学装置分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
8 . 一种水性电解液Zn-MnO2离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH) 存在)。电池放电时,下列叙述错误的是
存在)。电池放电时,下列叙述错误的是
 存在)。电池放电时,下列叙述错误的是
存在)。电池放电时,下列叙述错误的是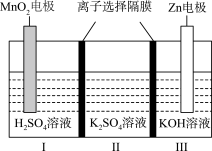
| A.Ⅱ区的K+通过隔膜向Ⅲ区迁移 |
B.Ⅰ区的SO 通过隔膜向Ⅱ区迁移 通过隔膜向Ⅱ区迁移 |
| C. MnO2电极反应:MnO2+2e-+4H+=Mn2++2H2O |
D.电池总反应:Zn+4OH-+MnO2+4H+=Zn(OH) +Mn2++2H2O +Mn2++2H2O |
您最近一年使用:0次
2022-06-08更新
|
25841次组卷
|
47卷引用:广东省东莞实验中学2022-2023学年高三上学期第一次月考化学试题
广东省东莞实验中学2022-2023学年高三上学期第一次月考化学试题2022年高考全国甲卷化学真题(已下线)专题08电化学及其应用-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题08电化学及其应用-2022年高考真题+模拟题汇编(全国卷)(已下线)专题08电化学及其应用-五年(2018~2022)高考真题汇编(全国卷)(已下线)2022年全国甲卷高考真题变式题(选择题)(已下线)第08练 以新型化学电源及电极反应式的书写突破原电池原理-2022年【暑假分层作业】高二化学(2023届一轮复习通用)浙江省绍兴市2021-2022学年高二下学期期末考试化学试题(已下线)考点18 原电池 化学电源-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题09 电化学基础-备战2023年高考化学母题题源解密(全国通用)(已下线)第34练 原电池-2023年高考化学一轮复习小题多维练(全国通用)陕西省西安市长安区第一中学2021-2022学年高二下学期期末考试化学试题(已下线)第18讲 原电池 化学电源(练)-2023年高考化学一轮复习讲练测(全国通用)四川省遂宁市射洪中学2022-2023学年高二上学期入学考试化学试题(已下线)第16讲 原电池 新型电源 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)山东省威海乳山市银滩高级中学2022-2023学年高二9月月考化学试题江苏省扬州市江都区邵伯高级中学2022-2023学年高二10月阶段性测试化学(选修)试题(已下线)易错点19 电化学基础-备战2023年高考化学考试易错题河南省濮阳市南乐县第一高级中学2022-2023学年高三上学期9月月考化学试题(已下线)热点情景汇编-专题八 化学反应中的电能(已下线)专题05 化学能与电能的转化(讲)-2023年高考化学二轮复习讲练测(新高考专用)北京市清华大学附属中学2022-2023学年高三上学期12月统练六化学试题(已下线)专题16 新型电化学装置分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 题型专攻2 电化学离子交换膜的分析与应用(已下线)角度1 一反常规(已下线)题型21 三室膜电解装置及其应用江苏省南京市燕子矶中学2022-2023学年高二下学期开学考试化学试题(已下线)专题一 原电池的工作原理及其应用(练习)(已下线)专题1 新型电池——化学学科发展前沿(已下线)专题卷16 离子隔膜在电化学中的应用-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点07 重温“两池”原理-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)山东省日照市莒县第一中学2022-2023学年高一下学期4月月考化学试题江苏省盐城市阜宁县2022-2023学年高一下学期4月期中考试化学试题(已下线)专题12 电化学的综合应用(已下线)专题12 电化学的综合应用(已下线)第16练 原电池 新型电池 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题10 电化学及其应用-2023年高考化学真题题源解密(全国通用)作业(二十三) 化学电源(已下线)考点18 原电池 化学电源(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第24讲原电池与化学电源河北省保定市唐县第一中学2022-2023学年高三上学期11月期中化学试题黑龙江省哈尔滨市第三中学2023-2024学年高二上学期开学测试化学试题四川省江油中学2023-2024学年高三上学期9月月考理科综合化学试题(已下线)题型02 电化学图像分析-2024年高考化学答题技巧与模板构建黑龙江省哈尔滨师范大学附属中学2023-2024学年高二上学期11月期中化学试题云南省宣威市第九中学2023-2024学年高三下学期入学考试理综试题-高中化学云南省大理白族自治州祥云祥华中学2023-2024学年高一下学期3月月考化学试题
解题方法
9 . 2021年,天津大学杨全红教授团队和上海师范大学万颖教授团队合作,设计了具有选择性催化作用的In基催化剂(In-based catalyst),为提高电池循环稳定性提供了新的策略。实验研究和计算模拟表明,在Li-S电池放电过程中,该催化剂降低了硫单质向可溶性Li2Sn的转化速率:更重要的是反应过程中生成的LiInS2可以提高可溶性Li2Sn向不溶放电产物Li2S的转化速率。其工作原理如图所示,电池总反应为: 16Li+xS8 =8Li2S。下列说法错误的是
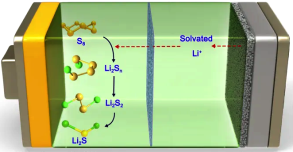

| A.电池工作时,正极可发生反应:Li2Sn+(2n- 2)Li++(2n-2)e-= nLi2S |
| B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14g |
| C.正极材料S8中掺入少量石墨烯,其作用主要是提高电极的导电性 |
| D.LiInS2为该电池的催化剂 |
您最近一年使用:0次
名校
10 . 阅读题目,回答问题:
(1)FeCl3常用于腐蚀印刷电路铜板,反应过程的离子方程式为____ ,若将此反应设计成原电池,请写出该原电池负极电极反应为____ ,正极电极反应为____ 。
(2)为探究FeCl3在H2O2制取O2反应中的作用,某兴趣小组进行下列实验:向试管中加入5mL11mol·L-1H2O2溶液,静置几分钟,无明显现象;滴加2滴1mol·L-1FeCl3溶液,立即产生大量气泡。(已知H2O2不与Cl-反应)
①加FeCl3溶液反应20min后,H2O2的浓度变为10.5mol·L-1,则20min内H2O2的平均反应速率为_____ 。
②反应结束后,滴加KSCN溶液,试管中溶液呈红色。经测定,溶液中Fe3+的量没有变化。综合以实验,可推断出:在H2O2制O2反应中,FeCl3作____ 剂。
(3)H2O2是实验室常见的强氧化剂,在医疗上可用作消毒剂等。某兴趣小组为探究外界条件对H2O2分解反应速率的影响,设计如表所示实验。
填写表中空白内容:II____ ,III____ ,IV____ 。
(4)如图装置可以把氢气中蕴含的化学能转化为电能,被称为氢氧燃料电池。

①该电池的正极是电极____ (填“a”或“b”),负极发生反应的方程式为____ 。
②电池工作时,溶液中的K+会向____ 区移动(填“正极”或“负极”),当外电路中转移1mol电子时,消耗的O2在标准状况下体积为____ 。
(1)FeCl3常用于腐蚀印刷电路铜板,反应过程的离子方程式为
(2)为探究FeCl3在H2O2制取O2反应中的作用,某兴趣小组进行下列实验:向试管中加入5mL11mol·L-1H2O2溶液,静置几分钟,无明显现象;滴加2滴1mol·L-1FeCl3溶液,立即产生大量气泡。(已知H2O2不与Cl-反应)
①加FeCl3溶液反应20min后,H2O2的浓度变为10.5mol·L-1,则20min内H2O2的平均反应速率为
②反应结束后,滴加KSCN溶液,试管中溶液呈红色。经测定,溶液中Fe3+的量没有变化。综合以实验,可推断出:在H2O2制O2反应中,FeCl3作
(3)H2O2是实验室常见的强氧化剂,在医疗上可用作消毒剂等。某兴趣小组为探究外界条件对H2O2分解反应速率的影响,设计如表所示实验。
| 试管编号 | 实验目的 | H2O2溶液 | 温度 | 水的体积/mL | FeCl3溶液体积/mL | |
| 质量分数 | 体积/mL | |||||
| I | 为编号II实验的参照 | 12% | 5.0 | 常温 | 0 | 0 |
| II | 温度对反应速率的影响 | —— | 5.0 | 60℃ | 0 | 0 |
| III | 为编号IV实验的参照 | 4.0% | 5.0 | 常温 | —— | 0 |
| IV | —— | 4.0% | 5.0 | 常温 | 0 | 1.0 |
填写表中空白内容:II
(4)如图装置可以把氢气中蕴含的化学能转化为电能,被称为氢氧燃料电池。

①该电池的正极是电极
②电池工作时,溶液中的K+会向
您最近一年使用:0次



