1 . 【化学选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大,其中非金属元素A的基态原子中成对电子数是未成时电子数的两倍,C元素在地壳中含量最高,D的单质是短周期中熔点最低的金属,E的合金是我国使用最早的合金。
(1)E元素的基态原子电子排布式为__________________ 。
(2)A的某种氢化物A2H2分子中含有___ 个σ键和____ 个π键。
(3)A 的含氧酸根离子AO3n-的空间构型是___________ 。
(4)B的最简单的氢化物的沸点比A 的最简单的氢化物的沸点高得多,其原因是_____ 。
(5)E的最高价氧化物对应的水化物溶解于氨水中生成的复杂化合物的化学式是______ 。
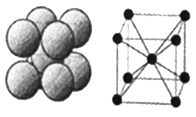
(6)下图是D单质的晶体堆积方式,这种堆积方式的晶胞中原子的配位数为____ ,若该原子的半径为rpm ,此晶体的密度ρ=______ g/cm3(用含r的代数式表示,阿伏伽德罗常数用NA表示)。
(1)E元素的基态原子电子排布式为
(2)A的某种氢化物A2H2分子中含有
(3)A 的含氧酸根离子AO3n-的空间构型是
(4)B的最简单的氢化物的沸点比A 的最简单的氢化物的沸点高得多,其原因是
(5)E的最高价氧化物对应的水化物溶解于氨水中生成的复杂化合物的化学式是
(6)下图是D单质的晶体堆积方式,这种堆积方式的晶胞中原子的配位数为

您最近一年使用:0次
2017-02-24更新
|
855次组卷
|
4卷引用:云南省红河州弥勒市中小学2018-2019学年高二下学期期末考试化学试题
2 . 砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________ 。
(2)根据元素周期律,原子半径Ga_____________ As,第一电离能Ga____________ As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________ ,其中As的杂化轨道类型为_________ 。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是__________ 。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________ ,Ga与As以________ 键键合。Ga和As的摩尔质量分别为MGag·mol-1和MAs g·mol-1,原子半径分别为rGapm和rAspm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________ 。

(1)写出基态As原子的核外电子排布式
(2)根据元素周期律,原子半径Ga
(3)AsCl3分子的立体构型为
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为

您最近一年使用:0次
2016-12-09更新
|
3902次组卷
|
21卷引用:2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷
2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷2016年全国普通高等学校招生统一考试化学(新课标3卷精编版)2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷四川省眉山中学2016-2017学年高二下学期期中考试理综化学试题新疆生产建设兵团第二中学2016-2017学年高二下学期第二次月考化学试题四川省绵阳中学实验学校2017届高三5月模拟理综化学试题河南省南阳市第一中学2018届高三实验班第一次考试化学试题贵州省遵义航天高级中学2018届高三第二次模拟(10月)理科综合化学试题吉林省实验中学2018高三一模理综化学试题【全国百强校】内蒙古集宁一中(东校区)2017-2018学年高二下学期期中考试化学试题【全国校级联考】四川省眉山一中办学共同体2019届高三9月月考化学试题吉林省实验中学2018届高三上学期第五次月考(一模)理科综合化学试题【全国百强校】四川省棠湖中学2019届高三上学期第三次月考理综-化学试题【全国百强校】江西省南昌市第十中学2019届高三上学期期末考试理科综合化学试题2016年全国普通高等学校招生统一考试化学(全国3卷参考版)2020届高中化学第一轮复习第十二章《物质结构与性质》测试卷湖北省武汉市华中师范大学第一附属中学2020届高三2月份网络教学质量监测理综化学试题广西壮族自治区田阳高中2019-2020学年高二下学期6月月考理科综合化学试题福建省永安市第三中学2021届高三9月月考化学试题广西河池市高级中学2021-2022学年高三上学期第三次月考化学试题湖南省郴州市永兴县第一中学2021-2022学年高三下学期期中考试化学试题
3 . 已知A、B、C、D四种短周期元素,它们的核电荷数依次增大。A、C原子的L能层中都有两个未成对的电子,C、D同主族。E、F都是第四周期元素,E原子核外有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态E原子中,电子占据的最高能层符号为_______ ,该能层具有的原子轨道数为_______ 。
(2)E3+离子的价层电子排布式为______________ 。
(3)DCl2中D原子采取的轨道杂化方式为_________________________ ,C元素的气态氢化物的VSEPR模型名称为____________________________ 。
(4)写出一个与DAB-离子互为等电子体的合理分子式:__________________________ 。
(5)利用E(AB)63-检验E2+的离子方程式为_________________________ 。
(6)已知F的晶体结构为面心立方,F的原子直径d= 0.256nm,求1cm3 F中,含有F原子的个数约为_______________ 个。(保留3位有效数字)
(1)基态E原子中,电子占据的最高能层符号为
(2)E3+离子的价层电子排布式为
(3)DCl2中D原子采取的轨道杂化方式为
(4)写出一个与DAB-离子互为等电子体的合理分子式:
(5)利用E(AB)63-检验E2+的离子方程式为
(6)已知F的晶体结构为面心立方,F的原子直径d= 0.256nm,求1cm3 F中,含有F原子的个数约为
您最近一年使用:0次
名校
4 . 利用电负性数值可以预测
| A.分子的极性 | B.分子的对称性 |
| C.分子的空间构型 | D.化学键的极性 |
您最近一年使用:0次
2016-12-09更新
|
180次组卷
|
5卷引用:云南省玉溪市华宁二中2018-2019学年9月份考试高二化学试题
5 . 在以下性质的比较中,正确的是
| A.微粒半径:O2-<F-<Na+<Li+ | B.第一电离能:He<Ne<Ar |
| C.分子中的键角:CH4>H2O>CO2 | D.共价键的键能:C-C<C=C<C≡C |
您最近一年使用:0次
2016-12-09更新
|
678次组卷
|
6卷引用:云南省楚雄彝族自治州民族中学2021-2022学年高二下学期3月月考化学试题
云南省楚雄彝族自治州民族中学2021-2022学年高二下学期3月月考化学试题2014-2015湖北省黄石市有色第一中学高二下学期期中考试化学试卷(人教版2019)选择性必修2 第二章 分子结构与性质 第一节 共价键天津耀华中学2021-2022学年高二下学期期末考试化学试题(已下线)专题14 分子结构与性质-2023年高考化学一轮复习小题多维练(全国通用)(已下线)综合01 物质结构与性质压轴80题-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(天津专用)
2014高三·全国·专题练习
名校
解题方法
6 . 某元素的最外层电子数为2,价电子数为5,并且是同族中原子序数最小的元素,关于该元素的判断错误的是( )
| A.电子排布式为1s22s22p63s23p63d34s2 |
| B.该元素为V |
| C.该元素为ⅡA族元素 |
| D.该元素位于d区 |
您最近一年使用:0次
2016-12-09更新
|
1331次组卷
|
15卷引用:云南省元江哈尼族彝族傣族自治县一中2018-2019学年高二上学期12月考试化学试题
云南省元江哈尼族彝族傣族自治县一中2018-2019学年高二上学期12月考试化学试题云南省盐津县第一中学2018-2019学年高二上学期12月份考试化学试题云南省玉溪市民族中学2021-2022学年高二上学期期末考试化学试题(已下线)2014届高考化学三轮复习排查 专题14物质结构与性质选修3练习卷河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:1.2 原子结构与元素的性质 第1课时山东省济宁市实验中学2018-2019学年高二上学期第二次月考化学试题吉林省松原市扶余市第一中学2018-2019学年高二上学期期末考试化学试题内蒙古自治区第一机械制造(集团)有限公司第一中学2018-2019学年高二下学期期中考试化学试题【全国百强校】天津市静海区第一中学2018-2019学年高二下学期5月月考化学试题黑龙江省鸡西市鸡东县第二中学2018-2019学年高二5月月考化学试题新疆乌鲁木齐市第四中学2018-2019学年高二下学期期末考试化学试题河北省衡水市桃城区第十四中学2019-2020学年高二下学期摸底考试化学试题福建省福州高级中学2020-2021学年高二下学期期中考试化学试题福建省福州教育学院附属中学2021-2022学年高二下学期3月月考化学试题福建省建瓯市芝华中学2023-2024学年高二下学期第一次阶段考试化学试题
7 . A~G是前四周期除稀有气体之外原子序数依次增大的七种元素。A与其他元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答下列问题:
(1)写出元素名称:B_______ ,G_______ 。
(2)写出F的价电子排布图:_______ 。
(3)写出化合物BC的结构式:__________________ 。
(4)由A、C、F三元素形成的离子[F(CA)4]— 是F在水溶液中的一种存在形式,其中F的杂化类型是________________ 。
(5)在测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的主要原因是______________________ 。
(6)E的一种晶体结构如图甲,则其一个晶胞中含有_______ 个E;G与D形成的化合物的晶胞结构如图乙,若晶体密度为ag/cm3,则G与D最近的距离为____ pm
(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;乙中○为G,●为D。)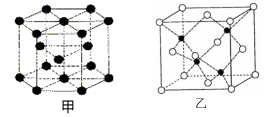
(1)写出元素名称:B
(2)写出F的价电子排布图:
(3)写出化合物BC的结构式:
(4)由A、C、F三元素形成的离子[F(CA)4]— 是F在水溶液中的一种存在形式,其中F的杂化类型是
(5)在测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的主要原因是
(6)E的一种晶体结构如图甲,则其一个晶胞中含有
(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;乙中○为G,●为D。)

您最近一年使用:0次
2016-12-09更新
|
888次组卷
|
5卷引用:云南省元阳县第一中学2020届高三上学期开学考试化学试题
云南省元阳县第一中学2020届高三上学期开学考试化学试题云南省凤庆县一中2020届高三上学期开学考试理综化学试题(已下线)2014届吉林省吉林市高三下学期第二次模拟考试理综化学试卷(已下线)2013-2014湖南省怀化市高三第三次模拟考试理综化学试卷贵州省平塘县民族中学2020届高三上学期开学考试(理综)化学试题
2014·全国·一模
名校
解题方法
8 . A、B、C、D、E、F六种元素的原子序数依次增大。A的最高正价和最低负价的绝对值相等。B的基态原子有3个不同的能级且各能级中电子数相等。D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子的s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍。请回答下列问题:
(1)F的基态原子价电子排布式为_______ 。
(2)B、C、D、E的原子的第一电离能由小到大的顺序为___ 。(用元素符号回答)
(3)下列关于B2A2分子和A2D2分子的说法正确的是________
A.分子中都含有σ键和π键
B.中心原子都sp杂化
C.都是含极性键和非极性键的非极性分子
D.互为等电子体
E.B2A2分子的沸点明显低于A2D2分子
(4)F2+能与BD分子形成[F(BD)4]2+,其原因是BD分子中含有____________ 。
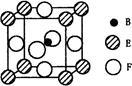
(5)由B、E、F三种元素形成的一种具有超导性的晶体,晶胞如图所示。B位于E和F原子紧密堆积所形成的空隙当中。与一个F原子距离最近的F原子的数目为_______ ,该晶体的化学式为____________ 。若该晶体的相对分子质量为M,阿伏加德罗常数为NA,B、E、F三种元素的原子半径分别为r1pm、r2pm、r3pm,,则该晶体的密度表达式为_______ g·cm-3。
(1)F的基态原子价电子排布式为
(2)B、C、D、E的原子的第一电离能由小到大的顺序为
(3)下列关于B2A2分子和A2D2分子的说法正确的是
A.分子中都含有σ键和π键
B.中心原子都sp杂化
C.都是含极性键和非极性键的非极性分子
D.互为等电子体
E.B2A2分子的沸点明显低于A2D2分子
(4)F2+能与BD分子形成[F(BD)4]2+,其原因是BD分子中含有
(5)由B、E、F三种元素形成的一种具有超导性的晶体,晶胞如图所示。B位于E和F原子紧密堆积所形成的空隙当中。与一个F原子距离最近的F原子的数目为

您最近一年使用:0次
12-13高三·贵州·阶段练习
名校
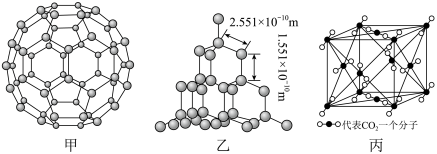
9 . 下面是C60、金刚石和二氧化碳的分子模型。
请回答下列问题:
(1)硅与碳同主族,写出硅原子基态时的核外电子排布式:_________________
(2)从晶体类型来看,C60属于_________ 晶体。
(3)二氧化硅结构跟金刚石结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察图乙中金刚石的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目是__________________________ ;晶体硅中硅原子与共价键的个数比为____________
(4)图丙是二氧化碳的晶胞模型,图中显示出的二氧化碳分子数为14个。实际上一个二氧化碳晶胞中含有________ 个二氧化碳分子,二氧化碳分子中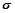 键与
键与 键的个数比为
键的个数比为________________ 。
(5)有机化合物中碳原子的成键方式有多种,这也是有机化合物种类繁多的原因之一。丙烷分子中2号碳原子的杂化方式是_______ ,丙烯分子中2号碳原子的杂化方式是_______ ,丙烯分子中最多有______ 个原子共平面。

请回答下列问题:
(1)硅与碳同主族,写出硅原子基态时的核外电子排布式:
(2)从晶体类型来看,C60属于
(3)二氧化硅结构跟金刚石结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察图乙中金刚石的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目是
(4)图丙是二氧化碳的晶胞模型,图中显示出的二氧化碳分子数为14个。实际上一个二氧化碳晶胞中含有
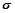 键与
键与 键的个数比为
键的个数比为(5)有机化合物中碳原子的成键方式有多种,这也是有机化合物种类繁多的原因之一。丙烷分子中2号碳原子的杂化方式是
您最近一年使用:0次
2016-12-09更新
|
961次组卷
|
4卷引用:云南省澄江市第一中学2021-2022学年高三下学期3月月考理综化学试题
10-11高一下·浙江杭州·期中
名校
解题方法
10 . 某原子核外共有n个电子层(n>3),则(n-1)层最多容纳的电子数为
| A.8个 | B.18个 | C.32个 | D.2(n-1)2个 |
您最近一年使用:0次
2016-12-09更新
|
614次组卷
|
10卷引用:云南省临沧市凤庆县第一中学2021-2022学年高一下学期3月份考试化学试题
云南省临沧市凤庆县第一中学2021-2022学年高一下学期3月份考试化学试题(已下线)2010—2011学年浙江省杭州师范大学附属中学高一下学期期中考试化学试卷(已下线)2011-2012学年浙江省余姚中学高一下学期期中考试文科化学试卷(已下线)2012-2013学年浙江省杭州市西湖高级中学高一3月月考化学试卷2016-2017学年四川省绵阳南山中学高一下学期3月月考化学试卷2020年春季鲁教版高中化学必修2第1章《原子结构与元素周期律》测试卷2020届高三化学二轮物质结构题型专攻——原子结构与性质【基础专练】河北省石家庄二中实验学校2019-2020学年高一下学期3月月考化学试题湖北省竹山县第二中学2020-2021学年高一下学期第一次月考化学试题(已下线)2.3.2 原子核外电子排布(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)



