1 . 五种前四周期的元素X、Y、Z、Q、T。已知X元素基态原子的M层有6种运动状态不同的电子;Y原子的价电子构型为3d84s2,基态Z原子的L层p能级有一个空轨道;Q原子的L电子层的p能级只有一对成对电子;基态T原子的M电子层上p轨道半充满。下列说法错误的是
| A.Y、Q及氢三种元素形成的某化合物,能用于制作可充电电池的电极材料 |
| B.若X、T、Z的最高价的氧化物对应的水化物分别为u、v、w,则酸性为:u>v>w。理由是含氧酸酸性与非羟基氧原子数有关 |
| C.X、Y、T三种元素第一电离能的大小次序是:X>T>Y |
| D.化合物ZQ2、ZX2均是由极性键构成的非极性分子 |
您最近一年使用:0次
2 . 下列关于价电子排布3s23p4的描述正确的是
| A.它的元素符号为O |
| B.它的核外电子排布式为1s22s22p63s23p4 |
| C.可以与H2化合生成液态化合物 |
D.其电子排布图为 |
您最近一年使用:0次
2024-04-13更新
|
231次组卷
|
44卷引用:云南省武定县第一中学2018-2019学年高二上学期12月份考试化学试题
云南省武定县第一中学2018-2019学年高二上学期12月份考试化学试题云南省昭通水田新区中学2018-2019学年高二上学期12月月考化学试题(已下线)吉林一中2009--2010学年度下学期期末考试第一次质量检测高二化学试卷(已下线)2011-2012学年福建省厦门一中高二上学期期中考试化学试卷(已下线)2012届浙江省杭州高中高三第二次月考化学试卷(已下线)2011-2012学年内蒙古包头三十三中高二下学期期中考试化学试卷(已下线)2011-2012学年河南许昌鄢陵一高高二下学期期中考试化学试卷(已下线)2012-2013学年山东省淄博市沂源一中高二下学期期中模块检测化学卷(已下线)2012-2013学年山东省济南一中高二下学期期中考试理科化学试卷(已下线)2013-2014学年福建省厦门一中高二上学期期中考试化学试卷2013-2014山东省即墨市高二下学期期中考试化学试卷2015-2016学年西藏日喀则一中高二10月月考化学试卷2015-2016学年贵州省思南中学高二下第二次月考化学试卷宁夏育才中学2016-2017学年高二下学期期中考试化学试题江苏省盘湾中学、陈洋中学2017-2018学年高二上学期期中联考(选修)化学试题2016-2017学年高中化学选修3(人教版)模块综合测评【全国校级联考】新疆昌吉市教育共同体四校2017-2018学年高二下学期期末联考化学试题宁夏回族自治区青铜峡市高级中学2018-2019学年高二上学期期末考试化学试题宁夏回族自治区银川市长庆高级中学2018-2019学年高二下学期第二次月考化学试题新疆维吾尔自治区北京大学附属中学新疆分校2018-2019学年高二下学期期中考试化学试题福建省长泰县第一中学2018-2019学年高二下学期期末考试化学试题新疆石河子第二中学2018-2019学年高二下学期第一次月考化学试题河南省林州市第一中学2019-2020学年高二3月线上调研考试化学试题江苏省盐城市伍佑中学2019-2020学年高二下学期第一次阶段考试化学试题湖北省武汉市黄陂区第六中学2019-2020学年高二下学期三月线上考试化学试题甘肃省静宁县第一中学2019-2020学年高二下学期期中考试(第二次月考)化学试题(普通班)广西防城港市防城中学2019-2020学年高二下学期期中考试化学试题湖北省仙桃市汉江中学2018-2019学年高二下学期期中考试化学试题新疆新源县第二中学2019-2020学年高二下学期期末考试化学试题(已下线)考点33 原子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时54 原子结构与性质-2022年高考化学一轮复习小题多维练(全国通用)宁夏石嘴山市平罗中学2021-2022学年高二上学期期中考试化学试题宁夏青铜峡市高级中学2021-2022学年高二上学期期末考试化学试题(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)黑龙江省牡丹江市海林市朝鲜族中学2021-2022学年高二下学期第一次月考化学试题宁夏吴忠市吴忠中学2022-2023学年高三上学期阶段性测试 化学试题河北省保定高碑店市崇德实验中学2022-2023学年高三上学期10月月考化学试题重庆市西南大学附属中学校2022-2023学年高二上学期开学定时训练化学试题(广延班)(已下线)考点41 原子结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)江西省南昌市八一中学2022-2023学年高二上学期1月期末考试化学试题(已下线)第01讲 原子结构-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)选择题6-10(已下线)第一章章节专项提升贵州省遵义市桐梓县荣兴高级中学2023-2024学年高二下学期第一次(3月)月考化学试题
名校
3 . 铬、钛、钴都属于过渡元素。
(1)铬元素属于周期表的___________ 区,基态Cr原子有___________ 个未成对电子。同周期的基态原子中,与Cr最高能层电子数相同的还有___________ (写元素符号)。
(2)钛元素形成的钛酸钡晶体的晶胞结构如图所示,该晶体经X射线分析得出,重复单元为立方体,顶点位置被Ti4+所占据,体心位置被Ba2+所占据,棱心位置被O2-所占据。___________ 。
②若将Ti4+置于晶胞的体心,Ba2+置于晶胞顶点,则O2-处于立方体的___________ 位置。
③Ti4+的氧配位数和Ba2+的氧配位数分别为___________ 。
(3)钴的某种配合物的化学式为[Co(H2O)6]F2,该配合物的立方晶胞如图所示,其晶胞参数为apm。___________ 个。
②设阿伏加德罗常数的值为NA,则[Co(H2O)6]F2晶体的密度为___________ g·cm-3。
(1)铬元素属于周期表的
(2)钛元素形成的钛酸钡晶体的晶胞结构如图所示,该晶体经X射线分析得出,重复单元为立方体,顶点位置被Ti4+所占据,体心位置被Ba2+所占据,棱心位置被O2-所占据。
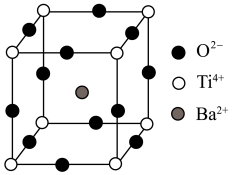
②若将Ti4+置于晶胞的体心,Ba2+置于晶胞顶点,则O2-处于立方体的
③Ti4+的氧配位数和Ba2+的氧配位数分别为
(3)钴的某种配合物的化学式为[Co(H2O)6]F2,该配合物的立方晶胞如图所示,其晶胞参数为apm。
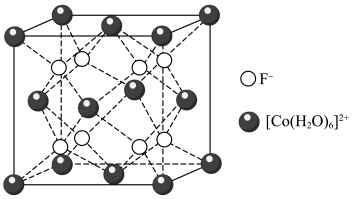
②设阿伏加德罗常数的值为NA,则[Co(H2O)6]F2晶体的密度为
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
(1)Fe成为阳离子时首先失去___________ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___________ 。
(2)基态S原子电子占据最高能级的电子云轮廓图为___________ 形。
(3)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该原子价层电子的轨道表示式___________ ,该元素名称为___________ 。
(4)已知CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为___________ 。
(5)某有机物的结构简式为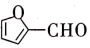 ,该分子内含有___________ (填序号)。
,该分子内含有___________ (填序号)。
(6)已知元素X的气态原子逐个失去第1个至第4个电子所需能量如下表所示:
元素X的常见化合价是___________(填序号)。
(1)Fe成为阳离子时首先失去
(2)基态S原子电子占据最高能级的电子云轮廓图为
(3)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该原子价层电子的轨道表示式
(4)已知CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
(5)某有机物的结构简式为
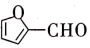 ,该分子内含有___________ (填序号)。
,该分子内含有___________ (填序号)。| A.11个σ键、2个π键 | B.10个σ键、2个π键 |
| C.10个σ键、3个π键 | D.11个σ键、3个π键 |
| I1 | I2 | I3 | I4 | |
| 电离能/(kJ·mol-1) | 578 | 1817 | 2745 | 11578 |
| A.+1 | B.+2 | C.+3 | D.+4 |
您最近一年使用:0次
5 . 下列状态的磷微粒中,失去最外层一个电子所需能量最大的是
| A.[Ne]3s23p3 | B.[Ne]3s23p2 | C.[Ne]3s23p24s1 | D.[Ne]3s23p14s1 |
您最近一年使用:0次
6 . 下列说法正确的是
| A.气态Mn2+再失去一个电子比气态Fe2+再失去一个电子容易 |
| B.离子半径Na+>Mg2+>O2- |
C.基态硫原子的电子排布式若写成 违背了洪特规则 违背了洪特规则 |
| D.两个p轨道之间只能形成π键,不能形成σ键 |
您最近一年使用:0次
7 . 一种工业洗涤剂中间体的结构如图,其中 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是
 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是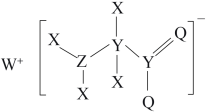
A.电负性大小: |
B.简单离子半径: |
C.简单氢化物的沸点: |
D.阴离子中各原子都满足 电子稳定结构 电子稳定结构 |
您最近一年使用:0次
2024-04-08更新
|
96次组卷
|
14卷引用:2024届高考化学考点剖析精创专题卷——专题七 物质结构 元素周期律
2024届高考化学考点剖析精创专题卷——专题七 物质结构 元素周期律云南省大理州实验中学2021-2022学年高二下学期化学期中考试题山东省德州市2020-2021学年高二下学期期末考试化学试题福建省三明市五县2021-2022学年高二下学期联合质检考试(期中)化学试题厦门外国语学校2021-2022学年高二下学期期中考试化学试题湖北省黄冈市麻城市第二中学2021-2022学年高二下学期3月月考化学试题 吉林省吉林第一中学2022-2023学年高二上学期11月月考化学试题陕西省武功县普集高级中学2022-2023学年高二下学期第一次月考化学试题广西钦州市第四中学2022-2023学年高二下学期2月考试化学试题福建省龙岩市一级校联盟2022-2023学年高二下学期4月期中考试化学试题福建省三明第一中学2022-2023学年高二下学期期中考试化学试题福建省厦门市湖滨中学2022-2023学年高二下学期期中考试化学试题四川省达州市万源中学2023-2024学年高二下学期4月月考化学试题河南省郑州市十校2023-2024学年高二下学期期中联考化学试卷
8 .  为原子序数依次增大的短周期主族元素,W与Z可形成两种常温下呈液态的化合物。Q的基态原子核外电子有29种运动状态,由
为原子序数依次增大的短周期主族元素,W与Z可形成两种常温下呈液态的化合物。Q的基态原子核外电子有29种运动状态,由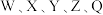 形成的一种化合物结构如图所示。
形成的一种化合物结构如图所示。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为原子序数依次增大的短周期主族元素,W与Z可形成两种常温下呈液态的化合物。Q的基态原子核外电子有29种运动状态,由
为原子序数依次增大的短周期主族元素,W与Z可形成两种常温下呈液态的化合物。Q的基态原子核外电子有29种运动状态,由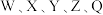 形成的一种化合物结构如图所示。
形成的一种化合物结构如图所示。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是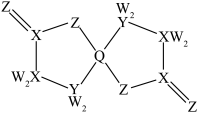
A.第一电离能: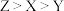 | B.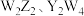 均为非极性分子 均为非极性分子 |
C. 该化合物中含 该化合物中含 键的数目为 键的数目为 | D.Q的基态原子价层电子排布式为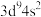 |
您最近一年使用:0次
2024-04-07更新
|
172次组卷
|
2卷引用:云南省昆明市2024届高三“三诊一模”教学质量检测(二模)理综-化学试题
9 . 已知四氨合铜离子的模型如图甲,CaF2晶体的晶胞如图乙,阿伏加德罗常数的值用NA表示。下列有关说法正确的是
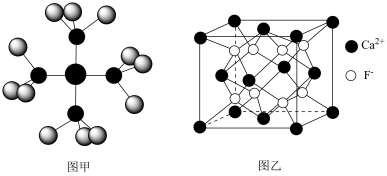

| A.基态Cu的电子排布式为[Ar]3d84s1 |
| B.四氨合铜离子中存在极性共价键、配位键、离子键 |
| C.距离Ca2+最近且等距离的F-有6个 |
D.若CaF2晶胞的棱长为acm,CaF2的密度为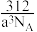 g/cm3 g/cm3 |
您最近一年使用:0次
名校
解题方法
10 . X、Y、Z三种元素基态原子的价电子排布式分别为 、
、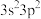 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是
 、
、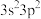 和
和 ,由这三种元素组成的化合物的化学式是
,由这三种元素组成的化合物的化学式是A. | B.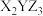 | C.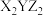 | D. |
您最近一年使用:0次
2024-04-04更新
|
151次组卷
|
10卷引用:云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题
云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题云南省宁蒗彝族自治县第一中学2021-2022学年高二下学期3月考试化学试题2014-2015河南省实验中学高二下学期期中考试化学试卷宁夏银川市唐徕回民中学2017-2018学年高二4月月考化学试题贵州省剑河县第二高级中学2018-2019学年高二上学期12月份考试化学试题吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题湖南省汨罗市楚雄中学2021-2022学年高二12月月考化学试题四川省广元中学2021-2022学年高二下学期第一次段考化学试题黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期12月月考化学试题甘肃省武山县第一高级中学2023-2024学年高二下学期第一次月考化学试卷



