解题方法
1 . X、Y、Z为短周期主族元素,X的原子序数是Y的8倍,X与Z同周期,且基态X、Z原子的未成对电子数相同。M是人体的必需微量元素之一,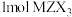 含有
含有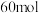 质子。下列说法一定正确的是
质子。下列说法一定正确的是
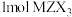 含有
含有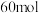 质子。下列说法一定正确的是
质子。下列说法一定正确的是| A.M在元素周期表中位于d区 | B. 中Z原子采用 中Z原子采用 杂化 杂化 |
| C.X、Z分别与Y形成化合物的沸点:X>Z | D.同周期元素中第一电离能比X大的有3种 |
您最近一年使用:0次
名校
解题方法
2 . 离子液体指由体积很大的阴、阳离子组成,并且在室温或室温附近温度下呈液态的盐。1-丁基-3-甲基咪唑六氟磷酸盐是一种离子液体,结构简式如图。下列关于它的叙述不正确的是
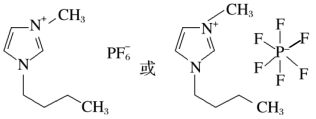
| A.该离子液体所有C原子的杂化方式与N原子杂化方式相同 |
| B.有关元素的电负性:H<C<N<F |
| C.该离子液体属于含共价键的离子化合物 |
| D.该离子液体难挥发,可用作溶剂 |
您最近一年使用:0次
名校
解题方法
3 . 镧镍合金是一种储氢材料,其晶胞可认为由两种结构不同的层交替堆积而成,如下图所示。已知该合金的密度为 ,该合金的晶胞中最多可容纳9个氢原子。下列叙述错误的是
,该合金的晶胞中最多可容纳9个氢原子。下列叙述错误的是
 ,该合金的晶胞中最多可容纳9个氢原子。下列叙述错误的是
,该合金的晶胞中最多可容纳9个氢原子。下列叙述错误的是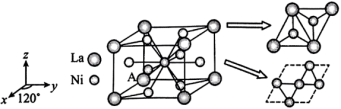
A.基态Ni原子的价电子排布式为 |
B.该合金的化学式为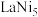 |
C.假定吸氢后体积不变,则合金中氢的最大密度为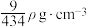 |
D.设A处La的原子坐标为 ,则晶胞底面上Ni的原子坐标为 ,则晶胞底面上Ni的原子坐标为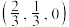 或 或 |
您最近一年使用:0次
解题方法
4 . 我国自主研发的用氟硼铍酸钾(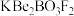 )晶体制造深紫外固体激光器技术领先世界。回答下列问题:
)晶体制造深紫外固体激光器技术领先世界。回答下列问题:
(1)基态K原子核外有_____ 种不同运动状态的电子,能量最低的空轨道的符号是_____ 。
(2)在1000℃时,氯化铍以 形式存在,该分子的空间构型为
形式存在,该分子的空间构型为_____ ;在500~600℃气相中,氯化铍则以二聚体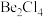 的形式存在,画出
的形式存在,画出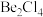 的结构:
的结构:_____ (标出配位键)。
(3)在第二周期中第一电离能介于B和O两种元素之间的元素有_____ (填元素符号)。
(4) 分子中的
分子中的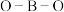 的键角大于
的键角大于 中的
中的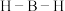 的键角,判断依据是
的键角,判断依据是_____ (从中心原子杂化方式的角度来解释)。
(5)一定条件下,实验测得的HF的相对分子质量总是大于理论值,原因是_____ 。
(6)六方氮化硼在高温高压下,可以转化为立方氮化硼,二者晶体结构如图所示: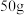 六方氮化硼晶体中含有六元环的数目为
六方氮化硼晶体中含有六元环的数目为_____  (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
②立方氮化硼晶体中,设晶胞中最近的B、N原子之间的距离为apm,晶体的密度为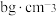 。则阿伏加德罗常数为
。则阿伏加德罗常数为_____  。(列式即可,用含a、b的代数式表示)
。(列式即可,用含a、b的代数式表示)
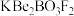 )晶体制造深紫外固体激光器技术领先世界。回答下列问题:
)晶体制造深紫外固体激光器技术领先世界。回答下列问题:(1)基态K原子核外有
(2)在1000℃时,氯化铍以
 形式存在,该分子的空间构型为
形式存在,该分子的空间构型为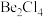 的形式存在,画出
的形式存在,画出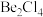 的结构:
的结构:(3)在第二周期中第一电离能介于B和O两种元素之间的元素有
(4)
 分子中的
分子中的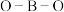 的键角大于
的键角大于 中的
中的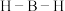 的键角,判断依据是
的键角,判断依据是(5)一定条件下,实验测得的HF的相对分子质量总是大于理论值,原因是
(6)六方氮化硼在高温高压下,可以转化为立方氮化硼,二者晶体结构如图所示:

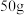 六方氮化硼晶体中含有六元环的数目为
六方氮化硼晶体中含有六元环的数目为 (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。②立方氮化硼晶体中,设晶胞中最近的B、N原子之间的距离为apm,晶体的密度为
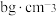 。则阿伏加德罗常数为
。则阿伏加德罗常数为 。(列式即可,用含a、b的代数式表示)
。(列式即可,用含a、b的代数式表示)
您最近一年使用:0次
7日内更新
|
78次组卷
|
2卷引用:湖北省十堰市2024届高三下学期第三次模拟化学试题
5 . 下列表述正确的是
A.基态 原子的核外电子排布式: 原子的核外电子排布式: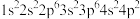 |
B.正丁烷的球棍模型: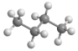 |
C.乙烯中 键与 键与 键的数量比为 键的数量比为 |
D. 溶液中含有的微粒: 溶液中含有的微粒: 、 、 、 、 、 、 |
您最近一年使用:0次
7日内更新
|
190次组卷
|
3卷引用:湖北省十堰市2024届高三下学期第三次模拟化学试题
名校
6 . 我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛转化为二氧化碳和水,反应化学方程式为: ,用
,用 表示阿伏加德罗常数的值,下列有关说法正确的是
表示阿伏加德罗常数的值,下列有关说法正确的是
 ,用
,用 表示阿伏加德罗常数的值,下列有关说法正确的是
表示阿伏加德罗常数的值,下列有关说法正确的是| A.该反应涉及元素中第一电离能最大的是C |
| B.HCHO为含极性键的平面正三角形分子 |
C.处理22.4L HCHO转移电子数目为 |
D.1mol  分子中,碳原子的价层电子对数为 分子中,碳原子的价层电子对数为 |
您最近一年使用:0次
7日内更新
|
40次组卷
|
2卷引用:湖北省宜荆荆随恩2023-2024学年高二下学期5月联考化学试题
名校
7 . 钛(Ti)、铬(Cr)、锰(Mn)、钴(Co)、镉(Cd)等过渡金属及其化合物在生产生活中应用广泛,回答下列问题。
(1)基态Cr原子的价层电子轨道表示式为___________ 。
(2)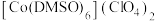 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中Cl原子的杂化轨道类型是
中Cl原子的杂化轨道类型是___________ , 中键角<C-S-O
中键角<C-S-O___________  中键角<C-C-O(填“大于”“小于”或“等于”)。
中键角<C-C-O(填“大于”“小于”或“等于”)。
(3) 与
与 等配体可形成配离子。
等配体可形成配离子。 中2个
中2个 被2个
被2个 替代只得到1种结构,则
替代只得到1种结构,则 的空间构型是
的空间构型是___________ 。
(4)钛与卤素形成的化合物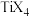 熔点如下表:
熔点如下表:
它们熔点差异的原因___________ 。
(5)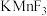 晶体有钙钛矿型的立方结构,晶胞结构如图1所示。在
晶体有钙钛矿型的立方结构,晶胞结构如图1所示。在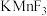 晶胞结构的另一种表示中,Mn处于各顶角位置,在该晶胞结构中,沿晶胞对角面取得的截图如图2所示。F在晶胞中的位置对应的序号为
晶胞结构的另一种表示中,Mn处于各顶角位置,在该晶胞结构中,沿晶胞对角面取得的截图如图2所示。F在晶胞中的位置对应的序号为___________ (填阿拉伯数字序号)。 占据
占据 形成的
形成的___________ (填“四面体空隙”或“八面体空隙”)。 为阿伏加德罗常数的值,钴蓝晶体的密度为
为阿伏加德罗常数的值,钴蓝晶体的密度为___________  (列计算式)。
(列计算式)。
(1)基态Cr原子的价层电子轨道表示式为
(2)
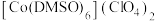 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中Cl原子的杂化轨道类型是
中Cl原子的杂化轨道类型是 中键角<C-S-O
中键角<C-S-O 中键角<C-C-O(填“大于”“小于”或“等于”)。
中键角<C-C-O(填“大于”“小于”或“等于”)。(3)
 与
与 等配体可形成配离子。
等配体可形成配离子。 中2个
中2个 被2个
被2个 替代只得到1种结构,则
替代只得到1种结构,则 的空间构型是
的空间构型是(4)钛与卤素形成的化合物
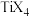 熔点如下表:
熔点如下表: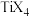 |  |  |  |  |
| 熔点℃ | 377 |  | 38.3 | 153 |
(5)
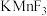 晶体有钙钛矿型的立方结构,晶胞结构如图1所示。在
晶体有钙钛矿型的立方结构,晶胞结构如图1所示。在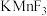 晶胞结构的另一种表示中,Mn处于各顶角位置,在该晶胞结构中,沿晶胞对角面取得的截图如图2所示。F在晶胞中的位置对应的序号为
晶胞结构的另一种表示中,Mn处于各顶角位置,在该晶胞结构中,沿晶胞对角面取得的截图如图2所示。F在晶胞中的位置对应的序号为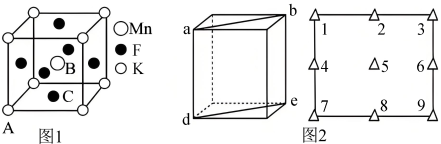
 占据
占据 形成的
形成的 为阿伏加德罗常数的值,钴蓝晶体的密度为
为阿伏加德罗常数的值,钴蓝晶体的密度为 (列计算式)。
(列计算式)。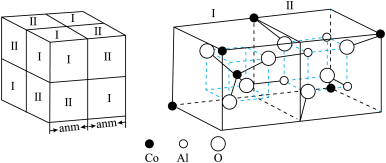
您最近一年使用:0次
名校
8 .  与
与 在水溶液中发生反应:
在水溶液中发生反应: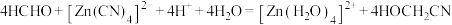 ,下列有关说法正确的是
,下列有关说法正确的是
 与
与 在水溶液中发生反应:
在水溶液中发生反应: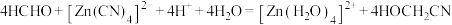 ,下列有关说法正确的是
,下列有关说法正确的是A. 中存在共价键和配位键 中存在共价键和配位键 |
B. 中碳原子以 中碳原子以 的形式杂化 的形式杂化 |
C. 中的 中的 键和 键和 键数目相同 键数目相同 |
D. 原子的 原子的 能级中有空轨道 能级中有空轨道 |
您最近一年使用:0次
名校
解题方法
9 . 七水硫酸亚铁,俗称绿矾,化学式为 ,能制造多种工业产品,其结构示意图如下。下列说法不正确的是
,能制造多种工业产品,其结构示意图如下。下列说法不正确的是
 ,能制造多种工业产品,其结构示意图如下。下列说法不正确的是
,能制造多种工业产品,其结构示意图如下。下列说法不正确的是
| A.第一电离能:O>S>Fe |
B. 的配位数为6 的配位数为6 |
C.气态基态 再失去一个电子比气态基态 再失去一个电子比气态基态 更难 更难 |
D. 中存在的作用力有离子键、极性键、配位键、氢键 中存在的作用力有离子键、极性键、配位键、氢键 |
您最近一年使用:0次
名校
10 . 锂离子电池中,一种电解质添加剂的阴离子结构如下图所示。Y、Z、M和R是原子序数依次增大的短周期元素。下列说法正确的是
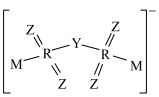
A.氧化性: | B.键角: |
| C.第一电离能:M>Z>Y | D.简单离子半径:R>Y>Z |
您最近一年使用:0次
7日内更新
|
106次组卷
|
3卷引用:湖北省黄冈中学2024届高三下学期5月第三次模拟考试化学试题



