解题方法
1 . 硅及其化合物在生活、生产和科技等方面应用广泛。工业制备高纯硅的主要过程如下:
石英砂(主要成分 )
)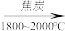 粗硅
粗硅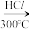

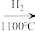 高纯硅
高纯硅
(1) 位于元素周期表第
位于元素周期表第_____ 周期,第_____ 族。
(2)由硅原子核形成的三种微粒,电子排布式分别为:a.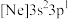 、b.
、b.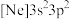 、c.
、c.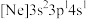 ,有关这些微粒的叙述,正确的是_____(填标号)。
,有关这些微粒的叙述,正确的是_____(填标号)。
(3)石英砂与焦炭反应制备粗硅的化学方程式为_____ 。粗硅与 反应过程中会有副产物
反应过程中会有副产物 生成,
生成, 中
中 的杂化轨道类型为
的杂化轨道类型为_____ 。 的键角
的键角_____ (填“大于”、“小于”或“等于”) 的键角。
的键角。
(4) 以空间结构为
以空间结构为_____ 。 和
和 会剧烈反应,写出该反应的化学方程式
会剧烈反应,写出该反应的化学方程式_____ (已知:电负性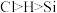 )。
)。
石英砂(主要成分
 )
)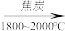 粗硅
粗硅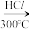

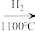 高纯硅
高纯硅(1)
 位于元素周期表第
位于元素周期表第(2)由硅原子核形成的三种微粒,电子排布式分别为:a.
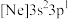 、b.
、b.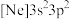 、c.
、c.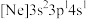 ,有关这些微粒的叙述,正确的是_____(填标号)。
,有关这些微粒的叙述,正确的是_____(填标号)。A.微粒半径: |
| B.电子排布属于基态原子(或离子)的是:a、b |
C.电离一个电子所需最低能量: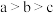 |
D.得电子能力: |
 反应过程中会有副产物
反应过程中会有副产物 生成,
生成, 中
中 的杂化轨道类型为
的杂化轨道类型为 的键角
的键角 的键角。
的键角。(4)
 以空间结构为
以空间结构为 和
和 会剧烈反应,写出该反应的化学方程式
会剧烈反应,写出该反应的化学方程式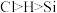 )。
)。
您最近一年使用:0次
2024-04-29更新
|
38次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
2 . 已知W、X、Y、Z、M是原子序数依次增大的前四周期元素。W的 轨道半充满;Y是电负性最大的元素:Z是短周期元素且Z的逐级电离能(
轨道半充满;Y是电负性最大的元素:Z是短周期元素且Z的逐级电离能( )依次为738、1451、7733、10540、13630、17995;M元素原子最外层电子只有一种自旋取向,其次外层内所有轨道的电子均成对。下列说法正确的是
)依次为738、1451、7733、10540、13630、17995;M元素原子最外层电子只有一种自旋取向,其次外层内所有轨道的电子均成对。下列说法正确的是
 轨道半充满;Y是电负性最大的元素:Z是短周期元素且Z的逐级电离能(
轨道半充满;Y是电负性最大的元素:Z是短周期元素且Z的逐级电离能( )依次为738、1451、7733、10540、13630、17995;M元素原子最外层电子只有一种自旋取向,其次外层内所有轨道的电子均成对。下列说法正确的是
)依次为738、1451、7733、10540、13630、17995;M元素原子最外层电子只有一种自旋取向,其次外层内所有轨道的电子均成对。下列说法正确的是A.第一电离能: |
| B.W、Y的简单氢化物的水溶液均可盛放于玻璃瓶中 |
| C.M基态原子核外电子有15种空间运动状态 |
D.工业上常用电解熔融 的方式制备单质Z 的方式制备单质Z |
您最近一年使用:0次
2024-04-29更新
|
75次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
3 . 下列判断及其解释都正确的是
| 选项 | 判断 | 解释 |
| A | 热稳定性: |  相对分子质量大 相对分子质量大 |
| B | 酸性: | 非金属性 大于S 大于S |
| C |  原子s电子云半径: 原子s电子云半径: | 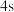 电子的能量高,在离核更远的区域出现的概率大 电子的能量高,在离核更远的区域出现的概率大 |
| D | 键角: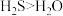 | 电负性O大于S, 中 中 键电子对之间的斥力小于 键电子对之间的斥力小于 中 中 键电子对之间的斥力 键电子对之间的斥力 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-29更新
|
54次组卷
|
2卷引用:湖北省黄冈市2023-2024学年高二上学期期末调研考试化学试题
4 . 下列化学用语表达正确的是
A. 的电子式: 的电子式: |
B. 分子的球棍模型: 分子的球棍模型: |
C. 的 的 模型: 模型: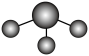 |
D.用电子云轮廓图表示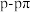 键的形成: 键的形成: |
您最近一年使用:0次
5 . 元素钇(Y)是制备航空航天设备所需的特殊材料的关键成分。一种从某矿石(含钇、铁、铝等元素)中提取Y元素的工艺流程如下:
回答下列问题。
(1)钇位于第5周期第IIIB族,钇的价电子排布式为___________ 。
(2)Mg的第一电离能___________ Al(填“>”或“<”),原因是___________ 。
(3)“过滤1”操作中需将所得混合滤渣洗涤2~3次,并将洗涤液与“滤液1”合并。
①验证混合滤渣已经洗涤干净的操作与现象是___________ 。
②洗涤液与“滤液1”合并的目的是___________ 。
(4)“过滤2”后,滤渣中无Mg元素,“滤液2”中 浓度为0.8
浓度为0.8 。为尽可能多的提取
。为尽可能多的提取 ,可提高
,可提高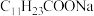 的加入量,但应确保“过滤2”前的溶液中
的加入量,但应确保“过滤2”前的溶液中 )低于
)低于___________ mol/L。
(5)钇可用于制备高活性的合金类催化剂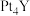 。
。
①还原YCl3和PtCl4混合熔融盐制备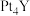 ,生成0.1
,生成0.1 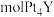 时转移的电子的物质的量为
时转移的电子的物质的量为___________ mol。
②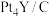 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化电极反应,则
用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化电极反应,则  发生的电极反应式为
发生的电极反应式为___________ 。
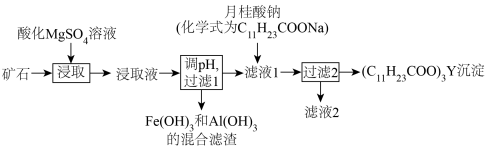

回答下列问题。
(1)钇位于第5周期第IIIB族,钇的价电子排布式为
(2)Mg的第一电离能
(3)“过滤1”操作中需将所得混合滤渣洗涤2~3次,并将洗涤液与“滤液1”合并。
①验证混合滤渣已经洗涤干净的操作与现象是
②洗涤液与“滤液1”合并的目的是
(4)“过滤2”后,滤渣中无Mg元素,“滤液2”中
 浓度为0.8
浓度为0.8 。为尽可能多的提取
。为尽可能多的提取 ,可提高
,可提高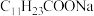 的加入量,但应确保“过滤2”前的溶液中
的加入量,但应确保“过滤2”前的溶液中 )低于
)低于(5)钇可用于制备高活性的合金类催化剂
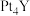 。
。①还原YCl3和PtCl4混合熔融盐制备
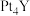 ,生成0.1
,生成0.1 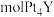 时转移的电子的物质的量为
时转移的电子的物质的量为②
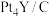 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化电极反应,则
用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化电极反应,则  发生的电极反应式为
发生的电极反应式为
您最近一年使用:0次
6 . 已知元素X、Y、Z、M和R在周期表中的位置如下图所示,其中X元素基态原子中M能层全充满,N能层只有一个电子。下列关于这5种元素说法正确的是
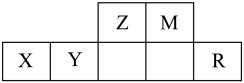
A.第二电离能: | B.M单质常温下不与NaOH溶液反应 |
C.R的核外电子排布式为[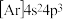 | D.工业上电解Z的氧化物制备Z单质 |
您最近一年使用:0次
解题方法
7 . 一水合甘氨酸锌是一种饲料添加剂,结构简式如图所示。下列关于该物质说法错误的是
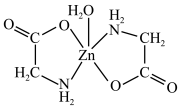
A.电负性: | B.Zn原子的杂化方式为sp3 |
| C.既有极性键又有非极性键 | D.碳原子的价层电子对数为3和4 |
您最近一年使用:0次
8 . 下列关于同主族元素结构性质对比的结论与解释有错误的是
| 选项 | 结论 | 解释 |
| A | 稳定性:H2O﹥H2S | O的半径比S的小 |
| B | 键角:PH3﹤NH3 | PH3的成键电子对间排斥力较小 |
| C | 酸性:HF﹥HCl | F的电负性比Cl大,H-F极性比H-C1大 |
| D | 稳定性:Si原子间的π键﹤C原子间的π键 | Si-Si σ键比C-C σ键的键长长 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . X、Y、Z、M均为第三周期主族元素。该周期所有主族元素中,X的第一电离能最大,Y的金属性最强。Z和M原子核外均有2个单电子,Z的原子半径大于M。下列说法正确的是
| A.简单离子半径:Y>M | B.X单质为单原子分子,不存在化学键 |
| C.Y离子能促进水的电离 | D.Z原子核外电子的空间运动状态有8种 |
您最近一年使用:0次
10 . 下列关于Be、Mg及其化合物结构与性质的论述错误的是
| A.基态Mg原子有四种能量不同的电子 |
| B.Be(OH)2和Mg(OH)2均能溶于盐酸,均不溶于NaOH溶液 |
C.0.1 mol/L  2溶液的pH比0.1mol/L Mg(NO3)2溶液小 2溶液的pH比0.1mol/L Mg(NO3)2溶液小 |
D.MgCl2溶液与  2溶液分别蒸干并灼烧,剩余固体成分相同 2溶液分别蒸干并灼烧,剩余固体成分相同 |
您最近一年使用:0次



