1 . 下列描述中正确的是
A.氮原子的价电子排布图: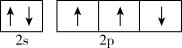 |
| B.2p和3p轨道形状均为哑铃形,能量也相等 |
C.价电子排布为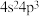 的元素位于第四周期ⅤA族,是p区元素 的元素位于第四周期ⅤA族,是p区元素 |
D.钠原子由 时,原子释放能量,由基态转化成激发态 时,原子释放能量,由基态转化成激发态 |
您最近一年使用:0次
2022-03-16更新
|
388次组卷
|
23卷引用:湖北省荆门市2021-2022学年高二上学期期末质量检测化学试题
湖北省荆门市2021-2022学年高二上学期期末质量检测化学试题2014-2015宁夏银川市唐徕回民中学高二下学期3月月考化学试卷2015届上海市青浦区高考二模化学试卷安徽省蚌埠市第二中学2016-2017学年高二下学期期中考试化学试题吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题新疆石河子第二中学2018-2019学年高二下学期期末考试化学试题江苏省南京师范大学苏州实验学校2019-2020学年高二上学期期中考试化学试题2020届高三化学选修三二轮专题复习——能级、能层、原子轨道第1章 原子结构——B拓展区综合拓展(鲁科版选修3)安微蚌埠二中2019-2020学年高二4月检测化学试题辽宁省清原满族自治县第二高级中学2020-2021学年高二下学期期中考试化学试题湖北省荆州市八县市2021-2022学年高二上学期期末质量检测化学试题重庆市第七中学2021-2022学年高二下学期第一次月考化学试题福建省三明市五县2021-2022学年高二下学期联合质检考试(期中)化学试题宁夏银川市景博中学2021-2022学年高二下学期第二次月考化学试题新疆精河县高级中学2021-2022学年高二下学期期中考试化学试题安徽省宿州市第二中学2022-2023学年高二下学期第一次月考化学试题安徽省蚌埠第二中学2022-2023学年高二下学期第一次月考化学试题安徽省安庆市第一中学2022-2023学年高二下学期第一次月考化学试题安徽省亳州市第一中学2022-2023学年高二下学期第一次月考化学试题广东番禺中学2022-2023学年高二下学期科开学考试化学试题宁夏育才中学2022-2023学年高二下学期5月期中考试化学试题湖北省武汉西藏中学2023-2024学年高二下学期5月期中考试化学试题
解题方法
2 . Ⅰ.硼氢化钠(NaBH4)是一种储氢密度较高、价格低廉、兼具安全性与稳定性的固态储氢材料。
(1)基态B原子中电子占据最高能级的符号是___ ,基态B原子中,核外存在___ 对自旋相反的电子。
(2)在周期表中,与B元素的化学性质最相似的邻族元素是___ 。
(3)基态29Cu原子的简化电子排布式为___ 。
Ⅱ.用CO做燃料电池电解CuSO4溶液、FeCl3和FeCl2混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。

(4)甲中通入O2的电极为____ 极,该电极反应方程式为:____ 。
(5)乙中A极析出的气体在标准状况下的体积为____ 。此时要使乙中CuSO4溶液恢复到原来的浓度,需要加入的物质及其物质的量是____ 。
(6)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,则图中③线表示的是____ (填离子符号)的变化。

(1)基态B原子中电子占据最高能级的符号是
(2)在周期表中,与B元素的化学性质最相似的邻族元素是
(3)基态29Cu原子的简化电子排布式为
Ⅱ.用CO做燃料电池电解CuSO4溶液、FeCl3和FeCl2混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。

(4)甲中通入O2的电极为
(5)乙中A极析出的气体在标准状况下的体积为
(6)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,则图中③线表示的是

您最近一年使用:0次
2022-02-19更新
|
129次组卷
|
2卷引用:湖北省荆门市2021-2022学年高二上学期期末质量检测化学试题
名校
解题方法
3 . 下列化学用语只能用来表示一种微粒的是
A. | B. | C. | D. |
您最近一年使用:0次
2021-04-09更新
|
226次组卷
|
4卷引用:湖北省荆门市龙泉中学2020-2021学年高三下学期5月月考化学试题
名校
解题方法
4 . 以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵((NH4)3Fe(C6H5O7)2)。
(1)Fe基态核外电子排布式为________ ;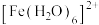 中与Fe2+配位的原子是
中与Fe2+配位的原子是______ (填元素符号)。
(2)H2O2是________ 分子(填“极性”“非极性”),电子式为_______ 。
(3)NH3分子中氮原子的轨道杂化类型是_______ ;C、N、O元素的第一电离能由大到小的顺序为___________ 。
(4)与 互为等电子体的一种分子为
互为等电子体的一种分子为_______ (填化学式)。
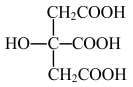
(5)柠檬酸的结构简式如下图。1mol柠檬酸分子中碳原子与氧原子形成的σ键为_________ mol。
(1)Fe基态核外电子排布式为
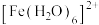 中与Fe2+配位的原子是
中与Fe2+配位的原子是(2)H2O2是
(3)NH3分子中氮原子的轨道杂化类型是
(4)与
 互为等电子体的一种分子为
互为等电子体的一种分子为(5)柠檬酸的结构简式如下图。1mol柠檬酸分子中碳原子与氧原子形成的σ键为

您最近一年使用:0次
2020-08-27更新
|
78次组卷
|
2卷引用:湖北省荆门市龙泉中学2021届高三8月月考化学试题
名校
解题方法
5 . 具有下列电子层结构或性质的原子:①2p轨道上有2对成对电子的原子;②外围电子构型为2s22p3的原子;③短周期第一电离能最小;④第三周期离子半径最小。则下列有关比较中正确的是( )
| A.第一电离能:②>③>①>④ |
| B.原子半径:④>③>②>① |
| C.电负性:①>②>④>③ |
| D.最高正化合价:②>③>①>④ |
您最近一年使用:0次
2020-05-27更新
|
369次组卷
|
5卷引用:湖北省荆门市2019-2020学年高二下学期期末考试化学试题
6 . 下列是几种原子的基态电子排布,电负性最大的原子是
| A.1s22s22p4 | B.1s22s22p63s23p3 |
| C.1s22s22p63s23p2 | D.1s22s22p63s23p64s2 |
您最近一年使用:0次
2020-05-22更新
|
298次组卷
|
38卷引用:湖北省荆门市2016-2017学年高二下学期期末质量检测化学试题
湖北省荆门市2016-2017学年高二下学期期末质量检测化学试题(已下线)09~10年银川一中高二下学期期末考试化学卷(已下线)2011-2012年陕西宁强天津中学高二下学期期中考试化学试卷(已下线)2011-2012学年吉林省汪清六中高二下学期期中考试化学试卷(已下线)2012--2013学年新疆乌鲁木齐市一中高二下学期期中考试化学试卷(平行班)(已下线)2012-2013学年四川省昭觉中学高二10月月考化学试卷(已下线)2013届新疆乌鲁木齐市一中高二第二学期期中考试化学试卷(已下线)2014-2015学年四川省成都外国语学校高二上学期期中化学试卷2014-2015辽宁省朝阳区三校高二下学期第一次阶段性检测化学试卷2014-2015吉林省吉林市第五十五中学高二下学期期中考试化学试卷2015-2016学年四川省雅安市天全中学高二9月月考化学试卷2015-2016学年四川省雅安天全中学高二上学期11月月考化学试卷2015-2016学年宁夏吴忠中学高二下开学考试化学试卷2015-2016学年吉林省吉林五十五中高二下3月月考化学试卷2015-2016学年陕西西藏民族学院附中高二4月月考化学卷2015-2016学年广东汕头金山中学高二下第十周练化学卷辽宁省实验中学分校2016-2017学年高二6月月考化学试题甘肃省兰州第一中学2017-2018学年高二下学期第一次月考化学试题贵州省息烽县一中2018-2019学年高二上学期期中考试化学试题贵州省遵义市正安县第一中学2018-2019学年高二上学期期中考试化学试题贵州省习水县一中2018-2019学年高二上学期12月份月考化学试题【全国百强校】山西省平遥中学2018-2019学年高二下学期第三次月考化学试题第1章 原子结构——B拓展区综合拓展(鲁科版选修3)安微蚌埠二中2019-2020学年高二4月检测化学试题黑龙江省海林市朝鲜族中学2019-2020学年高二下学期期中线上考试化学试题吉林省通化市通化县综合高级中学2019-2020学年高二下学期期中考试化学试题辽宁省六校协作体2019-2020学年高二下学期期中考试化学试卷高二选择性必修2(人教版2019)第一章 原子结构与性质 第二节 原子结构与元素的性质 课时2 元素周期律(已下线)第一单元 原子结构(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)(已下线)1.3.2 元素的电负性及其变化规律-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)福建省莆田第二十五中学2020-2021学年高二下学期第一次月考化学试题吉林省长春市第二十九中学2020-2021学年高二下学期期中考试化学试题宁夏海原第一中学2020-2021学年高二下学期期中考试化学试题宁夏青铜峡市高级中学2021-2022学年高二上学期期末考试化学试题吉林油田第十一中学2021-2022学年高二上学期期末考试化学试题四川省达州市第一中学校2022-2023学年高二上学期10月月考化学试题安徽省阜阳第一中学2022-2023学年高二下学期第一次月考化学试题1.3.2元素的电离能、电负性及其变化规律(课后)-鲁科版选择性必修2
名校
解题方法
7 . 在照相底片的定影过程中,未曝光的溴化银(AgBr)常用硫代硫酸钠(Na2S2O3)溶解,反应生成Na3[Ag(S2O3)2];在废定影液中加入Na2S使Na3[Ag(S2O3)2]中的银转化为Ag2S,并使定影液再生。将Ag2S在高温下转化为Ag,就达到了回收银的目的。
(1)铜、银、铬在元素周期表均为过渡金属元素,其中基态铬原子的价电子排布式为______ 。
(2)Na、O、S简单离子半径由大到小的顺序为___________ (用简单离子符号表示离子半径)。
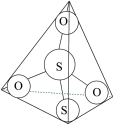
(3)S2O32-离子结构如图1所示,其中心硫原子的杂化轨道类型为________ 。
(4)Na3[Ag(S2O3)2]中存在的作用力有_____________ 。
A.离子键 B.共价键 C.范德华力 D.金属键 E.配位键
(5)在空气中灼烧Ag2S生成Ag和SO2,SO2分子空间构型为____________________ ;与SO3相比,____________ 的键角更大,原因是________________________________ 。
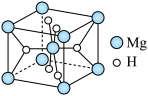
(6)如图是金属氢化物储氢材料,其晶胞如图所示,其化学式为____________________ ,已知该晶体的密度为ρg/cm3,则该晶胞的体积为_________ cm3(用含ρ、NA的代数式表示)。
(1)铜、银、铬在元素周期表均为过渡金属元素,其中基态铬原子的价电子排布式为
(2)Na、O、S简单离子半径由大到小的顺序为

(3)S2O32-离子结构如图1所示,其中心硫原子的杂化轨道类型为
(4)Na3[Ag(S2O3)2]中存在的作用力有
A.离子键 B.共价键 C.范德华力 D.金属键 E.配位键
(5)在空气中灼烧Ag2S生成Ag和SO2,SO2分子空间构型为

(6)如图是金属氢化物储氢材料,其晶胞如图所示,其化学式为
您最近一年使用:0次
8 . 氮气可以作食品包装、灯泡等的填充气,也是合成纤维、合成橡胶的重要原料。实验室制备氮气的反应式:NH4Cl+NaNO2 NaCl+N2↑+2H2O。下列说法正确的是( )
NaCl+N2↑+2H2O。下列说法正确的是( )
 NaCl+N2↑+2H2O。下列说法正确的是( )
NaCl+N2↑+2H2O。下列说法正确的是( )| A.元素的电负性:N>O>H |
B.氮气分子的电子式: |
C.钠电离最外层一个电子所需要的能量:①>②  |
| D.水中的氢键可以表示为:O—H…O,其中H…O之间的距离即为该氢键的键长 |
您最近一年使用:0次
2019-11-21更新
|
849次组卷
|
6卷引用:湖北省荆门市龙泉中学2021届高三上学期期中考试化学试题
9 . 铜、镁、金等的相关物质在生产生活中具有重要的作用。回答下列问题:
(1)铜元素在周期表中的位置是___________ ,基态铜原子中,核外电子占据最高能层的符号是___________ ,占据该最高能层的电子数为___________ 。
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、 Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于___________ (填“晶体”或“非晶体”)
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,lmol(SCN)2分子中含有σ键的数目为___________ 。(SCN)2对应的酸有硫氰酸(H-S-C≡N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是____________________________________________ 。
(4)铜与金形成的金属互化物的晶胞结构如图1所示,其晶胞边长为anm,该金属互化物的密度为___________ (用含a、NA的代数式表示)g·cm-3。

(6)某金属晶体中原子的堆积方式为六方最密堆积如图2所示,晶胞可用图3表示。已知该金属的原子半径为acm,该金属晶胞的高为bcm:若以晶胞中A点原子为原点建立空间直角坐标系o-xyz,则A点原子的坐标为(0,0,0),C点原子的坐标为(2a,0,0),D点原子的坐标为(0,0,b),则B点原子的坐标为______________________ 。
(1)铜元素在周期表中的位置是
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、 Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,lmol(SCN)2分子中含有σ键的数目为
(4)铜与金形成的金属互化物的晶胞结构如图1所示,其晶胞边长为anm,该金属互化物的密度为

(6)某金属晶体中原子的堆积方式为六方最密堆积如图2所示,晶胞可用图3表示。已知该金属的原子半径为acm,该金属晶胞的高为bcm:若以晶胞中A点原子为原点建立空间直角坐标系o-xyz,则A点原子的坐标为(0,0,0),C点原子的坐标为(2a,0,0),D点原子的坐标为(0,0,b),则B点原子的坐标为
您最近一年使用:0次
2019-02-13更新
|
459次组卷
|
3卷引用:【市级联考】湖北省荆门市2019届高三上学期元月调研考试理科综合化学试题
【市级联考】湖北省荆门市2019届高三上学期元月调研考试理科综合化学试题2020届高三化学二轮选修大题必练— —— 物质结构与性质(已下线)专题6.4 物质结构与性质(选考)(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升
名校
10 . 下图是元素周期表的一部分,已知a、b、c、d、e、f、g都是周期表中的前四周期元素,它们在周期表中的位置如图所示。
试回答下列问题:
(l)f元素基态原子的价电子排布式为______________ 。
(2)a、b、c的第一电离能由大到小的顺序______________ (用元素符号表示)。
(3)与b元素单质分子互为等电子体的阴离子为______________ 。
(4)下图为a元素某种氧化物的晶胞,其分子中心原子采用_____ 杂化,每个分子周围有___ 个分子与之距离相等且最近。若晶胞棱长为x pm,则该晶体密度的表达式为________ g•cm-3。
(5)g元素的最简单氢化物分子的空间构型为______ ,其沸点比b元素最简单的氢化物_______ (填 “高” 或“低”),其原因是______________________________ 。
(6)向CuSO4溶液中滴加入b元素最简单氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,加入乙醇析出深蓝色晶体的化学式为______________________ 。
(7)已知b的电负性大于氯,则bC13水解反应方程式为______________________________ 。
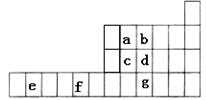
试回答下列问题:
(l)f元素基态原子的价电子排布式为
(2)a、b、c的第一电离能由大到小的顺序
(3)与b元素单质分子互为等电子体的阴离子为
(4)下图为a元素某种氧化物的晶胞,其分子中心原子采用

(5)g元素的最简单氢化物分子的空间构型为
(6)向CuSO4溶液中滴加入b元素最简单氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,加入乙醇析出深蓝色晶体的化学式为
(7)已知b的电负性大于氯,则bC13水解反应方程式为
您最近一年使用:0次



