名校
1 . 下表显示了元素周期表中的一部分。
请回答下列问题。
(1)硫元素的原子序数是_______ 。
(2)氟元素的原子结构示意图为_______ (填写字母)。
A.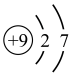 B.
B.
(3)镁元素在元素周期表的第_______ (填“二”或“三”)周期第_______ (填“ⅡA”或“ⅢA”)族。
(4)已知同主族元素从上到下原子半径逐渐增大,原子半径大小:H_______ (填“<”或“>”)Na。
(5)雷雨天闪电时空气中有O3生成,O2转化为O3是_______ (填“物理变化”或“化学变化”)。
(6)SiO2可用于生产光导纤维,SiO2中硅元素的化合价为_______ 。
(7)海水中的重要元素——钠和氯,形成生活中常见调味品的化学式为_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 第一周期 | 1 H 氢 | 2 He 氦 | ||||||
| 第二周期 | 3 Li 锂 | 4 Be 镀 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
| 第三周期1 | 1 Na 钠 | 12 Mg 镁 | 33 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 C 氯 | 18 Ar 氩 |
(1)硫元素的原子序数是
(2)氟元素的原子结构示意图为
A.
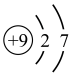 B.
B.
(3)镁元素在元素周期表的第
(4)已知同主族元素从上到下原子半径逐渐增大,原子半径大小:H
(5)雷雨天闪电时空气中有O3生成,O2转化为O3是
(6)SiO2可用于生产光导纤维,SiO2中硅元素的化合价为
(7)海水中的重要元素——钠和氯,形成生活中常见调味品的化学式为
您最近一年使用:0次
2023-05-11更新
|
181次组卷
|
2卷引用:云南省蒙自市第一高级中学2022-2023学年高一下学期5月期中考试化学试题
2 . 元素周期表中锑元素的数据如图。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第___________ 周期,第___________ 族。
(2)基态锑原子中有___________ 个未成对电子,这些未成对电子具有___________ (填“相同”或“不同”)的自旋状态。
(3)基态锑原子的5s轨道形状为___________ 形,该原子最外层电子占有___________ 个轨道。
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb___________ Bi;原子半径Sb___________ Bi (填“>”或“<”)。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第
(2)基态锑原子中有
(3)基态锑原子的5s轨道形状为
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb
您最近一年使用:0次
名校
3 .  是高效、广谱、绿色的消毒剂,回答下列问题。
是高效、广谱、绿色的消毒剂,回答下列问题。
(1)氯在元素周期表中的位置是___________ ,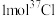 的中子数为
的中子数为___________ 。
(2)下列能判断Cl和O两种元素非金属性强弱的是___________ (填序号)。
a.原子得电子能力
b.与金属钠反应得电子的数目
c.最简单气态氢化物的稳定性
d.单质的沸点
(3)生产生活中含氯物质的排放会加快臭氧层的破坏。该过程的机理如图,总反应化学方程式为___________ 。

(4)化工、冶金行业的废水中存在 ,可用
,可用 气体将其转化为两种无毒气体
气体将其转化为两种无毒气体
① 的电子式为
的电子式为___________ 。
②该反应的离子方程式为___________ 。
(5)X、Y、Z、W四种短周期元素在周期表中的位置关系如图,Y和Z的核外电子数之和为22。将少量X的最高价氧化物通入到硅酸钠溶液中实现现象是___________ ,反应的离子方程式为___________ 。
 是高效、广谱、绿色的消毒剂,回答下列问题。
是高效、广谱、绿色的消毒剂,回答下列问题。(1)氯在元素周期表中的位置是
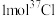 的中子数为
的中子数为(2)下列能判断Cl和O两种元素非金属性强弱的是
a.原子得电子能力
b.与金属钠反应得电子的数目
c.最简单气态氢化物的稳定性
d.单质的沸点
(3)生产生活中含氯物质的排放会加快臭氧层的破坏。该过程的机理如图,总反应化学方程式为

(4)化工、冶金行业的废水中存在
 ,可用
,可用 气体将其转化为两种无毒气体
气体将其转化为两种无毒气体①
 的电子式为
的电子式为②该反应的离子方程式为
(5)X、Y、Z、W四种短周期元素在周期表中的位置关系如图,Y和Z的核外电子数之和为22。将少量X的最高价氧化物通入到硅酸钠溶液中实现现象是
| X | Y | |
| Z | W |
您最近一年使用:0次
名校
解题方法
4 . 2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。
(1)In在周期表中的位置是______ 。
(2)In的最高价氧化物对应的水化物的碱性______ Ba(OH)2的碱性(填“>”或“<”)。
(3)硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。Se原子电子式可表示为______ 。
(4)下列说法合理的是______ 。
a.SeO2既有氧化性又有还原性 b.热稳定性:H2Se<HCl<H2S
c.酸性:H2SeO4<HBrO4<HClO4 d.Se比S更易与氢气反应
(1)In在周期表中的位置是
(2)In的最高价氧化物对应的水化物的碱性
(3)硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。Se原子电子式可表示为
(4)下列说法合理的是
a.SeO2既有氧化性又有还原性 b.热稳定性:H2Se<HCl<H2S
c.酸性:H2SeO4<HBrO4<HClO4 d.Se比S更易与氢气反应
您最近一年使用:0次
解题方法
5 . 按要求回答下列问题。
(1)写出漂白粉有效成分的化学式___________ 。
(2)某元素的一种核素可用于文物的年代测定,写出该元素在周期表中的位置___________ 。
(3)写出稀盐酸与石灰石反应的离子方程式___________ 。
(4)写出红热的铁与水蒸气反应的化学方程式___________ 。
(1)写出漂白粉有效成分的化学式
(2)某元素的一种核素可用于文物的年代测定,写出该元素在周期表中的位置
(3)写出稀盐酸与石灰石反应的离子方程式
(4)写出红热的铁与水蒸气反应的化学方程式
您最近一年使用:0次
名校
6 . 元素周期表体现了元素“位-构-性”的关系,下图是元素周期表的一部分,回答下列问题:
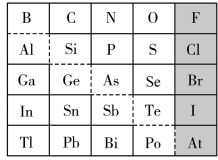
(1)Ga元素的原子结构示意图如图所示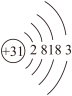 ,则其在元素周期表中的位置为
,则其在元素周期表中的位置为___________ 。
(2)Ge元素位于中金属元素和非金属元素的分界处,其最高正价为___________ ,可作___________ 材料使用;Bi元素的最高价氧化物为___________ (填化学式,下同);I元素的最高价氧化物对应的水化物为___________ 。
(3)以上元素中,失电子能力最强的元素是___________ ,非金属性最强的元素是___________ 。
(4)根据元素周期律等有关知识,推断:
①阴影部分元素对应的氢化物中最稳定的是___________ 。
② 、
、 、
、 、
、 ,四种离子半径由大到小的顺序:
,四种离子半径由大到小的顺序:___________ (用离子符号排序)。
③ 、
、 、
、 的酸性由强到弱的顺序:
的酸性由强到弱的顺序:___________ 。

(1)Ga元素的原子结构示意图如图所示
 ,则其在元素周期表中的位置为
,则其在元素周期表中的位置为(2)Ge元素位于中金属元素和非金属元素的分界处,其最高正价为
(3)以上元素中,失电子能力最强的元素是
(4)根据元素周期律等有关知识,推断:
①阴影部分元素对应的氢化物中最稳定的是
②
 、
、 、
、 、
、 ,四种离子半径由大到小的顺序:
,四种离子半径由大到小的顺序:③
 、
、 、
、 的酸性由强到弱的顺序:
的酸性由强到弱的顺序:
您最近一年使用:0次
名校
解题方法
7 . 根据所学知识,回答下列问题:
(1)写出C元素在元素周期表中的位置:___________ ;
(2)写出C与浓硫酸反应的化学方程式:___________ ;
(3)将胆矾晶体投入浓硫酸中,可观察到___________ ,体现了浓硫酸的___________ 性;
(4)除下列气体中的杂质所需要的试剂,括号内为杂质: (HCl)
(HCl)___________ ;NO( )
)___________
(1)写出C元素在元素周期表中的位置:
(2)写出C与浓硫酸反应的化学方程式:
(3)将胆矾晶体投入浓硫酸中,可观察到
(4)除下列气体中的杂质所需要的试剂,括号内为杂质:
 (HCl)
(HCl) )
)
您最近一年使用:0次
23-24高二上·浙江杭州·期末
8 . 氧(O)、硫(S)、硒、碲(Te)、钋(Po)、鉝(Lv)为元素周期表中原子序数依次增大的同主族元素。回答下列问题:
(1)硒_______ (填元素符号);鉝(Lv)_______ (填原子序数);
(2)碲有多种同位素原子,其中的核素是128 Te,它的中子数为_______ ;
(3)还原性:H2O_______ H2S (填">"或"<")
(4)氧常见的氢化物有两种,双氧水(H2O2)和水。双氧水在实验室和实际生产生活都有重要的作用。
①写出H2O2的电子式:_______ 。
②金属Al加到双氧水与NaOH的混合溶液中,金属Al溶解,写出反应的离子方程式_______ ;
③S2Cl2有类似于H2O2的性质,该物质遇水不稳定,生成一种黄色沉淀和无色有刺激性气味的气体,还得到一种强酸溶液,试写出该过程的反应方程式_______ ;
④实验室制氧气有多种方法,下列反应可以用来实验室制氧气的是_______ 。
A.氯酸钾加少量高锰酸钾受热分解
B.双氧水加二氧化锰
C.过氧化钠加水
D.过氧化钠中通二氧化碳
E.次氯酸受热分解
(1)硒
(2)碲有多种同位素原子,其中的核素是128 Te,它的中子数为
(3)还原性:H2O
(4)氧常见的氢化物有两种,双氧水(H2O2)和水。双氧水在实验室和实际生产生活都有重要的作用。
①写出H2O2的电子式:
②金属Al加到双氧水与NaOH的混合溶液中,金属Al溶解,写出反应的离子方程式
③S2Cl2有类似于H2O2的性质,该物质遇水不稳定,生成一种黄色沉淀和无色有刺激性气味的气体,还得到一种强酸溶液,试写出该过程的反应方程式
④实验室制氧气有多种方法,下列反应可以用来实验室制氧气的是
A.氯酸钾加少量高锰酸钾受热分解
B.双氧水加二氧化锰
C.过氧化钠加水
D.过氧化钠中通二氧化碳
E.次氯酸受热分解
您最近一年使用:0次
23-24高二上·浙江·期末
解题方法
9 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图,汞在第_______ 周期。

(2)硒(Se)与硫位于同主族,均是生命必需元素。下列推断不正确的是_______ 。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是75As,它的中子数为_______ 。
②已知NH4Cl与PH4I的性质相似,则对PH4I性质的推测不正确的是_______ (填序号)。
a.含有离子键和共价键 b.能与NaOH溶液反应
c.与NH4Cl加热充分分解产物的种类完全一样
③下列关于第VA族元素及其化合物的说法不正确的是_______ (填字母)。
a.热稳定性:NH3>PH3
b.酸性:HNO3>H3AsO4
c. As的氧化物的水化物是强碱
d.形成的简单离子半径随着原子序数递增而增大
(1)据汞的原子结构示意图,汞在第

(2)硒(Se)与硫位于同主族,均是生命必需元素。下列推断不正确的是
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是75As,它的中子数为
②已知NH4Cl与PH4I的性质相似,则对PH4I性质的推测不正确的是
a.含有离子键和共价键 b.能与NaOH溶液反应
c.与NH4Cl加热充分分解产物的种类完全一样
③下列关于第VA族元素及其化合物的说法不正确的是
a.热稳定性:NH3>PH3
b.酸性:HNO3>H3AsO4
c. As的氧化物的水化物是强碱
d.形成的简单离子半径随着原子序数递增而增大
您最近一年使用:0次
10 . 回答下列问题:
(1)第四周期中,未成对电子数最多的元素是_______ 。(填名称)
(2)它位于第_______ 族。
(3)核外电子排布式是_______ 。
(4)它有_______ 个能层,_______ 个能级,_______ 种运动状态不同的电子。
(5)价电子排布图_______ 。
(6)属于_______ 区。
(1)第四周期中,未成对电子数最多的元素是
(2)它位于第
(3)核外电子排布式是
(4)它有
(5)价电子排布图
(6)属于
您最近一年使用:0次



