解题方法
1 . 下表是元素周期表的一部分,根据表中给出的10种元素,按要求使用化学用语填空作答:
(1)地壳中含量最高的元素是_______ (填元素符号,下同);金属性最强的元素是_______ ;单质的化学性质最不活泼的元素是_______ ;气体单质有颜色的元素_______ ;可运输浓硫酸的金属元素是_______ 。
(2)最高价氧化物对应水化物酸性最强的是_______ ,碱性最强的是_______ (填化合物化学式);最高价氧化物不溶于水,但既溶于稀硫酸又溶于氢氧化钠溶液的是_______ (填化合物化学式);
(3)第三周期中两种金属元素的最高价氧化物对应的水化物相互反应的化学方程式为:_______ ,氢氧化铝治疗胃酸分泌过多的离子方程式:_______ 。
 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | H | |||||||
| 2 | C | N | O | Ne | ||||
| 3 | Na | Al | P | S | Cl |
(2)最高价氧化物对应水化物酸性最强的是
(3)第三周期中两种金属元素的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近一年使用:0次
22-23高一上·全国·课时练习
2 . 原子结构特点(F→I)
(1)相似性:最外层电子数均为_______ 。
(2)递变性:电子层数逐渐_______ ,原子半径逐渐_______ 。
(1)相似性:最外层电子数均为
(2)递变性:电子层数逐渐
您最近一年使用:0次
解题方法
3 . 按要求完成下列问题。
(1)硒(Se)是人体必需的微量元素,与O为同一主族元素,Se原子比O原子多两个电子层,则Se的原子序数为____ ,其最高价氧化物对应的水化物化学式为____ 。
(2)X射线衍射法可以测定某些分子结构,NH3分子结构为_____ 。
(3)水在液态时,几个水分子可以形成缔合水分子(H2O)n的原因是水分子之间存在____ 。
(4)漂白粉(有效成分Ca(ClO)2)与空气中CO2和水蒸气反应的化学方程式:____ 。
(5)完成氧化还原反应的离子方程式:____ 。
Cr2O +Fe2++_____=Cr3++Fe3++____
+Fe2++_____=Cr3++Fe3++____
(6)一定条件下金属钠和H2反应生成甲,甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。化合物甲和NaAlH4都是重要的还原剂。将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2。
①甲的化学式____ 。
②甲与AlCl3反应得到NaAlH4的化学方程式:____ 。
③NaAlH4与水发生氧化还原反应的化学方程式:____ 。
④甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式:____ 。
(1)硒(Se)是人体必需的微量元素,与O为同一主族元素,Se原子比O原子多两个电子层,则Se的原子序数为
(2)X射线衍射法可以测定某些分子结构,NH3分子结构为
(3)水在液态时,几个水分子可以形成缔合水分子(H2O)n的原因是水分子之间存在
(4)漂白粉(有效成分Ca(ClO)2)与空气中CO2和水蒸气反应的化学方程式:
(5)完成氧化还原反应的离子方程式:
Cr2O
 +Fe2++_____=Cr3++Fe3++____
+Fe2++_____=Cr3++Fe3++____(6)一定条件下金属钠和H2反应生成甲,甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。化合物甲和NaAlH4都是重要的还原剂。将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2。
①甲的化学式
②甲与AlCl3反应得到NaAlH4的化学方程式:
③NaAlH4与水发生氧化还原反应的化学方程式:
④甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式:
您最近一年使用:0次
2022-11-16更新
|
160次组卷
|
2卷引用:天津市部分区2022-2023学年高三上学期期中考试化学试题
名校
解题方法
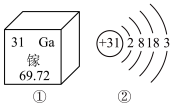
4 . 2019年是元素周期表年,镓是门捷列夫曾经预言的金属(类铝)。下图①是镓元素在元素周期表中的部分信息,②是镓原子的结构示意图。请回答:
A.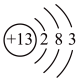 B.
B. 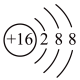 C.
C.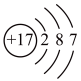 D.
D.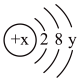
(1)镓原子的核电荷数为_______ ,镓元素的相对原子质量为_______ 。自然界中的镓共有两种稳定的同位素,其中69Ga的丰度为64.0%,则另一种镓的同位素质量数为_______ 。
(2)A、B、C三种微粒所属元素与镓元素化学性质相似的是_______ (填元素符号);微粒B的电子式为_______ ,则镓离子与B形成的化合物为_______ (填化学式)。
(3)D为某微粒的结构示意图,已知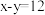 ,则x=
,则x=_______ ;写出C和D组成的化合物在水溶液中的电离方程式:_______ 。
(4)氮化镓(GaN)是第三代半导体材料,一般采用 与
与 在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为_______ 。

A.
 B.
B.  C.
C. D.
D.
(1)镓原子的核电荷数为
(2)A、B、C三种微粒所属元素与镓元素化学性质相似的是
(3)D为某微粒的结构示意图,已知
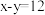 ,则x=
,则x=(4)氮化镓(GaN)是第三代半导体材料,一般采用
 与
与 在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
在一定条件下反应制得,同时得到另一种化合物,该反应的化学方程式为
您最近一年使用:0次
名校
5 . 前四周期的A、B、C、D、E、F六种元素,原子序数依次增大。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上有3个未成对的电子;C元素为最活泼的非金属元素;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
(1)E元素在周期表中位置为_______ ,E3+价电子轨道表示式为_______ 。
(2)F的元素符号为_______ ,B、C、F三种元素电负性由大到小的顺序为_______ (用元素符号表示),第一电离能D_______ (填“>”、“<”或“=”)Al。
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
(4)F元素可能的性质_______(填标号)。
 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。(1)E元素在周期表中位置为
(2)F的元素符号为
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是
(4)F元素可能的性质_______(填标号)。
| A.其单质可作半导体材料 |
| B.存在-3、+3、+5等多种化合价 |
| C.最高价氧化物对应的水化物是强酸 |
| D.单质还原性弱于磷单质 |
您最近一年使用:0次
2022-10-24更新
|
183次组卷
|
2卷引用:福建省永春美岭中学2021-2022学年高二下学期期中测试化学试题
6 . 下表为元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题。
(1)①~⑩中,最活泼的金属元素是_______ (写元素符号)
(2)①⑧的简单离子,其半径更大的是_______ (写离子符号)。
(3)⑧⑨的气态氢化物,更稳定的是_______ (填化学式)。
(4)元素的非金属性:⑥_______ ⑦(填“>”或“<”)。
(5)①~⑨的最高价氧化物的水化物中:酸性最强的物质是_______ (填化学式);碱性最强的是_______ (填化学式),该碱与⑤的最高价氧化物的水化物反应的离子方程式为_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑦ | ⑧ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑥ | ⑨ | |||
| 4 | ② | ④ |
(2)①⑧的简单离子,其半径更大的是
(3)⑧⑨的气态氢化物,更稳定的是
(4)元素的非金属性:⑥
(5)①~⑨的最高价氧化物的水化物中:酸性最强的物质是
您最近一年使用:0次
7 . 元素周期表的一部分,按要求完成各小题。
(1)化学性质最不活泼的元素____ ,(填元素符号,下同)非金属性最强的元素是____ ,金属性最强的单质与水反应的离子方程式为____ 。
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是____ 。
(3)①③⑤三种元素的原子半径由大到小的顺序为____ 。
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是____ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ⑥ | ⑦ | ⑪ | |||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
(1)化学性质最不活泼的元素
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是
(3)①③⑤三种元素的原子半径由大到小的顺序为
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是
您最近一年使用:0次
解题方法
8 . 如图是元素周期表的一部分,回答下列问题:
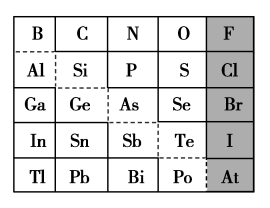
(1)元素Ga在元素周期表中的位置为:第_______ 周期第_______ 族。
(2)Sn的最高正价为_______ ,Cl的最高价氧化物对应的水化物的化学式为_______ ,Bi的最高价氧化物的化学式为_______ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是_______ (填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4_______ H2SeO4(填“>”或“<”下同)。
③氢化物的还原性:H2O_______ H2S。

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
您最近一年使用:0次
解题方法
9 . 根据如图所示,回答下列问题:

(1)硫原子的质子数为_______ ;
(2)硫原子属于_______ (选填“金属”“非金属”或“稀有气体”)元素;
(3)硫原子在化学反应中容易_______ (选填“得到”或“失去”)电子。

(1)硫原子的质子数为
(2)硫原子属于
(3)硫原子在化学反应中容易
您最近一年使用:0次
解题方法
10 . 下表是元素周期表的一部分,请回答:
(1)钠元素在元素周期表中的位置是___________ ;
(2)N、O、F三种元素中,非金属性最强的是___________ (填元素符号);
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为___________ ;
(4)碘与氯是同主族元素。下面关于碘的推断错误的是___________ (选填字母);
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ||||||||
| 2 | N | O | F | |||||
| 3 | Na | Si | Cl |
(1)钠元素在元素周期表中的位置是
(2)N、O、F三种元素中,非金属性最强的是
(3)由上表中两种元素组成的化合物是光导纤维的主要原料,该化合物的化学式为
(4)碘与氯是同主族元素。下面关于碘的推断错误的是
a.常温下,碘单质为气态 b.最高正化合价为+7 c.Cl2通入淀粉KI溶液中出现蓝色
(5)氮的氢化物和氯的氢化物反应生成一种铵盐,常用作氮肥,该反应的化学方程式为
您最近一年使用:0次



