1 . 元素X、Y、Z、M与Li同周期,其组成的新型化合物A结构如下图所示,其中Y原子核外的 轨道与
轨道与 轨道上的电子数目相等,下列叙述正确的是
轨道上的电子数目相等,下列叙述正确的是
 轨道与
轨道与 轨道上的电子数目相等,下列叙述正确的是
轨道上的电子数目相等,下列叙述正确的是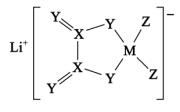
A.X、Y、Z的简单氢化物的稳定性: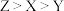 |
B.简单离子半径大小关系: |
C.第一电离能大小顺序为 |
D.化合物 中环上原子均采用 中环上原子均采用 杂化 杂化 |
您最近一年使用:0次
名校
解题方法
2 . 安全气囊在汽车部件中非常重要,它的工作原理是汽车碰撞时传感器产生的电流触发气体发生如下反应:
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为___________ ;某元素的最外层电子数是电子层数的3倍,则其简单离子的电子式为___________ ,能量最高的电子为___________ 层上的电子。反应中涉及的主族元素的简单离子半径从大到小的顺序是___________ (用离子符号表示)。
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是___________ ,其水溶液显___________ 性(填“酸”、“碱”或“中”),原因是___________ (用离子方程式表示)。
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有___________ 个氮原子(保留三个有效数字);已知获得上述N2需要NaN3130g,反应生成N2的产率是___________ %(产率= ×100%)
×100%)
2NaN3(s)=3N2(g)+2Na(s)
6Na(s)+Fe2O3(s)=3Na2O(s)+2Fe(s)
Na2O(s)+2CO2(g)+H2O(g)=2NaHCO3(s)
(1)上述反应所涉及元素中,某元素原子失去一个电子即可形成8电子稳定结构,该元素原子结构示意图为
(2)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐晶体中含有的化学键类型是
(3)汽车行驶过程中,能保护司机不受伤害的气囊需要0.065m3N2(S.T.P),其中约含有
 ×100%)
×100%)
您最近一年使用:0次
名校
解题方法
3 . N、P及其化合物在工业生产中起着重要的作用。回答下列问题:
(1)由磷原子核形成的三种微粒:a.([Ne]3s23p3)、b.([Ne]3s23p2)、c.([Ne]3s23p24s1),半径由大到小的顺序为___________ (填标号,下同);再失去一个电子所需最低能量由大到小的顺序为___________ 。
(2)已知HSCN的结构有两种,这两种分子结构中除氢外各原子均满足八电子稳定结构(无配位键),请画出沸点高的分子的结构式___________ 。
(3)杂环化合物咪唑结构如图,其分子中的大π键可表示为 ,则其结合质子能力更强的氮原子是
,则其结合质子能力更强的氮原子是___________ (填“①”或“②”),其原因是___________ 。

(4)氮、铜形成的一种化合物,为立方晶系晶体,晶胞参数为apm,沿体对角线投影如下图所示。已知该晶胞中原子的分数坐标如下:Cu:(0,0, );(0,
);(0, ,0);(
,0);( ,0,0);N:(0,0,0),其中与Cu原子等距且最近的Cu原子有
,0,0);N:(0,0,0),其中与Cu原子等距且最近的Cu原子有___________ 个,则该化合物的化学式为___________ 。

(5)PCl5是一种白色晶体,其晶胞如图所示。该晶体熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子。

①写出PCl5熔融时的电离方程式___________ 。
②若晶胞参数为anm,则晶体的密度为___________  (列出计算式)。
(列出计算式)。
(1)由磷原子核形成的三种微粒:a.([Ne]3s23p3)、b.([Ne]3s23p2)、c.([Ne]3s23p24s1),半径由大到小的顺序为
(2)已知HSCN的结构有两种,这两种分子结构中除氢外各原子均满足八电子稳定结构(无配位键),请画出沸点高的分子的结构式
(3)杂环化合物咪唑结构如图,其分子中的大π键可表示为
 ,则其结合质子能力更强的氮原子是
,则其结合质子能力更强的氮原子是
(4)氮、铜形成的一种化合物,为立方晶系晶体,晶胞参数为apm,沿体对角线投影如下图所示。已知该晶胞中原子的分数坐标如下:Cu:(0,0,
 );(0,
);(0, ,0);(
,0);( ,0,0);N:(0,0,0),其中与Cu原子等距且最近的Cu原子有
,0,0);N:(0,0,0),其中与Cu原子等距且最近的Cu原子有
(5)PCl5是一种白色晶体,其晶胞如图所示。该晶体熔融时形成一种能导电的液体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子。

①写出PCl5熔融时的电离方程式
②若晶胞参数为anm,则晶体的密度为
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2024-01-22更新
|
673次组卷
|
2卷引用:山东省高中名校2023-2024学年高三上学期12月统一调研考试化学试题
名校
4 . 有机增塑剂 和
和 的质子数均为32,其相对分子质量相差5;X、W、R三种元素同周期,X原子的最外层电子数为R电子总数的一半。下列说法正确的是
的质子数均为32,其相对分子质量相差5;X、W、R三种元素同周期,X原子的最外层电子数为R电子总数的一半。下列说法正确的是
 和
和 的质子数均为32,其相对分子质量相差5;X、W、R三种元素同周期,X原子的最外层电子数为R电子总数的一半。下列说法正确的是
的质子数均为32,其相对分子质量相差5;X、W、R三种元素同周期,X原子的最外层电子数为R电子总数的一半。下列说法正确的是| A.Y、Z互为同素异形体 | B.元素的第一电离能:W>R |
| C.原子半径:R>X | D.常温常压下,X、W的单质为固体 |
您最近一年使用:0次
2023-12-16更新
|
671次组卷
|
2卷引用:山东省实验中学2023-2024学年高三上学期12月月考化学试题
5 . 前四周期元素X、Y、Z、W的原子序数依次增大,X原子中有6个运动状态不同的电子,Y是地壳中含量最多的元素,基态Z原子K、L层上的电子总数是 原子轨道上电子数的两倍,基态W原子中有6个未成对电子。下列说法错误的是
原子轨道上电子数的两倍,基态W原子中有6个未成对电子。下列说法错误的是
 原子轨道上电子数的两倍,基态W原子中有6个未成对电子。下列说法错误的是
原子轨道上电子数的两倍,基态W原子中有6个未成对电子。下列说法错误的是A.电负性: ,原子半径: ,原子半径: | B.同周期中,元素Z的第一电离能最大 |
C.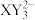 离子中存在 离子中存在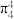 的离域π键 的离域π键 | D.在一定条件下,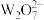 和 和 均具有强氧化性 均具有强氧化性 |
您最近一年使用:0次
解题方法
6 . 某化合物的结构如图所示,其中X、Y、Z、Q为原子序数依次增大的四种短周期元素,X是元素周期表中原子半径最小的元素,Q的最外层电子数是其内层电子数的3倍。下列说法错误的是
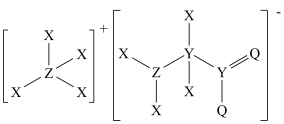

| A.四种元素中原子半径最大的是Y |
| B.Y、Z和Q三种元素的电负性逐渐减弱 |
| C.X和Q形成的化合物中可存在非极性键 |
| D.该化合物中Z、Y、Q均满足8电子稳定结构 |
您最近一年使用:0次
7 . Q、W、X、Y、Z为原子序数依次增大的不同主族短周期元素,只有W、X、Y同周期且相邻,W和X的原子序数之和等于Z的原子序数。下列说法正确的是
| A.简单离子半径:Z>X>Y |
| B.Q、W、X、Y形成的化合物一定是共价化合物 |
| C.一定条件下Y单质能够置换出X单质 |
| D.W和X的最高价氧化物对应的水化物均为强酸 |
您最近一年使用:0次
2023-12-03更新
|
244次组卷
|
2卷引用:2024届山东省临沂市高三11月教学质量检测考试 化学
8 . 化合物T是一种用于合成药物的重要试剂,其结构简式如图所示。已知X、Y、Z、M、N为原子序数依次增大的前四周期主族元素,Z、M位于同一主族,X、Y、N的最外层电子数之和等于Z的最外层电子数。下列有关叙述错误的是


A.简单离子半径: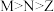 | B.简单氢化物稳定性: |
C.化合物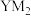 与 与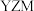 均为直线型分子 均为直线型分子 | D.化合物T中所有原子均符合8电子稳定结构 |
您最近一年使用:0次
9 . 常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为0.01 )的pH和原子半径、原子序数的关系如下图所示。下列说法错误的是
)的pH和原子半径、原子序数的关系如下图所示。下列说法错误的是
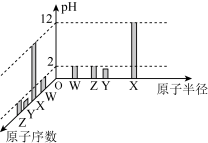
 )的pH和原子半径、原子序数的关系如下图所示。下列说法错误的是
)的pH和原子半径、原子序数的关系如下图所示。下列说法错误的是
| A.简单离子半径:Y>Z>W>X | B.单质的沸点:Y>Z |
| C.X与Y形成的化合物的水溶液呈酸性 | D. 可作为自来水的消毒剂 可作为自来水的消毒剂 |
您最近一年使用:0次
名校
解题方法
10 . 软包电池的关键组件结构如图所示。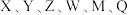 为原子序数依次增大的短周期元素,
为原子序数依次增大的短周期元素, 元素最外层电子数是次外层电子数的一半,
元素最外层电子数是次外层电子数的一半, 和
和 同主族。下列说法错误的是
同主族。下列说法错误的是

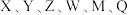 为原子序数依次增大的短周期元素,
为原子序数依次增大的短周期元素, 元素最外层电子数是次外层电子数的一半,
元素最外层电子数是次外层电子数的一半, 和
和 同主族。下列说法错误的是
同主族。下列说法错误的是
A.简单离子半径: |
B.简单氢化物的热稳定性: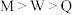 |
C.常温下 单质可以在水溶液中置换出 单质可以在水溶液中置换出 单质 单质 |
D. 为 为 形分子 形分子 |
您最近一年使用:0次



