解题方法
1 .  为一种重要的化工原料,其组成元素
为一种重要的化工原料,其组成元素  为原子序数依次增大的短周期主族元素,且
为原子序数依次增大的短周期主族元素,且  的一种核素常用于检测文物的年代,
的一种核素常用于检测文物的年代, 的最外层电子数是内层电子数的3倍,下列说法
的最外层电子数是内层电子数的3倍,下列说法错误 的是
 为一种重要的化工原料,其组成元素
为一种重要的化工原料,其组成元素  为原子序数依次增大的短周期主族元素,且
为原子序数依次增大的短周期主族元素,且  的一种核素常用于检测文物的年代,
的一种核素常用于检测文物的年代, 的最外层电子数是内层电子数的3倍,下列说法
的最外层电子数是内层电子数的3倍,下列说法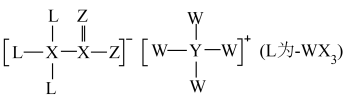
A.电负性: |
B.氢化物的沸点: |
C. 元素对应的单质不一定是非极性分子 元素对应的单质不一定是非极性分子 |
| D.由W、Y、Z三种元素组成的化合物一定抑制水的电离 |
您最近半年使用:0次
名校
解题方法
2 . 科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是
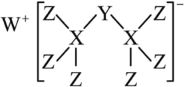
| A.WZ的水溶液呈碱性 |
B.元素非金属性的顺序为 |
| C.Y的最高价氧化物的水化物的晶体是分子晶体 |
| D.该新化合物中Y不满足8电子稳定结构 |
您最近半年使用:0次
解题方法
3 . 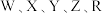 为短周期主族元素,原子序数依次增大。
为短周期主族元素,原子序数依次增大。 元素最外层电子数是次外层电子数的2倍;
元素最外层电子数是次外层电子数的2倍; 的阴离子和
的阴离子和 的阳离子与氖原子的电子层结构相同;常温下,
的阳离子与氖原子的电子层结构相同;常温下, 的单质是气体,
的单质是气体,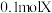 的气体与足量的氢气完全反应共有
的气体与足量的氢气完全反应共有 电子转移;
电子转移; 的单质在点燃时与
的单质在点燃时与 的单质充分反应,生成淡黄色固体,此淡黄色固体能与化合物
的单质充分反应,生成淡黄色固体,此淡黄色固体能与化合物 反应生成
反应生成 的单质;
的单质; 与
与 同族,
同族, 的气态氢化物能与其最高价含氧酸的浓溶液发生氧化还原反应。回答下列问题:
的气态氢化物能与其最高价含氧酸的浓溶液发生氧化还原反应。回答下列问题:
(1)在元素周期表中,W位于___________ 族,属于___________ 区。X、Y、R三种元素的简单离子的离子半径由小到大顺序为___________ (用离子符号表示)。
(2)X和Z的简单氢化物中,沸点更高的是___________ (填化学式),这是因为___________ 。
(3)Z元素在周期表的位置为___________ ,其非金属性比R弱,下列表述能证明这一事实的有___________ (填标号)。
A.常温下Z的单质和R的单质状态不同
B.R的简单氢化物比Z的简单氢化物稳定
C.一定条件下Z和R的单质都能与钠反应
D.Z的最高价含氧酸的酸性弱于R的最高价含氧酸
E.R的单质能与Z的简单氢化物反应生成Z的单质
(4)Z元素的低价氧化物与R单质的水溶液反应的离子方程式为___________ 。经测定 形成的氢化物
形成的氢化物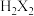 为二元弱酸,其酸性比碳酸弱,实验室常用稀硫酸处理
为二元弱酸,其酸性比碳酸弱,实验室常用稀硫酸处理 来制备
来制备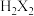 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
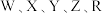 为短周期主族元素,原子序数依次增大。
为短周期主族元素,原子序数依次增大。 元素最外层电子数是次外层电子数的2倍;
元素最外层电子数是次外层电子数的2倍; 的阴离子和
的阴离子和 的阳离子与氖原子的电子层结构相同;常温下,
的阳离子与氖原子的电子层结构相同;常温下, 的单质是气体,
的单质是气体,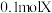 的气体与足量的氢气完全反应共有
的气体与足量的氢气完全反应共有 电子转移;
电子转移; 的单质在点燃时与
的单质在点燃时与 的单质充分反应,生成淡黄色固体,此淡黄色固体能与化合物
的单质充分反应,生成淡黄色固体,此淡黄色固体能与化合物 反应生成
反应生成 的单质;
的单质; 与
与 同族,
同族, 的气态氢化物能与其最高价含氧酸的浓溶液发生氧化还原反应。回答下列问题:
的气态氢化物能与其最高价含氧酸的浓溶液发生氧化还原反应。回答下列问题:(1)在元素周期表中,W位于
(2)X和Z的简单氢化物中,沸点更高的是
(3)Z元素在周期表的位置为
A.常温下Z的单质和R的单质状态不同
B.R的简单氢化物比Z的简单氢化物稳定
C.一定条件下Z和R的单质都能与钠反应
D.Z的最高价含氧酸的酸性弱于R的最高价含氧酸
E.R的单质能与Z的简单氢化物反应生成Z的单质
(4)Z元素的低价氧化物与R单质的水溶液反应的离子方程式为
 形成的氢化物
形成的氢化物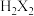 为二元弱酸,其酸性比碳酸弱,实验室常用稀硫酸处理
为二元弱酸,其酸性比碳酸弱,实验室常用稀硫酸处理 来制备
来制备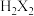 ,该反应的离子方程式为
,该反应的离子方程式为
您最近半年使用:0次
名校
4 . X、Y、Z、M、R、Q是短周期元素,其原子半径与主要化合价的关系如图所示。下列说法正确的是

| A.简单离子半径:M<R<Q |
| B.简单气态氢化物稳定性:Y<Z |
| C.R单质在空气中燃烧,只生成对应的氧化物 |
| D.X、Y、Z三种元素组成的化合物可能是离子化合物 |
您最近半年使用:0次
名校
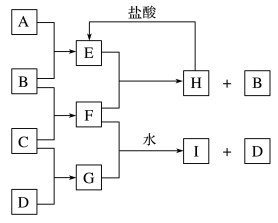
5 . A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组空气的成分。化合物F的焰色试验呈黄色。在G中,非金属元素与金属元素的原子个数比为1∶2,在一定条件下,各物质之间的相互转化关系如下图(图中部分产物未列出):
(1)A是___________ 。
(2)写出F和E反应的化学方程式___________ 。
(3)3.9克F与足量的E反应转移的电子数目为___________ 。
(4)在1L含1mol·L-1H的溶液中逐滴滴加1L0.75mol·L-1的 溶液生成标准状况下气体的体积是
溶液生成标准状况下气体的体积是___________ L(不考虑气体的溶解)
(5)F与G的水溶液反应生成I和D的离子方程式是___________ 。
(1)A是
(2)写出F和E反应的化学方程式
(3)3.9克F与足量的E反应转移的电子数目为
(4)在1L含1mol·L-1H的溶液中逐滴滴加1L0.75mol·L-1的
 溶液生成标准状况下气体的体积是
溶液生成标准状况下气体的体积是(5)F与G的水溶液反应生成I和D的离子方程式是
您最近半年使用:0次
名校
6 . 已知A、B、C、D、E、F、G、H是原子序数依次增大的短周期主族元素,已知A的某种原子核内没有中子,A和D,C和G分别为同一主族元素,B原子的最外层电子数比次外层多3,F的最高价氧化物的水化物既可以和强酸反应也可以和强碱溶液反应,G的单质常出现在火山口。
(1)C在元素周期表中的位置是_______ 。
(2)C、D分别形成的简单离子中,半径较大的是______ (填离子符号)。
(3)G和H的最高价氧化物的水化物酸性较强的是______ (填化学式)。
(4)由A、C、D形成的化合物中化学键的类型为_______ ,C、D形成摩尔质量为 的化合物的电子式为
的化合物的电子式为______ ,由A、B形成 化合物的结构式为
化合物的结构式为______ 。
(5)甲烷可与 组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式
组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式_______ 。
(6)D、F的最高价氧化物的水化物相互反应的离子方程式为_______ 。
(7)可用湿润的______ 试纸检验H对应单质,涉及反应的离子方程式为_______ 。
(8)由B、H形成的化合物分子中,B和H原子的最外层均达到8电子稳定结构,该化合物遇水可反应生成一种具有漂白性的化合物,写出反应的化学方程式:________ 。
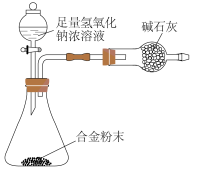
(9)E与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中E元素的含量。(装置中因空气质量引起的误差忽略不计)实验需要测定三个物理量:合金的质量m,反应前装置和药品的总质量a以及反应后装置和药品的总质量b,合金中E元素的质量分数是______ (用含m、a、b的式子表示)。
(1)C在元素周期表中的位置是
(2)C、D分别形成的简单离子中,半径较大的是
(3)G和H的最高价氧化物的水化物酸性较强的是
(4)由A、C、D形成的化合物中化学键的类型为
 的化合物的电子式为
的化合物的电子式为 化合物的结构式为
化合物的结构式为(5)甲烷可与
 组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式
组成燃料电池,写出用KOH溶液作电解质溶液时正极的电极反应式(6)D、F的最高价氧化物的水化物相互反应的离子方程式为
(7)可用湿润的
(8)由B、H形成的化合物分子中,B和H原子的最外层均达到8电子稳定结构,该化合物遇水可反应生成一种具有漂白性的化合物,写出反应的化学方程式:
(9)E与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中E元素的含量。(装置中因空气质量引起的误差忽略不计)实验需要测定三个物理量:合金的质量m,反应前装置和药品的总质量a以及反应后装置和药品的总质量b,合金中E元素的质量分数是
您最近半年使用:0次
7日内更新
|
95次组卷
|
2卷引用:福建省厦门双十中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
7 .  、
、 、
、 、
、 、
、 是五种短周期主族元素,
是五种短周期主族元素, 是空气中含量最多的物质,
是空气中含量最多的物质, 的最外层电子数是最内层电子数的一半,
的最外层电子数是最内层电子数的一半, 是地壳中含量最多的金属元素,
是地壳中含量最多的金属元素, 的最简单氢化物
的最简单氢化物 是一种有臭鸡蛋气味的气体,五种元素的原子序数和原子半径的关系如图所示。下列说法错误的是
是一种有臭鸡蛋气味的气体,五种元素的原子序数和原子半径的关系如图所示。下列说法错误的是
 、
、 、
、 、
、 、
、 是五种短周期主族元素,
是五种短周期主族元素, 是空气中含量最多的物质,
是空气中含量最多的物质, 的最外层电子数是最内层电子数的一半,
的最外层电子数是最内层电子数的一半, 是地壳中含量最多的金属元素,
是地壳中含量最多的金属元素, 的最简单氢化物
的最简单氢化物 是一种有臭鸡蛋气味的气体,五种元素的原子序数和原子半径的关系如图所示。下列说法错误的是
是一种有臭鸡蛋气味的气体,五种元素的原子序数和原子半径的关系如图所示。下列说法错误的是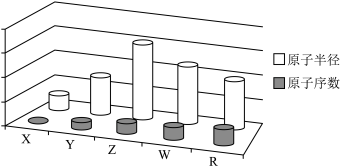
A.简单离子半径: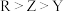 |
B. 、 、 、 、 三者的最高价氧化物对应的水化物能互相反应 三者的最高价氧化物对应的水化物能互相反应 |
C. 与 与 形成的一种化合物能使湿润的红色石蕊试纸变蓝 形成的一种化合物能使湿润的红色石蕊试纸变蓝 |
D. 、 、 、 、 能形成含有共价键的离子化合物 能形成含有共价键的离子化合物 |
您最近半年使用:0次
2024-04-21更新
|
93次组卷
|
3卷引用:江西省部分地区2023-2024学年高一下学期3月月考化学试题
名校
解题方法
8 . 短周期元素a、b、c、d的原子序数依次增大,在下列转化关系中,甲、乙、丙、丁、戊为上述四种元素组成的二元或三元化合物。其中A为d元素组成的单质,常温下乙为液体,丁物质常用于消毒、漂白。下列说法正确的是

| A.b元素位于周期表中IVA族 |
| B.b、c形成的化合物中阴、阳离子数目之比为1:1 |
| C.丙中既有离子键又有非极性键 |
D.a、b、d形成的有漂白性的化合物中,b的杂化方式是 |
您最近半年使用:0次
名校
9 . 甲是日常生活中是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟,D是食盐的主要成分(部分反应物和生成物及溶剂水已略去)。___________ ;甲在元素周期表的位置为___________ 。
(2)A的电子式为___________ 。
(3)实验室常用加热固体混合物制备B,其化学方程式为___________ 。
(4)物质B的催化氧化是工业制硝酸的基础,其化学方程式___________ 。
(5)丙在丁中点燃,其现象为___________ 。
(6)检验E溶液中阳离子的方法是___________ 。
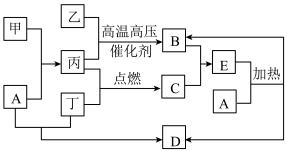
(2)A的电子式为
(3)实验室常用加热固体混合物制备B,其化学方程式为
(4)物质B的催化氧化是工业制硝酸的基础,其化学方程式
(5)丙在丁中点燃,其现象为
(6)检验E溶液中阳离子的方法是
您最近半年使用:0次
10 . 物质M可用作调味剂、乳化剂、抗氧化增效剂、吸湿剂、pH调节剂、增香剂、缓冲剂。其结构式如图所示,其组成元素X、Y、Z、Q为原子序数依次增大的短周期主族元素。下列说法正确的是

| A.第一电离能:Q<Y<X<Z |
| B.电负性:Q<Y<X<Z |
| C.元素Z与元素Q形成的化合物中一定含有非极性键 |
| D.由价电子排布式可知基态Y原子有4个单电子 |
您最近半年使用:0次



