1 . 下列化学用语正确的是
A.氮原子2py轨道的电子云图: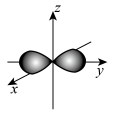 |
| B.基态As的简化电子排布式为:[Ar]4s24p3 |
| C.一定条件下,氯气可形成Cl2·8H2O的水合物晶体 |
| D.Na、Mg、Al三种元素第二电离能从大到小的顺序是Al>Mg>Na |
您最近半年使用:0次
名校
解题方法
2 . 第四周期的元素在工业、农业、科学技术以及人类生活等方面有重要作用。回答下列问题:
(1)钒(V)及其化合物广泛应用于工业催化、新材料等领域。
①周期表中铬位于钒旁边,基态铬原子的价层电子排布图为___________ 。
② 是一种常见的催化剂,在合成硫酸中起到重要作用,其结构式如图所示:则
是一种常见的催化剂,在合成硫酸中起到重要作用,其结构式如图所示:则 分子中σ键和π键数目之比为
分子中σ键和π键数目之比为___________ 。 溶解在NaOH溶液中,可得到钒酸钠(
溶解在NaOH溶液中,可得到钒酸钠(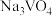 )。
)。 与
与 的空间构型相同,其中V原子的杂化方式为
的空间构型相同,其中V原子的杂化方式为___________ 。 作光催化剂可处理废水中的
作光催化剂可处理废水中的 ,则
,则 的电子式为
的电子式为___________ 。
② 是一种储氢材料。第一电离能介于B、N之间的第2周期元素有
是一种储氢材料。第一电离能介于B、N之间的第2周期元素有___________ 种。
(3)“玉兔二号”月球车是通过砷化镓(GaAs)太阳能电池提供能量进行工作的。第ⅤA族的As元素可以形成多种含氧酸,如 、
、 等,请预测:键角:
等,请预测:键角:
___________  (填“>”“<”或“=”)。基态砷原子的电子占据最高能级的电子云轮廓图为
(填“>”“<”或“=”)。基态砷原子的电子占据最高能级的电子云轮廓图为___________ 形。
(4) 常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测
常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测 是
是___________ 分子(填“极性”或“非极性”)。
(5)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态Ge原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Ge原子,其价电子自旋磁量子数的代数和为___________ 。
(1)钒(V)及其化合物广泛应用于工业催化、新材料等领域。
①周期表中铬位于钒旁边,基态铬原子的价层电子排布图为
②
 是一种常见的催化剂,在合成硫酸中起到重要作用,其结构式如图所示:则
是一种常见的催化剂,在合成硫酸中起到重要作用,其结构式如图所示:则 分子中σ键和π键数目之比为
分子中σ键和π键数目之比为 溶解在NaOH溶液中,可得到钒酸钠(
溶解在NaOH溶液中,可得到钒酸钠(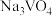 )。
)。 与
与 的空间构型相同,其中V原子的杂化方式为
的空间构型相同,其中V原子的杂化方式为
 作光催化剂可处理废水中的
作光催化剂可处理废水中的 ,则
,则 的电子式为
的电子式为②
 是一种储氢材料。第一电离能介于B、N之间的第2周期元素有
是一种储氢材料。第一电离能介于B、N之间的第2周期元素有(3)“玉兔二号”月球车是通过砷化镓(GaAs)太阳能电池提供能量进行工作的。第ⅤA族的As元素可以形成多种含氧酸,如
 、
、 等,请预测:键角:
等,请预测:键角:
 (填“>”“<”或“=”)。基态砷原子的电子占据最高能级的电子云轮廓图为
(填“>”“<”或“=”)。基态砷原子的电子占据最高能级的电子云轮廓图为(4)
 常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测
常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测 是
是(5)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态Ge原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Ge原子,其价电子自旋磁量子数的代数和为
您最近半年使用:0次
名校
解题方法
3 . 下列关于原子结构、原子轨道的说法正确的是
| A.M能层中有3s、3p、3d三个能级,共9个轨道,可容纳18种运动状态的电子 |
| B.在原子结构分层排布中,M层容纳电子数最多为18,最少为8 |
| C.s电子绕核运动,其轨道为球面,而p电子在哑铃形曲面上运动 |
D.114号元素是位于p区的金属元素,价电子排布式为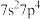 |
您最近半年使用:0次
4 . 下列说法正确的是
①基态碳原子电子排布式 违反了洪特规则
违反了洪特规则
②最外层电子数为 的元素都在元素化学性质都相似
的元素都在元素化学性质都相似
③充有氖气的霓虹灯管通电时会发出红光的主要原因,是电子由基态向激发态跃迁时吸收除红光以外的光
④某价层电子排布为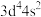 的基态原子,该元素位于周期表中第四周期第ⅥB族
的基态原子,该元素位于周期表中第四周期第ⅥB族
⑤电子云图中的小黑点的疏密程度表示电子在原子核外单位体积内出现概率的大小
①基态碳原子电子排布式
 违反了洪特规则
违反了洪特规则②最外层电子数为
 的元素都在元素化学性质都相似
的元素都在元素化学性质都相似③充有氖气的霓虹灯管通电时会发出红光的主要原因,是电子由基态向激发态跃迁时吸收除红光以外的光
④某价层电子排布为
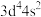 的基态原子,该元素位于周期表中第四周期第ⅥB族
的基态原子,该元素位于周期表中第四周期第ⅥB族⑤电子云图中的小黑点的疏密程度表示电子在原子核外单位体积内出现概率的大小
| A.③⑤ | B.①②⑤ | C.②③④ | D.①⑤ |
您最近半年使用:0次
5 . 按要求回答下列问题:
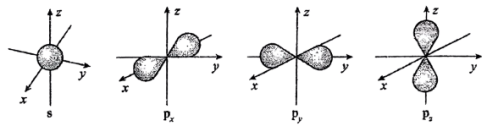
(1)如图是s能级和p能级的电子云轮廓图,试回答问题。______ 形,每个p能级有______ 个原子轨道。
(2)按要求作答:
①画出氯原子结构示意图______ ;
②写出基态O核外电子排布式为:______ ;
③写出基态N的原子轨道表示式:______ ;
(3)Sm的价层电子排布式为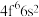 ,则
,则 价层电子排布式为
价层电子排布式为______ 。
(1)如图是s能级和p能级的电子云轮廓图,试回答问题。
(2)按要求作答:
①画出氯原子结构示意图
②写出基态O核外电子排布式为:
③写出基态N的原子轨道表示式:
(3)Sm的价层电子排布式为
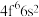 ,则
,则 价层电子排布式为
价层电子排布式为
您最近半年使用:0次
名校
解题方法
6 . 我国科学家利用锰簇催化剂(Mn4CaOx,x代表氧原子数)解密光合作用。锰簇的可逆结构异构化反应如图:
(1)基态钙原子中能量最高的电子所占据原子轨道的电子云轮廓图为_______ 形。
(2)已知:在元素周期表中Mn、Cr相邻,第二电离能与第一电离能之差较小的是_______ (填“Mn”或“Cr”),理由是_______ 。
(3)在上述异构化反应中,1molA中由Mn形成的σ键有_______ mol。
(4)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示:_______ ,距离Mn原子最近的Mn原子有_______ 个。
②以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。在MnS晶胞坐标系中,1号S原子坐标为(0,0,0),3号S原子坐标为(1,1,1),则2号S原子坐标为_______ 。
③已知:MnS晶体的密度为ρg·cm3, 为阿伏加德罗常数的值,则MnS晶胞中阴、阳离子最近距离为
为阿伏加德罗常数的值,则MnS晶胞中阴、阳离子最近距离为_______ pm(列出计算式即可)。

(1)基态钙原子中能量最高的电子所占据原子轨道的电子云轮廓图为
(2)已知:在元素周期表中Mn、Cr相邻,第二电离能与第一电离能之差较小的是
(3)在上述异构化反应中,1molA中由Mn形成的σ键有
(4)MnS晶胞与NaCl晶胞属于同种类型,MnS晶胞结构如图所示:

②以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。在MnS晶胞坐标系中,1号S原子坐标为(0,0,0),3号S原子坐标为(1,1,1),则2号S原子坐标为
③已知:MnS晶体的密度为ρg·cm3,
 为阿伏加德罗常数的值,则MnS晶胞中阴、阳离子最近距离为
为阿伏加德罗常数的值,则MnS晶胞中阴、阳离子最近距离为
您最近半年使用:0次
7 . 下列说法中错误的是
A.破损的 晶体放入饱和 晶体放入饱和 溶液中会自动变成规则的多面体 溶液中会自动变成规则的多面体 |
| B.电子云通常是用小黑点来表示电子出现的概率 |
| C.某固体是否是晶体,可利用X射线衍射判断 |
D.处于最低能量状态的原子叫基态原子, 过程中形成的是发射光谱 过程中形成的是发射光谱 |
您最近半年使用:0次
2024-04-28更新
|
54次组卷
|
2卷引用:江西省赣州市十八县(市)24校2023-2024学年高二下学期期中考试化学试题
8 . 化学用语是化学学科独特的语言,下列化学用语表示正确的是
A. 的 的 模型: 模型: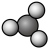 |
B. 的电子式: 的电子式: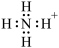 |
C.基态氧原子的 的电子云轮廓图: 的电子云轮廓图: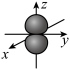 |
D.基态 原子的价层电子轨道表示式: 原子的价层电子轨道表示式: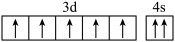 |
您最近半年使用:0次
名校
解题方法
9 . 研究发现,在饮用水、食物或牙膏中添加氟化物,能起到预防龋齿的作用。这是因为氟离子能与羟基磷灰石发生反应,生成氟磷灰石[ ],下列说法错误的是
],下列说法错误的是
 ],下列说法错误的是
],下列说法错误的是A. 的空间结构:正四面体形 的空间结构:正四面体形 |
| B.基态O原子核外电子的运动状态有8种 |
C. 比 比 稳定,是因为 稳定,是因为 分子间存在氢键 分子间存在氢键 |
D.基态 原子中,电子占据最高能级的电子云轮廓图为球形 原子中,电子占据最高能级的电子云轮廓图为球形 |
您最近半年使用:0次
2024-04-26更新
|
88次组卷
|
3卷引用:广西壮族自治区桂林市联考2023-2024学年高二下学期3月月考化学试题
10 . 化学与生活、生产息息相关,从化学视角认识世界,下列说法错误 的是
| A.人工合成的芳香型碳环C10和C14,两者互为同素异形体 |
| B.“杯酚”分离C60和C70,体现了超分子“分子识别”的特性 |
| C.日常生活中的焰火和霓虹灯光,都与原子核外电子跃迁吸收能量有关 |
| D.黄山迎客松扎根于岩石缝,以惊人的韧性和刚强创造了奇迹,松木富含糖类 |
您最近半年使用:0次



