1 . 铅是一种金属元素,可用作耐酸腐蚀、蓄电池等的材料。其合金可作铅字、轴承、电缆包皮之用,还可做体育运动器材铅球等。
(1)铅元素位于元素周期表第六周期IVA。IVA中原子序数最小的元素的原子有_______ 种能量不同的电子,其次外层的电子云有_______ 种不同的伸展方向。
(2)与铅同主族的短周期元素中,其最高价氧化物对应水化物酸性最强的是______ (填化学式),气态氢化物沸点最低的是_____________ (填化学式)。
(3)配平下列化学反应方程式,把系数以及相关物质(写化学式)填写在空格上, 并标出电子转移的方向和数目。
__ PbO2+___ MnSO4+___ HNO3 →___ HMnO4+___ Pb(NO3)2+___ PbSO4↓+____ ____
(4)把反应后的溶液稀释到1 L,测出其中的Pb2+的浓度为0.6 mol·L-1,则反应中转移的电子数为_______ 个。
(5)根据上述反应,判断二氧化铅与浓盐酸反应的化学方程式正确的是_______
A. PbO2+4HCl→PbCl4+2H2O B. PbO2+4HCl→PbCl2+ Cl2↑+2H2O
C. PbO2+2HCl+2H+→PbCl2+2H2O D. PbO2+4HCl→PbCl2+2OH-
(1)铅元素位于元素周期表第六周期IVA。IVA中原子序数最小的元素的原子有
(2)与铅同主族的短周期元素中,其最高价氧化物对应水化物酸性最强的是
(3)配平下列化学反应方程式,把系数以及相关物质(写化学式)填写在空格上, 并标出电子转移的方向和数目。
(4)把反应后的溶液稀释到1 L,测出其中的Pb2+的浓度为0.6 mol·L-1,则反应中转移的电子数为
(5)根据上述反应,判断二氧化铅与浓盐酸反应的化学方程式正确的是
A. PbO2+4HCl→PbCl4+2H2O B. PbO2+4HCl→PbCl2+ Cl2↑+2H2O
C. PbO2+2HCl+2H+→PbCl2+2H2O D. PbO2+4HCl→PbCl2+2OH-
您最近一年使用:0次
解题方法
2 . 下列有关化学表达正确的是( )
A.CS2的比例模型: |
B.铍原子最外层的电子云图: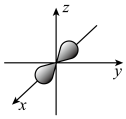 |
C.乙醇的球棍模型: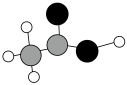 |
D.氮原子最外层轨道表示式: |
您最近一年使用:0次
2020-02-24更新
|
252次组卷
|
3卷引用:山东省济南市高新区新2019-2020学年高三化学一轮复习《物质结构与性质》专题测试
名校
解题方法
3 . 大型客机燃油用四乙基铅[Pb(CH2CH3)4])做抗震添加剂,但皮肤长期接触四乙基铅对身体健康有害,可用硫基乙胺(HSCH2CH2NH2)和KMnO4清除四乙基铅。
(1)碳原子核外电子的空间运动状态有______ 种,基态锰原子的外围电子排布式为___ ,该原子能量最高的电子的电子云轮廓图形状为________ 。
(2)N、C和Mn电负性由大到小的顺序为____________ 。
(3)HSCH2CH2NH2中C的杂化方式为_____ ,其中NH2-空间构型为____ ;N和P的价电子相同,但磷酸的组成为H3PO4,而硝酸的组成不是H3NO4,其原因是_______ 。
(4)Pb(CH2CH3)4是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于_____ 晶体。已知Pb(CH2CH3)4晶体的堆积方式如下。
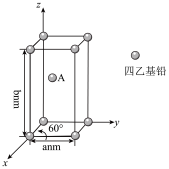
Pb(CH2CH3)4]在xy平面上的二维堆积中的配位数是___ ,A分子的坐标参数为_____ ;设阿伏加 德罗常数为NA/mol,Pb(CH2CH3)4]的摩尔质量为Mg/mol,则Pb(CH2CH3)4]晶体的密度是_____ g/cm3 (列出计算式即可)。
(1)碳原子核外电子的空间运动状态有
(2)N、C和Mn电负性由大到小的顺序为
(3)HSCH2CH2NH2中C的杂化方式为
(4)Pb(CH2CH3)4是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于

Pb(CH2CH3)4]在xy平面上的二维堆积中的配位数是
您最近一年使用:0次
2020-02-24更新
|
654次组卷
|
3卷引用:四川省遂宁市第二中学2020届高三上学期第二次高考模拟理综化学试题
四川省遂宁市第二中学2020届高三上学期第二次高考模拟理综化学试题(已下线)专题6.4 物质结构与性质(选考)(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升北京专家2020届高三高考模拟试卷(二)化学试题
解题方法
4 . 下列有关说法不正确的是
A.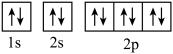 可表示单核10电子粒子基态时的电子排布 可表示单核10电子粒子基态时的电子排布 |
| B.电子仅在激发态跃迁到基态时才会产生原子光谱 |
| C.同一原子能层越高,s电子云的半径越大 |
| D.N、O、F电负性逐渐增大 |
您最近一年使用:0次
2020-02-24更新
|
167次组卷
|
2卷引用:天津市部分区2020届高三上学期期中练习 化学
5 . 下列有关电子云和原子轨道的说法正确的是( )
| A.原子核外的电子像云雾一样笼罩在原子核周围,故称电子云 |
| B.s轨道呈球形,处在该轨道上的电子只能在球壳内运动 |
| C.p轨道呈哑铃形,在空间有两个伸展方向 |
| D.与s原子轨道电子相同,p原子轨道电子的平均能量随能层的增大而增大 |
您最近一年使用:0次
2020-02-12更新
|
121次组卷
|
5卷引用:2020届高三化学二轮物质结构题型专攻——核外电子排布和运动【选择基础专练】
2020届高三化学二轮物质结构题型专攻——核外电子排布和运动【选择基础专练】云南省昭通市永善县第二中学2019—2020学年高二上学期期末考试化学试题(已下线)1.1.3 电子云与原子轨道 泡利原理与洪特规则 能量最低原理-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)黑龙江省哈尔滨市宾县第二中学2021-2022学年高二6月月考化学试题1.1原子结构模型(课后)-鲁科版选择性必修2
名校
解题方法
6 . 下列叙述中,正确的是
| A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子 |
| B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子 |
| C.如果某一基态原子3p轨道上仅有2个电子,它们自旋方向必然相反 |
| D.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高 |
您最近一年使用:0次
2020-01-07更新
|
73次组卷
|
6卷引用:2020届高三化学选修三二轮专题复习——原子核外运动的特点
7 . 镁、铝、铁是三种重要金属,它们的单质和化合物应用十分广泛。回答下列问题:
(1)镁、铝第一电离能大小的关系是I1(Mg)_________ I1(Al),金属镁、铝熔点大小关系是Mg_________ Al。(填“大于”、“等于”或“小于”)
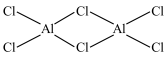
(2)氯化铝加热时易升华,实验测得铝元素与氯元素形成化合物的实际组成为Al2Cl6,其结构简式如图所示。其中处于中间的Al原子杂化轨道类型为_________ 杂化,分子中所有原子_________ (能、不能)在同一平面上。
(3)硝酸铁和尿素在乙醇中生成[Fe(H2NCONH2)6](NO3)3三硝酸六尿素合铁 。产物是一种重要的配合物,用作有机铁肥,简称铁氮肥。基态Fe3+的核外电子排布式为
。产物是一种重要的配合物,用作有机铁肥,简称铁氮肥。基态Fe3+的核外电子排布式为____________ 。尿素分子中 键与
键与 键的数目之比为
键的数目之比为_______ 。NO3-的空间构型为_________ ,经测定N2O5晶体中存在NO2+和NO3-,NO2+中氮原子为_________ 杂化。
(4)碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示。晶体中与相邻铁原子距离相等且最近的铁原子有________ 个,该物质的化学式为_________ 。若晶体密度为dg/cm3,则晶胞中最近的两个碳原子的距离为___________ pm(阿伏加 德罗常数的值为NA表示,写出简化后的计算式即可)。

(1)镁、铝第一电离能大小的关系是I1(Mg)
(2)氯化铝加热时易升华,实验测得铝元素与氯元素形成化合物的实际组成为Al2Cl6,其结构简式如图所示。其中处于中间的Al原子杂化轨道类型为

(3)硝酸铁和尿素在乙醇中生成[Fe(H2NCONH2)6](NO3)3三硝酸六尿素合铁
 。产物是一种重要的配合物,用作有机铁肥,简称铁氮肥。基态Fe3+的核外电子排布式为
。产物是一种重要的配合物,用作有机铁肥,简称铁氮肥。基态Fe3+的核外电子排布式为 键与
键与 键的数目之比为
键的数目之比为(4)碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示。晶体中与相邻铁原子距离相等且最近的铁原子有

您最近一年使用:0次
2020-01-07更新
|
147次组卷
|
2卷引用:2020届高三化学选修三二轮专题复习——晶体的缺陷及其应用
名校
8 . 符号“2p”没有给出的信息是( )
| A.能级 | B.电子层 |
| C.电子亚层 | D.电子云在空间的伸展方向 |
您最近一年使用:0次
2019-12-29更新
|
270次组卷
|
5卷引用:2019-2020学年上海各区(16区)高三化学一模选择题汇编-物质的组成与结构
名校
解题方法
9 . 含硼、氮、磷的化合物有许多重要用途,如:(CH3)3N、Cu3P、磷化硼等。回答下列问题:
(1)基态B原子电子占据最高能级的电子云轮廓图为_____ ;基态Cu+的核外电子排布式为_____ 。
(2)化合物(CH3)3N分子中N原子杂化方式为_____ ,该物质能溶于水的原因是_____ 。
(3)PH3分子的键角小于NH3分子的原因是_____ ;亚磷酸(H3PO3)是磷元素的一种含氧酸,与NaOH反应只生成NaH2PO3和Na2HPO3两种盐,则H3PO3分子的结构式为_____ 。
(4)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图1所示:
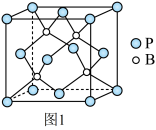
①在一个晶胞中磷原子的配位数为_____ 。
②已知磷化硼晶体的密度为ρg/cm3,阿伏加 德罗常数为NA,则B-P键长为_____ 。
(1)基态B原子电子占据最高能级的电子云轮廓图为
(2)化合物(CH3)3N分子中N原子杂化方式为
(3)PH3分子的键角小于NH3分子的原因是
(4)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图1所示:

①在一个晶胞中磷原子的配位数为
②已知磷化硼晶体的密度为ρg/cm3,阿伏加 德罗常数为NA,则B-P键长为
您最近一年使用:0次
10 . 研究者预想合成一个纯粹由氮组成的新物种—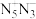 ,若
,若 离子中每个氮原子均满足8电子结构,下列关于含氮微粒的表述正确的是
离子中每个氮原子均满足8电子结构,下列关于含氮微粒的表述正确的是
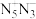 ,若
,若 离子中每个氮原子均满足8电子结构,下列关于含氮微粒的表述正确的是
离子中每个氮原子均满足8电子结构,下列关于含氮微粒的表述正确的是A. 有24个电子 有24个电子 | B.N原子中未成对电子的电子云形状相同 |
C.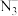 质子数为20 质子数为20 | D. 中N原子间形成离子键 中N原子间形成离子键 |
您最近一年使用:0次



