1 . 国产巨型载人飞艇AS700、歼20战机和C919国产大飞机等大国重器让世界瞩目。金属材料和复合材料在航空航天工业中具有重要的应用。回答下列问题:
(1)基态钛原子价层电子排布图为______ 。原子中运动电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的则用
表示,与之相反的则用 表示,称为电子的自旋磁量子数。对于基态钛原子,其价层电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态钛原子,其价层电子自旋磁量子数的代数和为______ 。
(2)以 为连续基体的碳陶瓷是一种复合材料,可应用于制造歼20。结构如图所示:
为连续基体的碳陶瓷是一种复合材料,可应用于制造歼20。结构如图所示:______ (填标号)。 晶体中硅原子与最近碳原子间距离为
晶体中硅原子与最近碳原子间距离为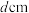 ,则硅原子与最近的硅原子间距离为
,则硅原子与最近的硅原子间距离为______  ,一个硅原子周围与其最近的硅原子的数目为
,一个硅原子周围与其最近的硅原子的数目为______ 。 晶体的密度为
晶体的密度为______  (用含有
(用含有 的式子表示)。
的式子表示)。
(1)基态钛原子价层电子排布图为
 表示,与之相反的则用
表示,与之相反的则用 表示,称为电子的自旋磁量子数。对于基态钛原子,其价层电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态钛原子,其价层电子自旋磁量子数的代数和为(2)以
 为连续基体的碳陶瓷是一种复合材料,可应用于制造歼20。结构如图所示:
为连续基体的碳陶瓷是一种复合材料,可应用于制造歼20。结构如图所示:
a.  b.
b.
c. 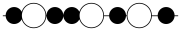 d.
d.
 晶体中硅原子与最近碳原子间距离为
晶体中硅原子与最近碳原子间距离为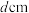 ,则硅原子与最近的硅原子间距离为
,则硅原子与最近的硅原子间距离为 ,一个硅原子周围与其最近的硅原子的数目为
,一个硅原子周围与其最近的硅原子的数目为 晶体的密度为
晶体的密度为 (用含有
(用含有 的式子表示)。
的式子表示)。
您最近一年使用:0次
2 . 近年来,我国以风电、光伏发电为代表的新能源发展成效显著,推动了绿色生态文明的建设。回答下列问题:
(1)光伏发电的传统材料是硅,基态硅原子核外电子有______ 种空间运动状态,与硅同主族的第四周期元素基态原子的价层电子排布式为______ 。
(2) 与N—甲基咪唑
与N—甲基咪唑 反应可以得到
反应可以得到 ,其结构如图1所示。
,其结构如图1所示。
①已知 —甲基咪唑分子具有类似苯环的结构,则该分子中存在的大
—甲基咪唑分子具有类似苯环的结构,则该分子中存在的大 键应表示为
键应表示为______ ,连甲基的 原子的价层孤电子对占据
原子的价层孤电子对占据______ 轨道。
②每个 含有个
含有个 键;除
键;除 键外,
键外, 中还存在的化学键有
中还存在的化学键有______ (填标号)。
A.极性键B.非极性键C.离子键D.范德华力E.配位键
(3)武汉大学闵杰课题组研究出一种小分子有机光伏材料,结构如图2所示。 由大到小的顺序为
由大到小的顺序为______ (用元素符号表示)。
② 是微电子工业中一种优良的等离子蚀刻气体,其分子空间构型与
是微电子工业中一种优良的等离子蚀刻气体,其分子空间构型与 相似,键角
相似,键角
______  (填“大于”“等于”或“小于”),原因是
(填“大于”“等于”或“小于”),原因是______ 。
(1)光伏发电的传统材料是硅,基态硅原子核外电子有
(2)
 与N—甲基咪唑
与N—甲基咪唑 反应可以得到
反应可以得到 ,其结构如图1所示。
,其结构如图1所示。
①已知
 —甲基咪唑分子具有类似苯环的结构,则该分子中存在的大
—甲基咪唑分子具有类似苯环的结构,则该分子中存在的大 键应表示为
键应表示为 原子的价层孤电子对占据
原子的价层孤电子对占据②每个
 含有个
含有个 键;除
键;除 键外,
键外, 中还存在的化学键有
中还存在的化学键有A.极性键B.非极性键C.离子键D.范德华力E.配位键
(3)武汉大学闵杰课题组研究出一种小分子有机光伏材料,结构如图2所示。
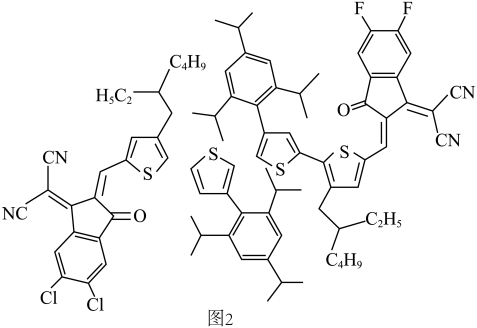
 由大到小的顺序为
由大到小的顺序为②
 是微电子工业中一种优良的等离子蚀刻气体,其分子空间构型与
是微电子工业中一种优良的等离子蚀刻气体,其分子空间构型与 相似,键角
相似,键角
 (填“大于”“等于”或“小于”),原因是
(填“大于”“等于”或“小于”),原因是
您最近一年使用:0次
3 . 磷酸亚铁锂( )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:
(1)在周期表中,与Li化学性质最相似的邻族元素是_______ ,画出基态O原子的价电子轨道表示式为_______ 。基态P原子电子占据最高能级的电子云轮廓图为_______ 形。
(2)原子核外电子有两种相反的自旋状态,分别用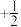 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为_______ 。
(3)P的第一电离能与同周期相邻元素相比大小关系为_______ (用元素符号和“>”表示),原因是_______ 。
(4)Fe元素位于周期表的_______ 区。已知: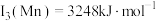 ,
,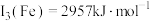 。第三电离能
。第三电离能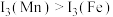 ,其主要原因是
,其主要原因是_______ 。
 )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:(1)在周期表中,与Li化学性质最相似的邻族元素是
(2)原子核外电子有两种相反的自旋状态,分别用
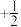 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为(3)P的第一电离能与同周期相邻元素相比大小关系为
(4)Fe元素位于周期表的
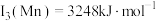 ,
,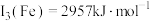 。第三电离能
。第三电离能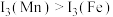 ,其主要原因是
,其主要原因是
您最近一年使用:0次
2023-01-13更新
|
232次组卷
|
3卷引用:山东省临沂第一中学2021-2022学年高二上学期期末检测化学试题
名校
解题方法
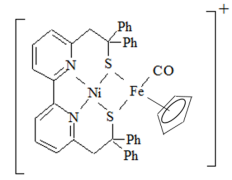
4 . (1)Ni2+和Fe2+可形成如图所示的配合物离子,其中铁的一个配体为茂环阴离子( ),该配体以π电子参与配位,其中Ni2+的价电子排布式为
),该配体以π电子参与配位,其中Ni2+的价电子排布式为______ ,配合物离子中铁周围的价电子数共有______ 个,S元素的杂化方式为______ ,该配合物离子中的 (Ⅰ)和气态
(Ⅰ)和气态 分子(Ⅱ)的三键相比,键长较长的为
分子(Ⅱ)的三键相比,键长较长的为______ (用Ⅰ或Ⅱ表示)。
(2)CsAuCl3的结构不能表示为CsCl·AuCl2,实际上可看作一种阳离子和两种阴离子按照个数比为2∶1∶1形成的,这两种阴离子形状分别是直线型和平面正方形,在平面正方形离子中Au的化合价为______ 。基态Cs原子中电子占据的能量最高的轨道是______ ,能量最低的空轨道是______ 。
(3)如果m个原子有相互平行的p轨道,这些p轨道中共有n个电子(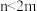 ),则可以形成大π键,表示为
),则可以形成大π键,表示为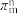 ,则SO2分子中的大π键可以表示为
,则SO2分子中的大π键可以表示为______ 。
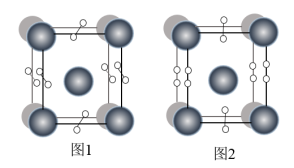
(4)如图表示的是某物质的两种结构的晶胞(大球表示的是K原子,小球表示O原子)图1中的O2单元空间取向有______ 种。若K之间底面上的最近距离为a pm,竖直方向上为c pm,图2表示的晶体密度为______  ,(NA表示阿伏加德罗常数)
,(NA表示阿伏加德罗常数)
 ),该配体以π电子参与配位,其中Ni2+的价电子排布式为
),该配体以π电子参与配位,其中Ni2+的价电子排布式为 (Ⅰ)和气态
(Ⅰ)和气态 分子(Ⅱ)的三键相比,键长较长的为
分子(Ⅱ)的三键相比,键长较长的为
(2)CsAuCl3的结构不能表示为CsCl·AuCl2,实际上可看作一种阳离子和两种阴离子按照个数比为2∶1∶1形成的,这两种阴离子形状分别是直线型和平面正方形,在平面正方形离子中Au的化合价为
(3)如果m个原子有相互平行的p轨道,这些p轨道中共有n个电子(
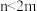 ),则可以形成大π键,表示为
),则可以形成大π键,表示为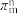 ,则SO2分子中的大π键可以表示为
,则SO2分子中的大π键可以表示为(4)如图表示的是某物质的两种结构的晶胞(大球表示的是K原子,小球表示O原子)图1中的O2单元空间取向有
 ,(NA表示阿伏加德罗常数)
,(NA表示阿伏加德罗常数)
您最近一年使用:0次
2021-01-03更新
|
582次组卷
|
4卷引用:山东省菏泽市单县第二中学2023届高三第一次模拟考试化学试题
山东省菏泽市单县第二中学2023届高三第一次模拟考试化学试题八省八校(T8联考)2020-2021学年高三上学期第一次联考化学试题(华中师大一附中)(已下线)大题08 物质结构与性质(一)(选修)-【考前抓大题】备战2021年高考化学(全国通用)湖南省常德市汉寿县第一中学2022届高三下学期第三次模考化学试题
解题方法
5 . 已知反应3NaH+Fe2O3 2Fe+3NaOH。
2Fe+3NaOH。
(1)基态Fe原子核外共有__ 种运动状态不相同的电子;Fe3+的价电子排布图为__ 。
(2)1molNaOH含有σ键数目为__ ;Fe3+可以和SCN-形成配合物,该反应是典型的可逆反应,说明配位原子配位能力__ (填“强”或“弱”)。
(3)上述反应中含Na的化合物晶体类型均为__ 晶体。
 2Fe+3NaOH。
2Fe+3NaOH。(1)基态Fe原子核外共有
(2)1molNaOH含有σ键数目为
(3)上述反应中含Na的化合物晶体类型均为
您最近一年使用:0次



