名校
1 . 下列由电子排布式或排布图所得的结论错误的是
| 选项 | 电子排布式 | 结论 |
| A | 1s22s22p 2p 2p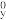 2p 2p | 违背洪特规则 |
| B | 1s22s22p63s23p63d3 | 违背能量最低原理 |
| C | N的电子排布图: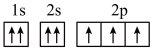 | 违背泡利原理 |
| D | 1s22s22p63s23p63d54s1 | 违背能量最低原理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-05-12更新
|
806次组卷
|
11卷引用:吉林省长春市第二十九中学2019-2020学年高二下学期线上检测化学试题
吉林省长春市第二十九中学2019-2020学年高二下学期线上检测化学试题鲁科版2019选择性必修2第1章 原子结构与元素性质 第1章学科素养提升(人教版2019)选择性必修2第一章 原子结构与性质 学科素养提升福建省泉州科技中学2020-2021学年高二下学期第一次月考化学试题辽宁省大石桥市第三高级中学2020-2021学年高二下学期期初考试化学试题山西省怀仁市大地学校2020-2021学年高二下学期第三次月考化学试题黑龙江省哈尔滨市第三十二中学2019-2020学年高二下学期期中考试化学试题黑龙江省哈尔滨师范大学附属中学2021-2022学年高二下学期期中考试化学试题吉林省长春市十一高中2021-2022学年高二下学期第二学程考试化学试题河南省温县第一高级中学2022-2023学年高二下学期第一次月考化学试题甘肃省张掖市 高台县第一中学2022-2023学年高二下学期3月月考化学试题
名校
2 . 下列关于物质的组成、结构或性质的叙述中,正确的是
①HF的稳定性很强,是因为其分子间能形成氢键
②基态原子价电子排布式为(n-1)d6~8ns2的元素属于第ⅧB族
③能层为1时,有自旋方向相反的两个轨道
④“量子化”就是连续的意思,微观粒子运动均有此特点
⑤前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有5种
⑥次氯酸分子的电子式:
⑦氯离子与硫离子的核外电子排布相同,都是1s22s22p63s23p6,两粒子的3p能级上的电子离核的距离相同
⑧S2-、Cl-、K+、Na+半径逐渐减小
⑨最外层有3个未成对电子的原子一定属于主族元素
①HF的稳定性很强,是因为其分子间能形成氢键
②基态原子价电子排布式为(n-1)d6~8ns2的元素属于第ⅧB族
③能层为1时,有自旋方向相反的两个轨道
④“量子化”就是连续的意思,微观粒子运动均有此特点
⑤前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有5种
⑥次氯酸分子的电子式:

⑦氯离子与硫离子的核外电子排布相同,都是1s22s22p63s23p6,两粒子的3p能级上的电子离核的距离相同
⑧S2-、Cl-、K+、Na+半径逐渐减小
⑨最外层有3个未成对电子的原子一定属于主族元素
| A.①③④⑦⑧ | B.⑤⑧⑨ | C.②③⑤⑥⑦⑨ | D.②⑦⑧⑨ |
您最近一年使用:0次
3 . 以下是一些同学书写的某些原子的2p能级或3d能级中的电子排布情况,其中违反了洪特规则的是( )
A. 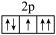 | B. 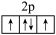 |
C. 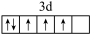 | D. 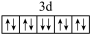 |
您最近一年使用:0次
解题方法
4 . A、B、C三种短周期元素,它们的原子序数依次增大。A元素原子的核外p电子数比s电子数少1,B元素原子核外有4种能级,且全部充满电子;C元素的主族序数与周期数的差为4。
(1)A的基态原子中能量最高的电子,其电子云在空间有________ 个方向,原子轨道呈________ 形。
(2)某同学推断B基态原子的核外电子排布为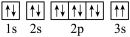 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了_____________ 。
(3)C位于______ 族_____ 区,价电子排布式为_________ 。
(1)A的基态原子中能量最高的电子,其电子云在空间有
(2)某同学推断B基态原子的核外电子排布为
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(3)C位于
您最近一年使用:0次
解题方法
5 . 下列有关多电子原子的叙述中正确的是()
| A.在一个多电子原子中,不可能有两个运动状态完全相同的电子 |
| B.在一个多电子原子中,不可能有两个能量相同的电子 |
| C.Sc基态原子的电子排布式1s22s22p63s23p63d3符合构造原理(能量最低原理) |
| D.某个多电子原子的3p能级上仅有两个电子,它们的自旋状态必须相反 |
您最近一年使用:0次
6 . 下列轨道表示式所表示的元素原子中,其能量处于最低状态的是( )
A.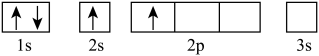 |
B.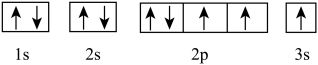 |
C.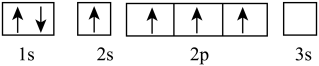 |
D.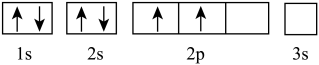 |
您最近一年使用:0次
7 . 以下列出的是一些原子的2p能级和3d能级中电子的排布情况。试判断,违反了泡利不相容原理的是 ___________ (填序号,下同),违反了洪特规则的是 _______ 。
① ②
②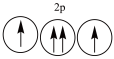 ③
③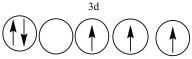 ④
④ ⑤
⑤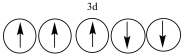
①
 ②
② ③
③ ④
④ ⑤
⑤
您最近一年使用:0次
8 . 下列轨道表示式表示的元素原子中,能量处于最低状态的是( )
A. 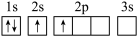 | B. 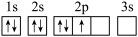 |
C. 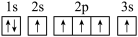 | D. 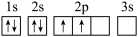 |
您最近一年使用:0次
2020-04-09更新
|
196次组卷
|
5卷引用:上海市民星中学2019—2020学年高三上学期期中考试化学试题
9 . H、C、N、O、V(钒)五种元素形成的某分子结构如图所示,下列说法错误是
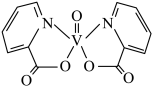

| A.N原子核外存在3种不同能量的电子 |
B.基态V原子的价电子轨道表示式为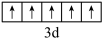 |
| C.基态O原子,电子占据的最高能级符号为2p |
| D.基态C、N两种原子中,核外存在相同对数自旋方向相反的电子 |
您最近一年使用:0次
2020-04-03更新
|
246次组卷
|
6卷引用:山东省威海市文登区2018-2019学年高二下学期期末考试化学试题
名校
解题方法
10 . 铜是人类最早使用的金属之一,其单质及化合物具有广泛的用途。
(1)基态铜原子核外有________ 对自旋相反的电子。
(2)青铜是铜与锡或铅等元素按一定比例熔铸而成的合金。第一电离能I1(Sn)____________ I1(Pb)(填“大于”或“小于”)。
(3)新制的Cu(OH)2能够溶解于浓氨水中,反应的离子方程式是____________________________________ ;
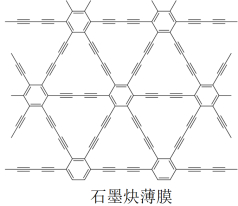
(4)利用铜片表面催化反应,我国研究人员用六炔基苯为原料,在世界上首次通过化学方法获得全碳材料—石墨炔薄膜(结构片段如图所示),开辟了人工化学合成碳同素异形体的先例。石墨炔中碳原子_________________________ 的杂化方式。
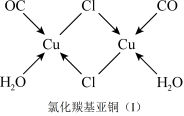
(5)CuCl的盐酸溶液能吸收CO形成氯化羰基亚铜(I),可用于定量测定气体混合物中CO的含量。氯化羰基亚铜(I)中含___________ σ键数目。
(6)Cu2O可用于半导体材料。
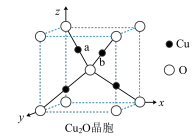
①Cu2O晶胞(如图所示)中,O原子的配位数为________________ ;a位置Cu+坐标为(0.25,0.25,0.75),则b位置Cu+坐标_______________________ 。
②Cu2S与Cu2O具有相似晶体结构,则两者的熔点是Cu2O比Cu2S的_________ (填“高”或“低”),请解释原因___________________ 。
(1)基态铜原子核外有
(2)青铜是铜与锡或铅等元素按一定比例熔铸而成的合金。第一电离能I1(Sn)
(3)新制的Cu(OH)2能够溶解于浓氨水中,反应的离子方程式是
(4)利用铜片表面催化反应,我国研究人员用六炔基苯为原料,在世界上首次通过化学方法获得全碳材料—石墨炔薄膜(结构片段如图所示),开辟了人工化学合成碳同素异形体的先例。石墨炔中碳原子



(5)CuCl的盐酸溶液能吸收CO形成氯化羰基亚铜(I),可用于定量测定气体混合物中CO的含量。氯化羰基亚铜(I)中含
(6)Cu2O可用于半导体材料。
①Cu2O晶胞(如图所示)中,O原子的配位数为
②Cu2S与Cu2O具有相似晶体结构,则两者的熔点是Cu2O比Cu2S的
您最近一年使用:0次
2020-04-02更新
|
308次组卷
|
3卷引用:山东省潍坊市2020届高三下学期第三次线上检测化学试题



